Dr. José María Huguet Malaves / Dra. Lucía Ruiz Sánchez josemahuguet@gmail.com / luciar79@hotmail.com

Dr. Jose María Huguet Malaves y Dra. Lucía Ruiz Sánchez
Fuente: Drs. Huguet Malaves y Ruiz Sánchez
INTRODUCCIÓN
Los inhibidores del factor de necrosis tumoral (TNF), incluido el infliximab (IFX), han mejorado significativamente el manejo de la Enfermedad Inflamatoria Intestinal (EII), tanto en monoterapia como en combinación con inmunomoduladores (IM)1. El biosimilar intravenoso (IV) de IFX CT-P13 ha demostrado una eficacia, seguridad e inmunogenicidad comparables a las del IFX original, tanto en estudios reales como aleatorizados2,3, y se ha demostrado que el cambio entre productos es seguro y eficaz4.
Posteriormente, la Agencia Europea del Medicamento (EMA) aprobó una formulación subcutánea (SC) de CT-P13, distinta de la formulación IV, para la indicación en adultos en colitis ulcerosa (CU) y en enfermedad de Crohn (EC). Esta formulación se ha considerado biobetter del biosimilar CT-P13, dado que permite una autoadministración subcutánea quincenal, unos niveles séricos más estables, mejora el control de la enfermedad y facilita estrategias más personalizadas5-8. El cambio de CT-P13 IV a SC se ha mostrado con una eficacia favorable, seguridad, persistencia del tratamiento, baja inmunogenicidad y buena aceptación por parte del paciente a los 6 y 12 meses9-11. Además, varias publicaciones muestran que estos beneficios se mantienen a los 2 años del inicio del IFX SC12.
El objetivo de este artículo es presentar datos de persistencia a largo plazo (3 años) en una cohorte de práctica clínica real.
DISEÑO Y RESULTADOS PRINCIPALES DEL ESTUDIO
En 8 hospitales de Valencia realizamos un estudio prospectivo, observacional y multicéntrico en el que incluimos pacientes con EII tratados con IFX SC como parte de la práctica clínica. En total se incluyeron 74 pacientes en el estudio, con una edad media de 42 años, y el 53% de los pacientes eran hombres. Las principales razones para iniciar IFX IV fueron el fracaso en el tratamiento convencional en el 45% de los casos y corticodependencia en el 18,7%. La media de años desde el diagnóstico fue de 10,38 ± 7,54, mientras que la media de meses en tratamiento con infliximab endovenoso previos al cambio al subcutáneo fue de 35,84 ± 34,13 meses. El 51,4% de los pacientes tenían intensificación de IFX IV antes del cambio a subcutáneo (dosis > de 5 mg/kg cada 8 semanas, ya fuera por aumento de dosis o acortamiento del intervalo de administración).
Los cambios en los marcadores inflamatorios y los niveles de SC CT-P13 entre el inicio y el final del seguimiento se resumen en la Tabla 1. El único cambio significativo fue un aumento en los niveles de valle de SC CT-P13 al final del seguimiento, con resultados similares en los subgrupos de CU y EC. La actividad clínica se mantuvo estable durante todo el seguimiento (medida por índice de Harvey-Bradshaw para EC y la puntuación parcial de Mayo para CU), con la mayoría de los pacientes manteniendo la remisión (85% para CU y 97% para EC).
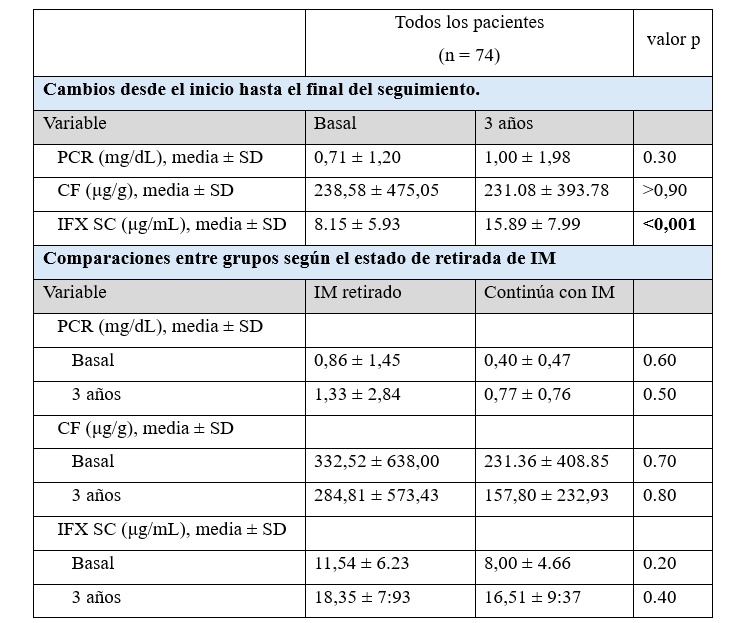
Tabla 1. Cambios en los marcadores inflamatorios y los niveles plasmáticos de IFX SC
PCR: proteína C-reactiva; IFX: infliximab; CF: calprotectina fecal; IM: terapia inmunomoduladora; SC: subcutánea; SD: desviación estándar
Adaptada de referencia 24
El uso concomitante de IM disminuyó de 38 pacientes (34,2%) al inicio a 15 (13,5%) al final del seguimiento. Según el grupo de pacientes a los que se les suspendió o no el IM, no se observaron diferencias significativas en los marcadores inflamatorios ni en las concentraciones de IFX SC.
Los niveles de valle de IFX SC aumentaron significativamente desde el inicio hasta el final del seguimiento tanto en pacientes que recibieron dosis estándar (6,28 ± 5,31 a 16,22 ± 8,38 μg/mL, p <0,001) como en aquellos previamente intensificados (10,08 ± 6,00 a 15,58 ± 7,74 μg/mL, p = 0,003).
PERSISTENCIA DEL TRATAMIENTO
La persistencia del tratamiento se definió como el tiempo desde el inicio del IFX SC hasta la suspensión por cualquier motivo. La discontinuación fue debida a la falta de eficacia, eventos adversos o a la decisión del paciente o el médico.
La persistencia del fármaco a los 3 años fue del 88% si consideramos la suspensión por pérdida de eficacia o eventos adversos y del 80% si consideramos cualquier motivo (Figura 1). Las razones de la retirada del IFX SC incluyeron pérdida de efectividad (6,7%), eventos adversos (5,4%), decisión del paciente de volver a la vía intravenosa (5,4%), decisión del paciente de suspender el tratamiento (4,0%) y pérdida de seguimiento (1,3%).
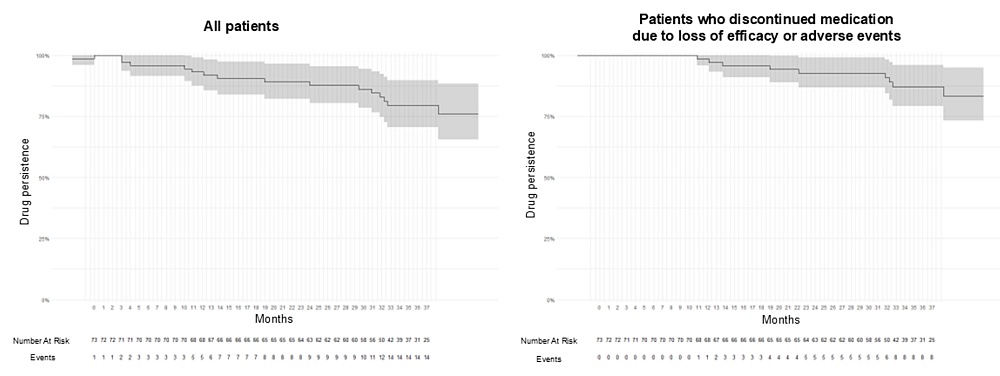
Figura 1. Persistencia del fármaco a los 3 años
Extraída de referencia 24
SEGURIDAD
Los eventos aversos se clasificaron como leves o moderados según su impacto en las actividades diarias. Los eventos adversos serios se definieron como eventos que eran fatales o potencialmente mortales, que requerían hospitalización o prolongación de la hospitalización, que causaban discapacidad o incapacidad persistentes, o que resultaban en anomalías congénitas o defectos congénitos. La relación causal entre la SC CT-P13 y cada evento adverso fue evaluada por el investigador conforme a criterios predefinidos13.
Un total de 14 pacientes (19%) experimentaron al menos un evento adverso, solo 4 pacientes suspendieron el fármaco debido a un evento adverso (5,4%). El evento más frecuente fue la infección en 5 pacientes (6,7%) y que conllevó la suspensión del tratamiento en 1 paciente (1,3%). Se observó lupus inducido por fármacos en 1 paciente al que se le retiró el tratamiento. Dos pacientes presentaron psoriasis paradójica que no motivó la suspensión del tratamiento. En otros dos pacientes se les retiró el tratamiento por eventos adversos (2,7%). No se observaron diferencias significativas en los resultados de seguridad entre los subgrupos de CU y EC.
DISCUSIÓN
Nuestros hallazgos son consistentes con la evidencia previa de ensayos clínicos y estudios de la vida real, y la amplían. El registro ENEIDA reportó una persistencia a un año del 92%14. En las extensiones abiertas del estudio LIBERTY, las tasas de persistencia a dos años fueron de aproximadamente el 75-80%, con concentraciones de IFX valle elevadas y estables (~20 µg/mL)12,15-19. De manera similar, el estudio de la vida real REMSWITCH-LT reportó una persistencia a dos años del 72% en pacientes que cambiaron de IFX intravenoso intensificado, con un aumento en los niveles valle de ~6-8 a ~17-20 µg/mL y una asociación significativa entre concentraciones más altas y la remisión20-21. En nuestra cohorte, la persistencia a los 3 años fue ligeramente superior (88% al excluir las interrupciones no relacionadas con la eficacia o la seguridad), con un aumento comparable en los niveles valle de IFX SC (de 8,15 ± 5,93 a 15,89 ± 7,99 µg/mL).
En todos los estudios, los resultados de seguridad fueron favorables, con bajas tasas de eventos adversos, en su mayoría leves, y sin nuevos problemas de seguridad, lo que refuerza la tolerabilidad a largo plazo del IFX SC.
También observamos una reducción en el uso concomitante de IM durante el seguimiento, sin un impacto aparente en los resultados clínicos, biomarcadores inflamatorios o niveles valle de CT-P13, en línea con datos previos del mundo real que sugieren que la monoterapia con SC podría ser factible en pacientes seleccionados22. Este hallazgo es clínicamente relevante dado el mayor riesgo de infección y tumores asociados con la terapia combinada23.
CONCLUSIONES
En esta cohorte prospectiva multicéntrica en el mundo real, el cambio de IFX IV a SC biosimilar CT-P13 se asoció con:
- Una persistencia sostenida en el tratamiento, control estable de la enfermedad y farmacocinética favorable durante 3 años.
- El tratamiento fue bien tolerado, sin identificar nuevas señales de seguridad.
- Se observó una reducción considerable en el uso concomitante de IM.
- En general, estos datos respaldan al CT-P13 SC como una opción de mantenimiento a largo plazo eficaz y conveniente en la práctica clínica rutinaria.
Bibliografía
1. Panaccione R, Ghosh S, Middleton S, et al. Combination therapy with infliximab and azathioprine is superior to monotherapy with either agent in ulcerative colitis. Gastroenterology 2014;146(2):392-400.e3. DOI:10.1053/j.gastro.2013.10.052
2. Albshesh A, Ben-Horin S. CT-P13: a review on a biosimilar to infliximab in the treatment of inflammatory bowel disease. Expert Opin Biol Ther 2019;19(10):971-8. DOI:10.1080/14712598.2019.1653848
3. Huguet JM, Cortés X, Bosca-Watts MM, et al. Real-world data on the infliximab biosimilar CT-P13 (Remsima®) in inflammatory bowel disease. World J Clin Cases 2021;9(36):11285-11299. DOI:10.12998/wjcc.v9.i36.11285
4. Chaparro M, Garre A, Guerra Veloz MF, et al. Effectiveness and Safety of the Switch from Remicade® to CT-P13 in Patients with Inflammatory Bowel Disease. J Crohns Colitis 2019;13(11):1380-6. DOI:10.1093/ecco-jcc/jjz070
5. Westhovens R, Yoo DH, Jaworski J, et al. Novel formulation of ct-p13 for subcutaneous administration in patients with rheumatoid arthritis: initial results from a phase i/iii randomised controlled trial. Ann Rheum Dis 2018;77(Suppl 2):315. Abstract THU0191. DOI:10.1136/annrheumdis-2018-eular.1810
6. Yoo D, Jaworski J, Matyska-Piekarska E, et al. A novel formulation of CT-P13 (infliximab biosimilar) for subcutaneous administration: 1-year results from a part 1 of phase I/III randomized controlled trial in patients with active rheumatoid arthritis. Ann Rheum Dis 2019;78 (Suppl 2):733. Abstract FRI0128. DOI:10.1136/annrheumdis-2019-eular.1094
7. Westhovens R, Wiland P, Zawadzki M, et al. A novel formulation of CT-P13 for subcutaneous administration: 30 week results from a part 2 of phase I/III randomized controlled trial in patients with rheumatoid arthritis. Ann Rheum Dis 2019;78 (Suppl 2):1158.2-9. Abstract SAT0170. DOI:10.1136/annrheumdis-2019-eular.612
8. Smith PJ, Critchley L, Storey D, et al. Efficacy and Safety of Elective Switching from Intravenous to Subcutaneous Infliximab [CT-P13]: A Multicentre Cohort Study. J Crohns Colitis 2022;16(9):1436-46. DOI:10.1093/ecco-jcc/jjac053
9. Schreiber S, Ben-Horin S, Leszczyszyn J, et al. Randomized Controlled Trial: Subcutaneous vs Intravenous Infliximab CT-P13 Maintenance in Inflammatory Bowel Disease. Gastroenterology 2021;160(7):2340-53. DOI:10.1053/j.gastro.2021.02.068
10. Chetwood JD, Tran Y, Subramanian S, et al. Intravenous Versus Subcutaneous Infliximab in Inflammatory Bowel Disease: A Systematic Review and Meta-analysis. J Crohns Colitis 2024;18(9):1440-9. DOI:10.1093/ecco-jcc/jjae059
11. Huguet JM, García-Lorenzo V, Martí L, et al. Subcutaneous Infliximab [CT-P13], a True Biologic 2.0. Real Clinical Practice Multicentre Study. Biomedicines 2022;10(9):2130. DOI:10.3390/biomedicines10092130
12. Colombel JF, Sandborn WJ, Schreiber S, et al. Subcutaneous Infliximab (CT-P13 SC) as Maintenance Therapy for Crohn's Disease and Ulcerative Colitis: 2-Year Results from Open-Label Extensions of Two Randomized Controlled Trials (LIBERTY). J Crohns Colitis 2025;19(6):jjaf060. DOI:10.1093/ecco-jcc/jjaf060
13. National Institute on Aging. Adverse Event and Serious Adverse Event Guidelines [Internet]. Bethesda, MD: National Institute on Aging; 2018 [cited 2025 August 23]. Available at: https://www.nia.nih.gov/sites/default/files/2018-09/nia-ae-and-sae-guidelines-2018.pdf
14. Iborra M, Caballol B, Garrido A, et al. Subcutaneous Infliximab Cutoff Points in Patients With Inflammatory Bowel Disease: Data From the ENEIDA Registry. J Crohns Colitis 2025;19(1):jjae127. DOI:10.1093/ecco-jcc/jjae127
15. Schreiber S, Colombel JF, Hanauer SB, et al. Comparing Outcomes With Subcutaneous Infliximab (CT-P13 SC) by Baseline Immunosuppressant Use: A Post Hoc Analysis of the LIBERTY-CD and LIBERTY-UC Studies. Inflamm Bowel Dis Published online April 30, 2025. DOI:10.1093/ibd/izaf038
16. Hanauer SB, Sands BE, Schreiber S, et al. Subcutaneous Infliximab (CT-P13 SC) as Maintenance Therapy for Inflammatory Bowel Disease: Two Randomized Phase 3 Trials (LIBERTY). Gastroenterology 2024;167(5):919-33. DOI:10.1053/j.gastro.2024.05.006
17. Sands BE, Hanauer SB, Colombel JF, et al. P957: Subcutaneous infliximab (CT-P13 SC) for ulcerative colitis: 2-year extension results of the LIBERTY-UC study. J Crohns Colitis 2024;18 (Supplement_1):i1737-38. DOI:10.1093/ecco-jcc/jjad212.1087
18. Colombel JF, Hanauer SB, Sandborn WJ, et al. P902: Subcutaneous infliximab (CT-P13 SC) as maintenance therapy for Crohn’s disease: 2 years results of the LIBERTY-CD study. J Crohns Colitis 2024;18(Suppl_1):i1653-4. DOI:10.1093/ecco-jcc/jjad212.1032
19. Roblin X, Nancey S, Papamichael K, Duru G, Flamand M, Kwiatek S, Cheifetz A, Fabien N, Barrau M, Paul S. Higher Serum Infliximab Concentrations Following Subcutaneous Dosing are Associated with Deep Remission in Patients with Inflammatory Bowel Disease. J Crohns Colitis 2024;18(5):679-85. DOI: 10.1093/ecco-jcc/jjad188.
20. Buisson A, Nachury M, Reymond M, et al. Effectiveness of Switching From Intravenous to Subcutaneous Infliximab in Patients With Inflammatory Bowel Diseases: the REMSWITCH Study. Clin Gastroenterol Hepatol 2023;21(9):2338-46.e3. DOI:10.1016/j.cgh.2022.08.011
21. Buisson A, Nachury M, Bazoge M, et al. Long-term effectiveness and acceptability of switching from intravenous to subcutaneous infliximab in patients with inflammatory bowel disease treated with intensified doses: The REMSWITCH-LT study. Aliment Pharmacol Ther 2024;59(4):526-34. DOI:10.1111/apt.17822
22. Smith PJ, Fumery M, Leong RW, Novak K, Dignass A. Real-world experience with subcutaneous infliximab: broadening treatment strategies for inflammatory bowel disease. Expert Rev Clin Immunol 2023;19(9):1143-56. DOI:10.1080/1744666X.2023.2231148
23. Dai C, Huang YH, Jiang M. Combination therapy in inflammatory bowel disease: Current evidence and perspectives. Int Immunopharmacol 2023;114:109545. DOI:10.1016/j.intimp.2022.109545
24. Huguet JM, Martí Romero L, Boscá-Watts MM, et al. Long-term use of subcutaneous infliximab biosimilar CT-P13 in patients with inflammatory bowel disease in clinical practice. Rev Esp Enferm Dig. Published online January 29, 2026. doi:10.17235/reed.2026.11727/2025




