El brote grave de colitis ulcerosa (BGCU) sigue siendo, hoy en día, una de las situaciones más difíciles que puede afrontar un gastroenterólogo en un hospital. El paciente llega con diarrea sanguinolenta, dolor, fiebre y afectación del estado general. El margen de maniobra es estrecho y las decisiones de las primeras 72 horas condicionan el pronóstico a corto y largo plazo.
Durante buena parte del siglo XX, el BGCU era prácticamente una sentencia de colectomía urgente, postoperatorio complejo y una causa no infrecuente de mortalidad. Antes de disponer de corticoides intravenosos (IV), se estima que más de la mitad de los pacientes con un brote grave fallecían1. La historia de cómo hemos pasado de esa realidad a la situación actual -con mortalidades cercanas al 1% y múltiples opciones de rescate- permite entender el manejo llevado a cabo en la actualidad, y también por qué seguimos discutiendo cuál es la mejor dosis, qué fármaco priorizar y cuándo es realmente el mejor momento para ir a quirófano.

Dr. Alfonso Elosua
Fuente: GETECCU / Harmon
Truelove, Witts y la primera piedra: definir la gravedad y demostrar que los corticoides salvan vidas
En los años 50, Truelove y Witts describieron con precisión clínica lo que entendemos hoy como BGCU: seis o más deposiciones con sangre al día acompañadas de fiebre, taquicardia, anemia y elevación de marcadores inflamatorios2. Y, lo más importante, demostraron que la administración de corticoides por vía sistémica reducía de forma significativa la mortalidad frente al tratamiento conservador.
Desde entonces, los corticoides IV se convirtieron en el pilar del manejo del BGCU. Sin embargo, pronto quedó claro que no eran la solución definitiva: alrededor de un tercio de los pacientes no respondía y terminaba en quirófano. La colectomía seguía siendo frecuente y muchas veces se realizaba tarde, en pacientes ya sépticos y desnutridos y con un alto riesgo quirúrgico.
El grupo de Oxford: la idea que cambió la historia fue “no esperar”
El siguiente gran salto no vino de un fármaco nuevo, sino de una estrategia diferente. En 1996, el grupo del hospital John Radcliffe de Oxford, con Simon Travis a la cabeza, se planteó una pregunta muy simple: ¿estamos operando demasiado tarde? Sus trabajos mostraron que era posible predecir, ya en el día 3 de tratamiento con corticoides IV, qué pacientes tenían una alta probabilidad de fracasar3.
De ahí nacieron los “criterios de Oxford”: si en el día 3 el paciente sigue con más de ocho deposiciones diarias, o con entre tres y ocho pero con una proteína C reactiva (PCR) superior a 45 mg/L, el riesgo de colectomía es muy elevado. En la práctica, esto cambió la actitud clínica: en lugar de “seguir esperando a ver si mejora”, se empezó a plantear la colectomía de forma precoz o, cuando estuvo disponible, la terapia de rescate.
El impacto fue enorme. Adelantar la decisión quirúrgica en los pacientes que no respondían redujo la mortalidad a cifras inferiores al 1-2% en muchas series contemporáneas. La lección sigue vigente: en el BGCU, el problema es llegar tarde a la decisión.
Manejo inicial actual: las primeras 72 horas siguen mandando
La forma en que manejamos hoy un brote grave se construye sobre esa evidencia. Cualquier paciente que cumple criterios de BGCU debe ser ingresado en un entorno hospitalario con experiencia en Enfermedad Inflamatoria Intestinal (EII)4.
Se solicitan coprocultivos y toxina de Clostridioides difficile para descartar infección, y se valora una rectosigmoidoscopia para confirmar la actividad inflamatoria y descartar diagnósticos alternativos, incluyendo la posible sobreinfección por citomegalovirus en pacientes de riesgo. Además, se plantea una prueba de imagen para descartar complicaciones como megacolon tóxico o perforación. Se inicia corticoide IV a dosis plenas (equivalente a 1 mg/kg de prednisona), junto con profilaxis antitrombótica sistemática, dado el alto riesgo de eventos tromboembólicos.
Durante las primeras 48-72 horas, el paciente se monitoriza estrechamente: número de deposiciones, presencia de sangre y criterios de dolor, temperatura, frecuencia cardiaca, PCR, albúmina y hemoglobina. Ese “día 3” sigue siendo el punto de inflexión. Si hay respuesta clara, se continúa con descenso progresivo de corticoides y se planifica el tratamiento de mantenimiento. Si no la hay, la pregunta pasa a ser “¿rescate médico o cirugía?”.
Ciclosporina: el primer rescate que demostró que la colectomía no era el único final posible
A mediados de los 90 apareció el primer fármaco capaz de cambiar el destino inmediato de muchos pacientes que no respondían a esteroides: la ciclosporina. En un ensayo pequeño pero muy influyente, Lichtiger y colegas mostraron que la ciclosporina IV conseguía respuesta clínica en nueve de once pacientes con BGCU refractario a corticoides, frente a ninguno del grupo placebo5. El estudio se interrumpió prematuramente por motivos éticos, dada la diferencia tan marcada.

Autoría: Crear con IA
Fuente: depositphotos.com
Durante años, la ciclosporina fue el estándar de rescate. Su rapidez de acción era indiscutible y evitaba colectomías inmediatas en una proporción importante de pacientes. Sin embargo, también quedaron claras sus limitaciones: requería monitorización estrecha de niveles, tenía potencial de toxicidad renal y neurológica y, sobre todo, su capacidad de mantener la remisión a largo plazo era modesta. Grandes series sitúan la tasa de respuesta inicial en torno al 70%, pero con un porcentaje relevante de colectomías o necesidad de cambio a otros tratamientos en el seguimiento a uno o dos años6.
Infliximab: un rescate igual de eficaz, más manejable y con mantenimiento integrado
La llegada de infliximab a la colitis ulcerosa moderada-grave abrió la puerta a su uso en el brote grave. Pronto se vio que también podía revertir cuadros refractarios a corticoides, con el añadido de que el mismo fármaco servía para inducir y mantener la remisión.
La pregunta obvia era si uno de los dos rescates era claramente superior. Los ensayos CySIF y CONSTRUCT, publicados en 2012 y 2016, compararon infliximab y ciclosporina cara a cara en BGCU refractario a esteroides. La conclusión fue consistente: no hubo diferencias significativas en eficacia, tasas de colectomía, calidad de vida ni seguridad a corto plazo7,8. A largo plazo los resultados con ciclosporina eran inferiores9, por lo que a día de hoy no se utiliza ciclosporina como mantenimiento, siendo habitualmente un puente hacia otros fármacos; clásicamente, la azatioprina y más recientemente hacia el vedolizumab o el ustekinumab6.
En la práctica, esto significa que ambas alternativas son opciones válidas de rescate. La elección depende del perfil del paciente (comorbilidades, riesgo renal, historia de anti-factor de necrosis tumoral [anti-TNF]), de la experiencia del centro y de la estrategia de mantenimiento6. Hoy infliximab es el rescate más utilizado en muchos hospitales españoles, mientras que la ciclosporina mantiene un papel relevante en centros con tradición en su uso o cuando infliximab no es la mejor opción10.
Más inflamación, menos fármaco: farmacocinética, intensificación y lo que nos dicen PREDICT-UC y TITRATE
Con infliximab ya integrado en la práctica, empezaron a aparecer datos que explicaban por qué algunos pacientes fallaban a pesar de recibir la pauta estándar. Estudios farmacocinéticos demostraron que, en el BGCU, los niveles de infliximab caen de forma acelerada: hay pérdidas fecales, la albúmina baja y la inflamación sistémica aumenta su aclaramiento11.
Esta observación llevó a plantearse la pauta acelerada. El estudio de Gibson, en 2015, comparó retrospectivamente la pauta convencional (0, 2 y 6 semanas) con un esquema intensificado de tres dosis en unos 24 días. La colectomía precoz se redujo del 40% al 6,7% con la pauta intensificada, aunque sin diferencias claras en colectomía a largo plazo, lo que sugiere que, en algunos casos, más que evitarla, la retrasaría12 (Figura 1).
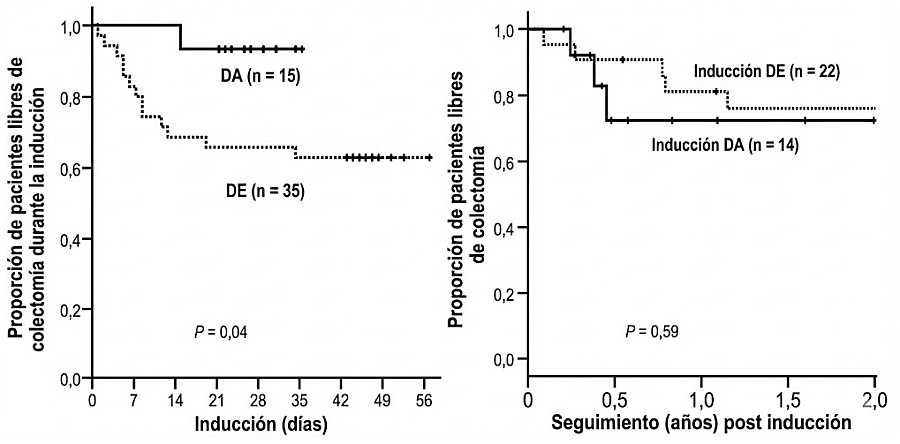
Figura 1. Tasas de supervivencia libre de colectomía en pacientes con BGCU: comparación entre pauta de inducción de infliximab acelerada (DA) y pauta estándar (DE).
La gráfica muestra la marcada reducción de la necesidad de cirugía en los primeros 30 días con el uso de dosis acelerada (DA), así como la posterior convergencia de las curvas con la dosis estándar (DE) en el seguimiento a largo plazo.
Adaptada de referencia 12
Hasta hace poco, la evidencia sobre intensificación procedía casi sólo de estudios observacionales. PREDICT-UC cambió esto al evaluar de forma aleatorizada una estrategia de infliximab intensificado upfront frente a la pauta estándar. El resultado fue una mejor respuesta clínica temprana (día 7), pero sin reducción de la colectomía ni mejora de la respuesta mantenida a los tres meses13. Ensayos como TITRATE, que intentó guiar la dosis por modelos farmacocinéticos, apuntan en la misma dirección: la intensificación tiene sentido, pero probablemente no para todos14. El mensaje práctico actual es que podría tener sentido intensificar de forma individualizada en pacientes con alta carga inflamatoria y alto riesgo de aclaramiento acelerado del fármaco, pero no como reflejo automático.
Cuando el primer rescate falla: estrategias secuenciales y tercera línea
Otra cuestión clave es qué hacer cuando el primer rescate fracasa. Tradicionalmente, se desaconsejaba administrar ciclosporina tras infliximab (o viceversa) por miedo a la inmunosupresión acumulada y al riesgo infeccioso. Sin embargo, las series modernas muestran que, en manos de equipos expertos, el rescate secuencial puede evitar la colectomía en aproximadamente la mitad de los pacientes6.
El estudio REASUC, publicado en 2024, aporta datos especialmente relevantes15. Incluye pacientes con BGCU refractario a esteroides que además habían fracasado a infliximab o ciclosporina. A estos enfermos se les ofreció una tercera línea de rescate (el fármaco alternativo, tofacitinib o ustekinumab). Más de la mitad evitó la colectomía durante el año de seguimiento, con una mortalidad baja, del 2,6%, pero no despreciable.
Esto no significa que la triple inmunosupresión deba generalizarse, pero sí que, en centros con experiencia, existe margen terapéutico más allá del primer rescate, especialmente en pacientes jóvenes, sin comorbilidades significativas y con alto impacto potencial de una colectomía urgente16.
Los inhibidores de JAK (iJAK): una nueva vía con potencial para cambiar el algoritmo
En los últimos años, los iJAK se han consolidado como una de las líneas de desarrollo más prometedoras en el brote grave. Su perfil farmacológico resulta especialmente adecuado para este contexto: administración oral, inicio de acción muy rápido, vida media corta y ausencia de inmunogenicidad. Las series recopiladas en revisiones recientes muestran que tofacitinib y upadacitinib permiten evitar la colectomía a en torno el 80% de los pacientes tratados en escenarios de rescate, incluso tras exposición previa a biológicos o fracaso de infliximab durante la hospitalización17.
Pese a ello, la evidencia disponible procede en su mayoría de cohortes retrospectivas y pequeños estudios prospectivos, de modo que la utilización de iJAK se concentra hoy en unidades de EII con experiencia, fundamentalmente como segunda o tercera línea en pacientes jóvenes, con baja comorbilidad y alto impacto esperado de una colectomía urgente. La cuestión ya no es tanto si son eficaces, sino cuál debe ser su lugar en el algoritmo: si han de reservarse para el fallo de infliximab o ciclosporina, si pueden competir con ellos como rescate de elección o incluso plantearse como alternativa inicial a los corticoides IV en perfiles muy seleccionados.
Ensayos en marcha como SMART (NCT05867329), que compara estrategias secuenciales con corticoides IV, upadacitinib y ciclosporina, o TOCASU (NCT05112263), que enfrenta directamente tofacitinib y ciclosporina en el brote corticorrefractario, serán determinantes para definir ese posicionamiento en los próximos años.

Autor/a: duiwoy
Fuente: depositphotos.com
¿Dónde estamos y hacia dónde vamos?
Setenta años después de Truelove y Witts, el BGCU ya no es sinónimo de mortalidad alta ni de colectomía inevitable. La combinación de criterios de predicción precoz (Oxford), corticoides IV bien utilizados, rescates efectivos (ciclosporina, infliximab), estrategias de intensificación en pacientes seleccionados, posibilidad de rescate secuencial y tercera línea, y aparición de fármacos orales de acción rápida como los iJAK han transformado el pronóstico inmediato del brote grave.
Persisten, no obstante, retos importantes: la incidencia del BGCU no se ha reducido, la tasa global de colectomía se mantiene en torno al 25-30% en muchas series y la variabilidad entre centros sigue siendo considerable. Además, seguimos sin biomarcadores robustos que indiquen de forma temprana quién responderá a corticoides, quién a infliximab, quién a ciclosporina o quién se beneficiará más de un iJAK.
Lo que empieza a vislumbrarse es que el BGCU deja de ser un “callejón sin salida" para convertirse en un escenario donde las decisiones basadas en la evidencia, la anticipación y las nuevas terapias ofrecen un margen de actuación real. Cada avance -desde los criterios de Oxford hasta los iJAK- ha ido recortando el peso de la colectomía urgente y ampliando las opciones de rescate. El futuro es esperanzador cuando equipos interdisciplinares saben convertir conocimiento y anticipación en decisiones oportunas.
Referencias
1. Caprilli R, Clemente V, Frieri G. Historical evolution of the management of severe ulcerative colitis. J Crohns Colitis. 2008;2(3):263-268. doi:10.1016/j.crohns.2008.03.008
2. Truelove SC, Witts LJ. Cortisone in ulcerative colitis; final report on a therapeutic trial. Br Med J. 1955;2(4947):1041-1048. doi:10.1136/bmj.2.4947.1041
3. Travis SP, Farrant JM, Ricketts C, Nolan DJ, Mortensen NM, Kettlewell MG, et al. Predicting outcome in severe ulcerative colitis. Gut. 1996;38(6):905-910. doi:10.1136/gut.38.6.905
4. Sicilia B, García-López S, González-Lama Y, Zabana Y, Hinojosa J, Gomollón F. Guía GETECCU 2020 para el tratamiento de la colitis ulcerosa. Elaborada con metodología GRADE. Gastroenterol Hepatol. 2020;43:1-57. doi:10.1016/j.gastrohep.2020.07.001
5. Lichtiger S, Present DH, Kornbluth A, Gelernt I, Bauer J, Galler G, et al. Cyclosporine in severe ulcerative colitis refractory to steroid therapy. N Engl J Med. 1994;330(26):1841-1845. doi:10.1056/NEJM199406303302601
6. Gisbert JP, García MJ, Chaparro M. Rescue Therapies for Steroid-refractory Acute Severe Ulcerative Colitis: A Review. J Crohns Colitis. 2023;17(6):972-994. doi:10.1093/ecco-jcc/jjad004
7. Laharie D, Bourreille A, Branche J, Allez M, Bouhnik Y, Filippi J, et al. Ciclosporin versus infliximab in patients with severe ulcerative colitis refractory to intravenous steroids: a parallel, open-label randomised controlled trial. The Lancet. 2012;380(9857):1909-1915. doi:10.1016/S0140-6736(12)61084-8
8. Williams JG, Alam MF, Alrubaiy L, Arnott I, Clement C, Cohen D, et al. Infliximab versus ciclosporin for steroid-resistant acute severe ulcerative colitis (CONSTRUCT): a mixed methods, open-label, pragmatic randomised trial. Lancet Gastroenterol Hepatol. 2016;1(1):15-24. doi:10.1016/S2468-1253(16)30003-6
9. Laharie D, Bourreille A, Branche J, Allez M, Bouhnik Y, Filippi J, et al. Long-term outcome of patients with steroid-refractory acute severe UC treated with ciclosporin or infliximab. Gut. 2018;67(2):237-243. doi:10.1136/gutjnl-2016-313060
10. Rodríguez-Lago I, Ferreiro-Iglesias R, Nos P, Gisbert JP. Manejo de la colitis ulcerosa aguda grave en España: Resultados de una encuesta sobre práctica clínica. Gastroenterol Hepatol. 2019;42(2):90-101. doi:10.1016/j.gastrohep.2018.09.002
11. Brandse JF, Van Den Brink GR, Wildenberg ME, Van der Kleij D, Rispens T, Jansen JM, et al. Loss of Infliximab Into Feces Is Associated With Lack of Response to Therapy in Patients With Severe Ulcerative Colitis. Gastroenterology. 2015;149(2):350-355.e2. doi:10.1053/j.gastro.2015.04.016
12. Gibson DJ, Heetun ZS, Redmond CE, Nanda KS, Keegan D, Byrne K, et al. An Accelerated Infliximab Induction Regimen Reduces the Need for Early Colectomy in Patients With Acute Severe Ulcerative Colitis. Clin Gastroenterol Hepatol. 2015;13(2):330-335.e1. doi:10.1016/j.cgh.2014.07.041
13. Choy MC, Li Wai Suen CFD, Con D, Boyd K, Pena R, Burrell K, et al. Intensified versus standard dose infliximab induction therapy for steroid-refractory acute severe ulcerative colitis (PREDICT-UC): an open-label, multicentre, randomised controlled trial. Lancet Gastroenterol Hepatol. 2024;9(11):981-996. doi:10.1016/S2468-1253(24)00200-0
14. Gecse K, Van Oostrom J, Rietdijk S, Frigstad SO, Doherty G, Irving P, et al. DOP056 TDM-Based Dose-Intensification of Infliximab is not Superior to Standard Dosing in Patients with Acute Severe Ulcerative Colitis: Results from the TITRATE Study. J Crohns Colitis. 2025;19(Supplement_1):i194-i195. doi:10.1093/ecco-jcc/jjae190.0095
15. García MJ, Riestra S, Amiot A, Julsgaard M, García de la Filia I, Calafat M, et al. Effectiveness and safety of a third-line rescue treatment for acute severe ulcerative colitis refractory to infliximab or ciclosporin (REASUC study). Aliment Pharmacol Ther. 2024;59(10):1248-1259. doi:10.1111/apt.17938
16. Raine T, Bonovas S, Burisch J, Kucharzik T, Adamina M, Annese V, et al. ECCO Guidelines on Therapeutics in Ulcerative Colitis: Medical Treatment. J Crohns Colitis. 2022;16(1):2-17. doi:10.1093/ecco-jcc/jjab178
17. Gisbert JP, Chaparro M. Janus kinase inhibitors in the management of acute severe ulcerative colitis: a comprehensive review. J Crohns Colitis. 2025;19(2):jjaf021. doi:10.1093/ecco-jcc/jjaf021




