La menopausia constituye una etapa de transición importante en la vida de la mujer y puede dar lugar a síntomas incapacitantes como sofocos, alteraciones del sueño, depresión de inicio reciente o alteraciones en el humor, atrofia vaginal y disfunción sexual1,2. La edad media de la menopausia en España se sitúa entre los 51 y 52 años2.
A pesar de la elevada prevalencia y del impacto que estos síntomas relacionados con la menopausia tienen sobre la calidad de vida de las mujeres, continúan siendo síntomas infradiagnosticados y, en muchas ocasiones, subestimados tanto por pacientes como por profesionales sanitarios. Esta falta de reconocimiento puede traducirse en un abordaje insuficiente, repercutiendo negativamente en el bienestar físico, emocional y social de las pacientes. Además, la deficiencia relativa de estrógenos propia de esta etapa se asocia a un mayor riesgo de enfermedad cardiovascular, osteoporosis y trastornos neurodegenerativos3. Por ello, es importante realizar una evaluación activa de estos síntomas y condiciones durante el período de transición y primeros años de la menopausia.

Dra. Margalida Calafat
Fuente: Dra. Calafat
Por otro lado, las hormonas sexuales femeninas pueden impactar en el funcionamiento del sistema inmune y pueden jugar un papel en la etiología y la fisiopatología de enfermedades crónicas autoinmunes, exponiendo a las mujeres a un mayor riesgo de presentarlas4,5. Concretamente, los receptores de estrógenos periféricos localizados en el colon o intestino delgado contribuyen al correcto funcionamiento de la permeabilidad intestinal6, por lo que la caída de los estrógenos que caracteriza a la menopausia podría modificar los síntomas y la homeostasis intestinales.
Las Enfermedades Inflamatorias Intestinales (EII) son patologías crónicas inmunomediadas de etiología multifactorial que pueden verse influidas por los cambios hormonales que se producen en las mujeres (tanto en la edad fértil como en el climaterio o la menopausia establecida)4,5.
En la menopausia, que se caracteriza por el declive hormonal -especialmente de los estrógenos-, se han propuesto mecanismos por los que el cambio hormonal podría influir en la EII. Aunque en términos clínicos, la evidencia es heterogénea.
Edad de la menopausia y EII
Estudios iniciales sugerían que las mujeres con enfermedad de Crohn (EC) podían presentar una menopausia más temprana, si bien el mecanismo subyacente no está claramente establecido7. Un estudio retrospectivo con 171 mujeres observó que la edad media de la menopausia era significativamente menor en pacientes con EII (50 años frente a 51,5 años en mujeres sin EII)8. Además, el papel que pueden jugar los estrógenos en las diferentes entidades autoinmunes está por dilucidar, aunque en un estudio retrospectivo se objetivó que, a mayor edad de aparición de la menopausia, más tardío aparecía el diagnóstico de la EII9, proponiendo un supuesto papel protector.

Autor/a: IgorVetushko
Fuente: depositphotos.com
En términos generales, la menopausia precoz se asocia con una menor densidad ósea y un mayor riesgo de fracturas y de enfermedad cardiovascular, como demuestran estudios a gran escala del Women’s Health Initiative10-12. En este sentido, cabe destacar que las pacientes con EII ya presentan un riesgo aumentado para estas comorbilidades.
Interacción entre actividad de la EII y menopausia
En mujeres con EII, se ha observado que pueden presentar un incremento en los síntomas intestinales, presentando peores puntuaciones de calidad de vida relacionada con la menopausia, especialmente en los ámbitos psicosocial, físico y sexual8.
En una encuesta en la que contestaron más de 1.200 pacientes con EII, y en la que se evaluaban los síntomas de la EII (sCDAI EC [the short Crohn’s Diseases Activity Index, o índice corto de actividad de la EC]; SCCAI CU [Simple Clinical Colitis Activity Index, o índice simple de actividad clínica de la colitis ulcerosa (CU)]) en función de las diferentes etapas del ciclo menstrual, se evidenció un empeoramiento de los síntomas intestinales en aquellas pacientes postmenopáusicas13 (Tabla 1).
Por otro lado, se ha descrito que el tratamiento hormonal substitutivo puede tener una evolución más favorable de la EII con un menor riesgo de brote en los primeros dos años de tratamiento hormonal14,15. No obstante, existe algún estudio contradictorio que describe que la terapia hormonal substitutiva se relacionó con un mayor riesgo de desarrollar una CU incidente, pero no de EC16.
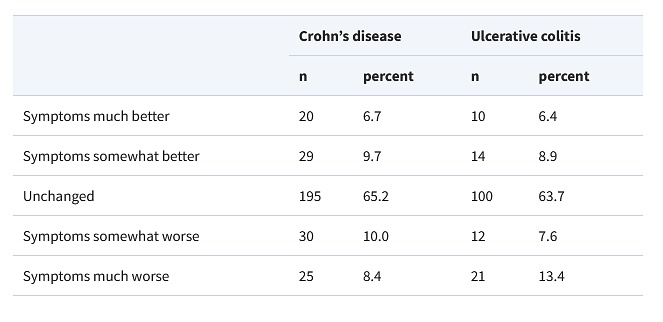
Tabla 1. Curso de los síntomas de la EII después de la menopausia en mujeres con EC/CU
Extraída de referencia 13
Enfoque terapéutico
A pesar de la escasez de evidencia específica sobre menopausia y EII, parece prudente incorporar una perspectiva “ciclo-menopausia” en la atención de la mujer con EII, más allá de la relevancia de la interrupción de la capacidad reproductiva propia de esta etapa. Reconocer las distintas etapas del ciclo y la transición menopáusica permite diferenciar las fluctuaciones hormonales y síntomas funcionales o extraintestinales de la actividad inflamatoria, y así optimizar el abordaje sintomático y evitar escaladas terapéuticas innecesarias.
Asimismo, la identificación de una menopausia precoz o insuficiencia ovárica debe motivar la derivación a ginecología para confirmación diagnóstica y manejo específico. Cuando esté indicada, la terapia hormonal de la menopausia podría asociarse a un impacto favorable o, al menos, no perjudicial sobre el curso de la EII, si bien se requieren estudios de mayor calidad.
De forma paralela, la transición menopáusica obliga a una evaluación proactiva de comorbilidades y complicaciones relevantes en EII: salud ósea (prevención, cribado y tratamiento de osteoporosis), riesgo cardiovascular, riesgo trombótico y salud sexual/urogenital. Todo ello requiere un enfoque multidisciplinar y coordinado con ginecología, atención primaria y enfermería especializada, con individualización del plan según edad, factores de riesgo, exposición a corticoides, estado nutricional y control inflamatorio.
Finalmente, el objetivo central debe seguir siendo mantener una remisión sostenida de la EII mediante la optimización del tratamiento y el seguimiento estrecho, ya que el control de la inflamación es clave para reducir complicaciones, minimizar el impacto de la menopausia sobre la calidad de vida y mejorar los resultados a largo plazo en estas pacientes.
Bibliografía
1. Wang G, Ching C, Hanna Y, Tandon P, Huang V. Health Maintenance and Unique Health Needs of the Perimenopausal and Postmenopausal Woman with Inflammatory Bowel Disease. Dig Dis Sci. 2025. Epub ahead of print.
2. Mendoza N, Juliá MD, Galliano D, Coronado P, Díaz B, Fontes J, et al. Spanish consensus on premature menopause. Maturitas. 2015;80(2):220-5.
3. Takahashi TA, Johnson KM. Menopause. Med Clin North Am. 2015;99(3):521-34.
4. Bharadwaj S, Kulkarni G, Shen B. Menstrual cycle, sex hormones in female inflammatory bowel disease patients with and without surgery. J Dig Dis. 2015;16:245–255.
5. Gargallo-Puyuelo C, Ricart E, Iglesias E, De Francisco R, Gisbert JP, Taxonera C, et al. Sex-Related Differences in the Phenotype and Course of Inflammatory Bowel Disease: SEXEII Study of ENEIDA. Clin Gastroenterol Hepatol. 2024;22(11):2280-2290.
6. Garcia-Villatoro EL, Allred CD. Estrogen receptor actions in colitis. Essays in Biochemistry. 2021;65:1003–1013.
7. Lichtarowicz A, Norman C, Calcraft B, Morris JS, Rhodes J, Mayberry J. A study of the menopause, smoking, and contraception in women with crohn’s disease. Q J Med. 1989;72:623–631.
8. Moktan VP, Daoud ND, Tremaine WJ, Loftus Jr EV, Kane SV, Hochwald AP, et al. A cohort study of the age at menopause in female patients with and without inflammatory bowel disease. Crohns & Colitis 360. 2022;4:027.
9. Donaldson EK, Huang V, Ross S, Sydora BC. Experience of menopause in women with inflammatory bowel disease: pilot study. Climacteric. 2017;20:545–551.
10. Sullivan SD, Lehman A, Nathan NK, Thomson CA, Howard BV. Age of menopause and fracture risk in postmenopausal women randomized to calcium + Vitamin D, hormone therapy, or the combination: results from the Women’s Health Initiative Clinical Trials. Menopause. 2017;24:371–378.
11. Appiah D, Schreiner PJ, Demerath EW, Loehr LR, Chang PP, Folsom AR. Association of age at menopause with incident heart failure: a prospective cohort study and meta-analysis. J Am Heart Assoc. 2016;5:e003769.
12. Zhu D, Chung HF, Dobson AJ, Pandeya N, Giles GG, Bruinsma F, et al. Age at natural menopause and risk of incident cardiovascular disease: a pooled analysis of individual patient data. Lancet Public Health. 2019;4:e553–e564.
13. Rolston VS, Boroujerdi L, Long MD, McGovern DPB, Chen W, Martin CF, et al. The Influence of Hormonal Fluctuation on Inflammatory Bowel Disease Symptom Severity-A Cross-Sectional Cohort Study. Inflamm Bowel Dis. 2018;24(2):387-393.
14. Kane SV, Reddy D. Hormonal replacement therapy after menopause is protective of disease activity in women with inflammatory bowel disease. Am J Gastroenterol. 2008;103:1193–1196.
15. Rossouw JE, Anderson GL, Prentice RL, LaCroix AZ, Kooperberg C, Stefanick ML, et al. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women’s Health Initiative randomized controlled trial. JAMA. 2002;288(3):321–333.
16. Khalili H, Higuchi LM, Ananthakrishnan AN, Manson JE, Feskanich D, Richter JM, et al. Hormone therapy increases risk of ulcerative colitis but not Crohn's disease. Gastroenterology. 2012;143(5):1199-1206.




