Redacción Farmacosalud.com
La invasión y la metástasis son características que determinan que un cáncer que crece localmente se transforme en un proceso sistémico que pueda poner en peligro la vida del paciente. La metástasis en cerebro es frecuente en el cáncer de mama y una de las causas más comunes de las muertes por cáncer. Para llegar hasta el cerebro, las células del cáncer de mama deben migrar desde el tumor donde se originaron, entrar en el torrente sanguíneo y cruzar otra barrera que protege de forma especial el cerebro, por lo que la mayoría de ellas muere antes de implantarse en el órgano cerebral.
Todos y cada uno de estos pasos implican alteraciones mecánicas en las células tumorales. Tienen que modificar su forma y estrujarse para avanzar por los reducidos espacios disponibles, como hace un pulpo para esconderse en lugares inverosímiles. También tienen que liberar unas proteínas que, a modo de taladro químico, les permiten deshacer las barreras que se presentan a lo largo de su recorrido. Y finalmente, en el caso de las células del cáncer de mama que metastatizan en cerebro, necesitan unas proteínas, las serpinas, que anulan las defensas naturales del órgano cerebral, permitiendo el crecimiento del tumor en su nueva localización.

Micrografías de células en el proceso de adaptación de su forma para atravesar microtúneles de un diámetro 10 veces menor que el tamaño celular
Fuente: UPF
Un nivel alto del canal Piezo2 favorece la secreción de serpinas
Investigadores del Laboratorio de Fisiología Molecular del Departamento de Ciencias Experimentales y de la Salud de la Universidad Pompeu Fabra (UPF, en Barcelona), liderado por Miguel Ángel Valverde, han identificado que un nivel bajo del canal Piezo2 dificulta la secreción de serpinas, la invasión y la proliferacion; mientras que un nivel alto las favorece. La investigación se publica en la revista ‘Proceedings of the National Academy of Sciences’ y cuenta con la participación de investigadores del Instituto de Bioingeniería de Cataluña (IBEC) y de las Universidades de Grenoble (Francia) y Johns Hopkins (USA)
“Nuestro objetivo inicial era averiguar de qué depende que las células del cáncer de mama que producen metástasis en el cerebro liberen las serpinas, para que estas anulen las defensas del cerebro”, explica Carlos Pardo-Pastor, investigador en formación del Laboratorio de Fisiología Molecular de la UPF y primer firmante del artículo. “Durante el recorrido de una célula metastásica, ésta tiene que adaptarse a numerosos cambios en las propiedades físicas y mecánicas de su entorno. Por tanto, postulamos que los canales iónicos que detectan cambios mecánicos y osmóticos en las células pueden ser relevantes para la metástasis”, añade Miguel Ángel Valverde.
El trabajo, realizado con cultivos celulares de cáncer de mama, analizó la presencia de numerosos canales iónicos que pudieran servir para explorar el entorno físico de las células y descubrió que las células de cáncer de mama que específicamente metastatizan en cerebro presentan unos niveles más elevados del canal Piezo2 que las células que no presentan predilección por este lugar de metástasis.
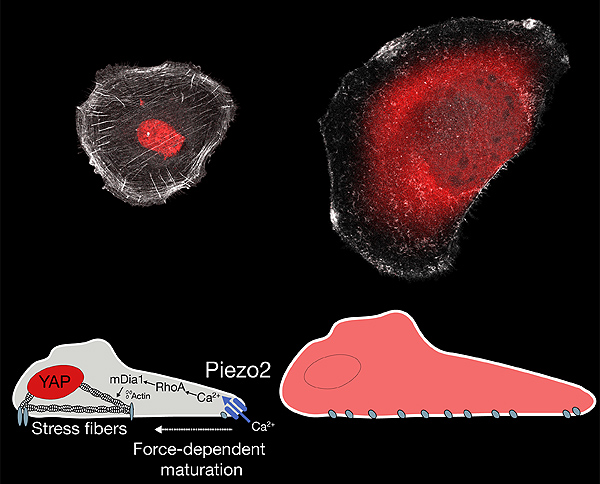
Imágenes microscópicas de una célula con niveles altos del canal Piezo2 (izquierda) o niveles bajos (derecha). La presencia del canal Piezo 2 es necesaria para que se organice el esqueleto celular (líneas blancas que cruzan la célula) y que una proteína (YAP en rojo) que controla muchas funciones celulares relacionadas con su capacidad tumoral se localice en el núcleo, lugar donde ejerce su función. Cuando el canal Piezo2 no está presente desaparece el esqueleto celular y la proteína YAP no se encuentra en el núcleo
Fuente: UPF
Las invadosomas, estructuras necesarias para permitir el paso de las células
Los canales iónicos son puertas selectivas a través de las cuales los iones entran y salen de la célula. En el caso de los canales Piezo, su apertura permite el flujo de calcio cuando la célula detecta cambios en la rigidez del entorno o cuando esta atraviesa espacios excesivamente estrechos (conocido como confinamiento celular). Según detalla el estudio, esta señal de calcio, a su vez, desencadena una amplia gama de respuestas que van desde la organización de la estructura esquelética celular a la activación de factores que controlan la expresión de genes necesarios para mantener la proliferación celular, la secreción de serpinas y la generación de unas estructuras conocidas como invadosomas, necesarias para perforar la matriz extracelular y permitir el paso de las células.
El descubrimiento podría convertir estos canales en el objetivo de nuevos fármacos que disminuyan el riesgo de metástasis. La investigación ha sido financiada, entre otras fuentes, por el Ministerio de Economía y Competitividad, Fondos FEDER y el Programa María de Maeztu para las unidades de excelencia en investigación y desarrollo.
Artículo de referencia:
Carlos Pardo-Pastor, Fanny Rubio-Moscardo, Marina Vogel-González, Selma A. Serra, Alexandros Afthinos, Sanela Mrkonjic, Olivier Destaing, Juan F. Abenza, José M. Fernández-Fernández, Xavier Trepat, Corinne Albiges-Rizo, Konstantinos Konstantopoulos, and Miguel A. Valverdea. Piezo2 channel regulates RhoA and actin cytoskeleton to promote cell mechanobiological responses. Proceedings of the National Academy of Sciences U.S.A. Febrero 2018




