Redacción Farmacosalud.com
Sanofi y Regeneron Pharmaceuticals, Inc. han anunciado de forma detallada los resultados positivos obtenidos del ODYSSEY ESCAPE, un ensayo de fase III que ha evaluado la inyección subcutánea de Praluent® (alirocumab) en pacientes con hipercolesterolemia familiar heterocigótica (HFHe) que por causa hereditaria tienen los niveles de colesterol muy altos y necesitan someterse con regularidad a un tratamiento semanal o quincenal de aféresis del cLDL. El ensayo ha demostrado que añadir Praluent al tratamiento existente reduce el colesterol LDL en aproximadamente un 50% desde el inicio del estudio (en comparación con el aumento del 2% experimentado con placebo). El medicamento reduce de forma significativa las necesidades del tratamiento de aféresis; concretamente, en un 75% en comparación con placebo (p <0,0001), que era el objetivo principal del estudio. Los resultados se han presentado en el marco del Congreso 2016 de la SEC (Sociedad Europea de Cardiología), que se celebra en Roma (Italia).
La aféresis es un procedimiento similar a la diálisis renal, mediante el cual el colesterol malo (colesterol de las LDL) se extrae de la sangre. Este procedimiento se reserva para pacientes de alto riesgo cardiovascular con niveles de colesterol muy altos para los que resulta imposible alcanzar los objetivos de reducción del colesterol mediante cualquier otra terapia con fármacos. Los pacientes que entraron el estudio ODYSSEY ESCAPE tenían un nivel medio de colesterol LDL muy alto, de 181 mg/dL (miligramos/decilitro), casi dos tercios (el 63%) de los pacientes tratados con Praluent no volvieron a necesitar la terapia de aféresis tras seis semanas de tratamiento con Praluent. En ese mismo momento, la media del nivel de colesterol LDL entre los miembros del grupo tratados con Praluent era de 90 mg/dL, en comparación con los 185 mg/dL del grupo de placebo. Las directrices europeas recomiendan un nivel deseado de colesterol LDL sea de 70-115 mg/dL, en función del riesgo cardiovascular.

Autor/a: Sabine Sauermaul
Fuente: www.publicdomainpictures.net
“Posibilidad de reducir la dependencia de los costosos tratamientos de aféresis”
“Los resultados de ODYSSEY ESCAPE muestran la importancia de Praluent en el control integral de los pacientes con HFHe que se someten con regularidad a terapia de aféresis, y ofrecen la posibilidad de reducir la dependencia de los costosos tratamientos de aféresis”, afirma Patrick M. Moriarty, director médico y catedrático del Departamento de Medicina Interna y director del Centro de Aterosclerosis y de Aféresis de Lipoproteínas del Hospital Clínico Universitario de la Universidad de Kansas, en Estados Unidos. “Se trata de un progreso notable en el proceso de la continua investigación sobre este fármaco en pacientes con HFHe, ya que constituye el primer ensayo clínico que demuestra que Praluent reduce la frecuencia de la terapia de aféresis”.
La terapia de aféresis supone un tratamiento invasivo, caro y que consume gran cantidad de tiempo, dirigido a algunos de los pacientes más difíciles de tratar. El coste del tratamiento puede ascender a los 100.000 $ por paciente y año en EE.UU. y a los 60.000 € en Alemania, donde hay 200 centros y la aféresis de LDL se usa con mayor frecuencia. Por el contrario, en EE.UU. hay solamente unos 60 centros de aféresis y gran cantidad de pacientes se ven obligados a recorrer largas distancias para someterse al tratamiento. Otros resultados clave de ODYSSEY ESCAPE, que se han publicado paralelamente en el European Heart Journal [Revista Europea del Corazón], comprenden los siguientes puntos:
• El 93% de los pacientes tratados con Praluent tuvieron una reducción del 50% como mínimo, en el procedimiento de la aféresis (p> 0,0001).
• Durante el ensayo, los pacientes tratados con Praluent experimentaron reducciones significativas de su colesterol LDL, empezando en la semana 6 (un 55% de reducción en comparación con placebo) y acabando en el momento de finalización del ensayo, en la semana 18 (un 46% de reducción en comparación con placebo) (p <0,0001).
• Una proporción similar de pacientes padeció algún acontecimiento adverso (AA) tanto en el grupo tratado con Praluent como en el grupo de placebo (el 76% en ambos grupos). Los AA más comunes (presentados en al menos el 5% del grupo tratado con Praluent) fueron: fatiga (15% con Praluent; 10% con placebo), nasofaringitis (10% con Praluent; 10% con placebo), diarrea (10% con Praluent; 0% con placebo), mialgia (10% con Praluent; 5% con placebo), infección de las vías respiratorias altas (7% con Praluent; 19% con placebo), cefalea (7% con Praluent; 5% con placebo), artralgia (7% con Praluent; 10% con placebo) y dolor de espalda (5% con Praluent; 10% con placebo).
En el ensayo clínico ODYSSEY ESCAPE en fase III controlado con placebo han participado 62 pacientes de 14 centros de tratamiento de aféresis en EE.UU. y Alemania. Al inicio del estudio, estos pacientes recibían terapia de aféresis con regularidad a intervalos fijos semanales o quincenales antes de la aleatorización. La media de colesterol de las LDL al inicio del estudio fue de181 mg/dL. El 86% de los pacientes del grupo de placebo y el 90% de los pacientes del grupo tratado con Praluent presentaban antecedentes previos de cardiopatía coronaria. Los pacientes fueron aleatorizados para recibir, o bien Praluent de 150 mg (n = 41) subcutáneo cada 2 semanas, o bien placebo (n = 21), añadido a su tratamiento previo. El periodo de tratamiento doble ciego comprendió dos fases: durante las primeras 6 semanas, los pacientes mantuvieron el calendario de aféresis establecido al inicio del estudio; durante las siguientes 12 semanas, la frecuencia de la aféresis se ajustó basándose en la respuesta del colesterol LDL del paciente al tratamiento. ODYSSEY ESCAPE forma parte del programa ODYSSEY en fase III global, que incluye a más de 25 000 pacientes.
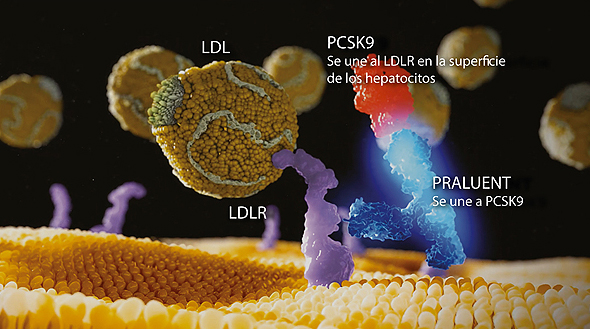
Infografía sobre colesterol LDL y PCSK9
Fuente: Sanofi (Archivo)
Inhibición de la unión de la PCSK9 a los receptores del colesterol LDL
Praluent inhibe la unión de la PCSK9 (proproteína convertasa subtilisina/kexina tipo 9) a los receptores del colesterol LDL y de este modo aumenta el número de receptores de LDL disponibles en la superficie de las células hepáticas, lo que da como resultado un nivel más bajo de colesterol LDL en sangre. Praluent es el único inhibidor de la PCSK9 que actualmente se encuentra disponible en dos dosis (75 mg y 150 mg) con dos niveles de eficacia, lo que permite al profesional sanitario elegir la dosis en función de las necesidades de reducción del colesterol LDL de cada paciente.
El uso de Praluent está autorizado en aproximadamente 40 países de todo el mundo: EE.UU, Japón, Canadá, Suiza, México, Brasil, entre otros, y en la Unión Europea (UE). En la UE, Praluent ha sido autorizado para el tratamiento de adultos con hipercolesterolemia primaria (HFHe y no familiar) o dislipidemia mixta como tratamiento complementario a la dieta: a) en combinación con estatinas, o estatinas con otros tratamientos hipolipidemiantes en pacientes que no logren alcanzar el nivel deseado de colesterol de las LDL con la dosis máxima tolerada de estatinas, o b) solo o en combinación con otros tratamientos hipolipidemiantes para pacientes que no toleren las estatinas o para los que un tipo de estatinas esté contraindicado.
El efecto de Praluent sobre la morbimortalidad cardiovascular todavía no se ha determinado. El estudio ODYSSEY OUTCOMES actualmente en marcha evalúa de manera prospectiva el efecto de Praluent en la aparición de acontecimientos cardiovasculares en aproximadamente 18.000 pacientes que sufrieron un síndrome coronario agudo. Este medicamento está sujeto a controles adicionales, lo que permitirá una detección rápida de la nueva información de seguridad. Se solicita a los profesionales sanitarios que notifiquen cualquier sospecha de reacción adversa.




