Redacción Farmacosalud.com
El CAR-T ARI0002h, desarrollado en el Hospital Clínic Barcelona-IDIBAPS, ha recibido el visto bueno del Comité de Evaluación de Medicamentos de Uso Humano de la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) para su aprobación como medicamento de terapia avanzada de fabricación no industrial en pacientes con mieloma múltiple (MM) en recaída.
El visto bueno del Comité de la AEMPS es el paso previo a la notificación de la aprobación de la exención hospitalaria que recibirá el Hospital Clínic Barcelona en los próximos días. El proceso de luz verde desde este centro hospitalario lo ha coordinado el equipo del Servicio de Farmacología Clínica, liderado por el Dr. Gonzalo Calvo. Por otro lado, la Clínica de la Universidad de Navarra será autorizada como segundo centro productor, ya que también ha producido la terapia CAR-T para los estudios clínicos.

Procedimiento vinculado a la terapia CAR-T
Autor/a de la imagen: @franciscoavia
Fuente: Hospital Clínic Barcelona
El primer CAR-T desarrollado íntegramente en Europa
El mieloma múltiple es un tipo de cáncer que afecta a las células plasmáticas de la médula ósea. Representa un 10% de los tumores malignos sanguíneos y, aunque existen diversos tratamientos disponibles, muchos enfermos desarrollan resistencia a ellos, lo que lleva a recaídas y una necesidad urgente de disponer de nuevos tratamientos. Aquí es donde las terapias CAR-T pueden tener un papel fundamental.
ARI0002h ha sido desarrollado íntegramente en el IDIBAPS por el grupo de investigación del Dr. Álvaro Urbano-Ispizua, coordinador del Programa CAR-T del Clínic-IDIBAPS y jefe del grupo Trasplante de progenitores hemopoyéticos del IDIBAPS. Es el primer CART europeo que demuestra una eficacia clínica en pacientes con MM. En concreto, es un fármaco que se dirige contra el antígeno BCMA, que se encuentra en la superficie de las células tumorales del mieloma. Dos estudios previos liderados por el Clínic-IDIBAPS y publicados en las revistas ‘Lancet Oncology’ y ‘Clinical Cancer Research’ han avalado la eficacia de ARI0002h en sujetos con dicha patología que han recaído tras, al menos, a dos líneas de tratamiento y están expuestos ya a los principales medicamentos usados en esta enfermedad.

Autor/a de la imagen: @franciscoavia
Fuente: Hospital Clínic Barcelona
El 95% de los enfermos mostraban respuesta al tratamiento
En los dos ensayos se validó la eficacia del tratamiento en un total de 60 pacientes; los resultados evidenciaron que el 95% de los enfermos mostraban respuesta al tratamiento con un perfil favorable de toxicidad.
El Dr. Carlos Fernández de Larrea, hematólogo del Clínic y jefe del grupo sobre mieloma, amiloidosis, macroglobulinemia y otras gammapatías del IDIBAPS, ha liderado el desarrollo clínico del CART ARI0002h, en el que han participado siete hospitales españoles: Hospital Clínic de Barcelona, Clínica Universidad de Navarra, Hospital Universitario de Salamanca, Hospital Virgen de la Arrixaca de Murcia, Hospital 12 de Octubre de Madrid, el Hospital Virgen del Rocío en Sevilla y el Hospital Clínico Universitario de Santiago (Santiago de Compostela, en A Coruña).
La preparación de los CARTs para su administración a los pacientes se ha realizado en el centro barcelonés, por el parte del equipo del servicio de Inmunología dirigido por el Dr. Manel Juan, jefe del Servicio de Inmunología del Clínic y del grupo Inmunogenética e inmunoterapia en la respuesta autoinflamatoria e inmunitaria del IDIBAPS, y en la Clínica Universidad de Navarra.
La eficacia del tratamiento se evalúa no sólo por la respuesta inicial del paciente, sino también por la durabilidad de esa reacción. Así, los investigadores también describieron la forma óptima de administrar la terapia y han identificado biomarcadores de respuesta que podrían mejorar la selección de enfermos y la personalización de los tratamientos. La primera dosis se aplica de forma fraccionada, en tres alícuotas, y, pasados 100 días desde la primera infusión, se administra una dosis de recuerdo que proporciona una respuesta sostenida con una baja toxicidad. Esto permite reducir la gravedad de los efectos adversos sin reducir la eficacia de la terapia.
Optimizar resultados, ajustar la estrategia terapéutica…
Por otro lado, se han analizado distintos factores y biomarcadores que permiten predecir la respuesta y la duración de ésta después del abordaje con ARI0002h. “Conocer qué pacientes responderán favorablemente a la terapia nos permitirá optimizar los resultados, ajustar la estrategia terapéutica y minimizar los efectos secundarios”, apunta el Dr. Fernández de Larrea.
La terapia CAR-T (llamada así por sus siglas en inglés Chimeric Antigen Receptor T-Cell o receptor de antígeno quimérico de células T) es un tratamiento que implica la modificación genética de las células T del paciente para que puedan reconocer y atacar células cancerosas. En el caso de ARI0002h, se ha diseñado específicamente para atacar las células del mieloma múltiple, un tipo de cáncer que afecta a las células plasmáticas en la médula ósea.
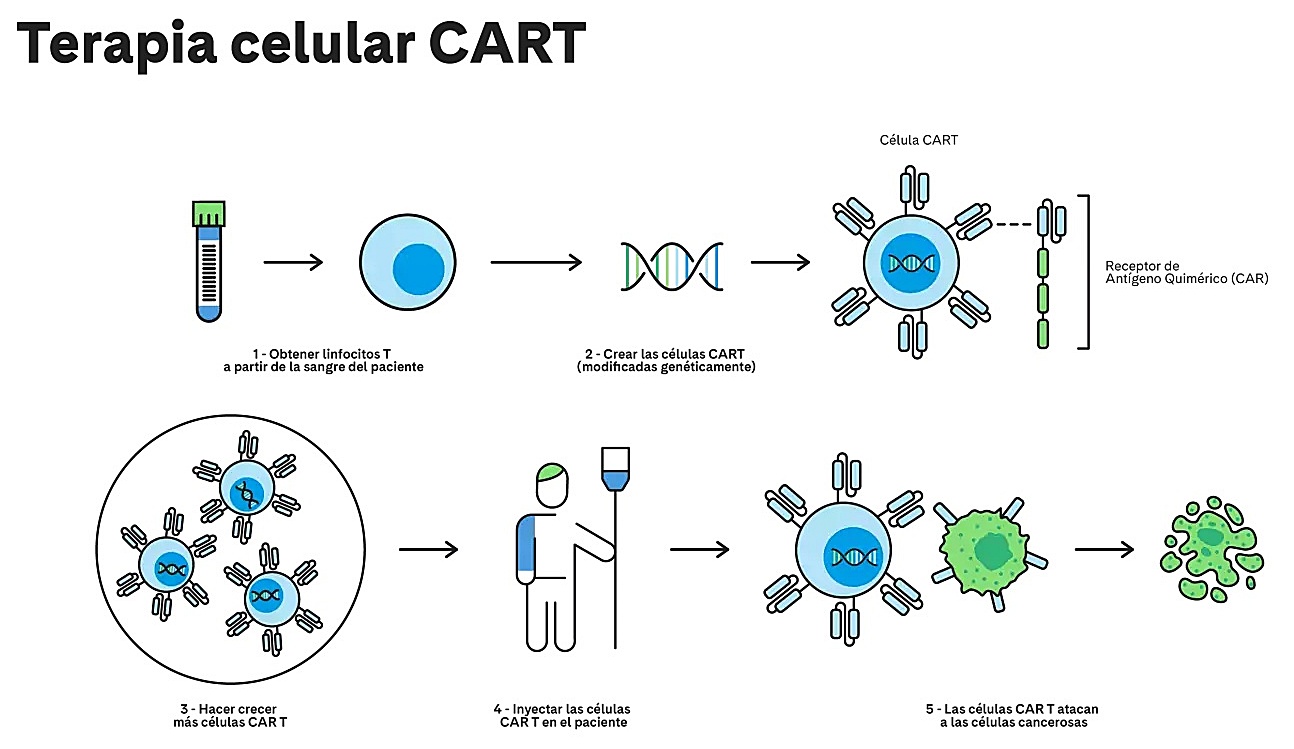
Proceso para la elaboración y administración de la terapia con células CAR-T
Fuente: Hospital Clínic Barcelona




