Redacción Farmacosalud.com
Janssen-Cilag International NV (Janssen) ha presentado los datos de un estudio fase 3 que demuestra una mejora significativa de la supervivencia libre de progresión (SLP) al administrar una terapia combinada basada en VELCADE® (bortezomib), y en comparación con el tratamiento de referencia en pacientes de nuevo diagnóstico de linfoma de células del manto. Los resultados indican que, en comparación con la combinación R-CHOP, el régimen basado en VELCADE (VR-CAP) aumenta la supervivencia libre de progresión (SLP, o el tiempo que viven los pacientes sin progresión de su enfermedad) en un 59% entre los pacientes con linfoma de células del manto (LCM) no tratados previamente (24,7 frente a 14,4 meses; RRI 0,63; p<0,001), ha informado la compañía Janssen mediante un comunicado.
“El linfoma de células del manto es un cáncer sanguíneo agresivo y difícil de tratar, y existen opciones muy limitadas como tratamiento de primera línea en los pacientes con diagnóstico reciente,” explica el Profesor Cavalli, investigador principal del estudio. “Este estudio demuestra claramente una serie de posibles beneficios asociados al uso de un tratamiento de primera línea basado en bortezomib en pacientes con linfoma de células del manto. Además de las mejoras significativas en la SLP, nuestro análisis ha demostrado también que el tratamiento basado en bortezomib puede prolongar el tiempo que un paciente permanece sin tratamiento y tener un efecto importante en la calidad de vida.”
487 pacientes en estudio
El estudio LYM-3002 es un estudio internacional de fase 3, aleatorizado, abierto, controlado con medicación activa, multicéntrico y prospectivo, realizado en 487 pacientes de nuevo diagnóstico reciente de LCM que no eran candidatos para un trasplante de médula ósea. Su objetivo es comparar la eficacia y la seguridad de la combinación de VR-CAP (VELCADE IV en combinación con rituximab, ciclofosfamida, doxorubicina y prednisona) con un tratamiento de referencia actual de primera línea para el LCM, R-CHOP (rituximab, ciclofosfamida, doxorubicina, vincristina, y prednisona). El criterio de valoración principal fue la supervivencia libre de progresión.
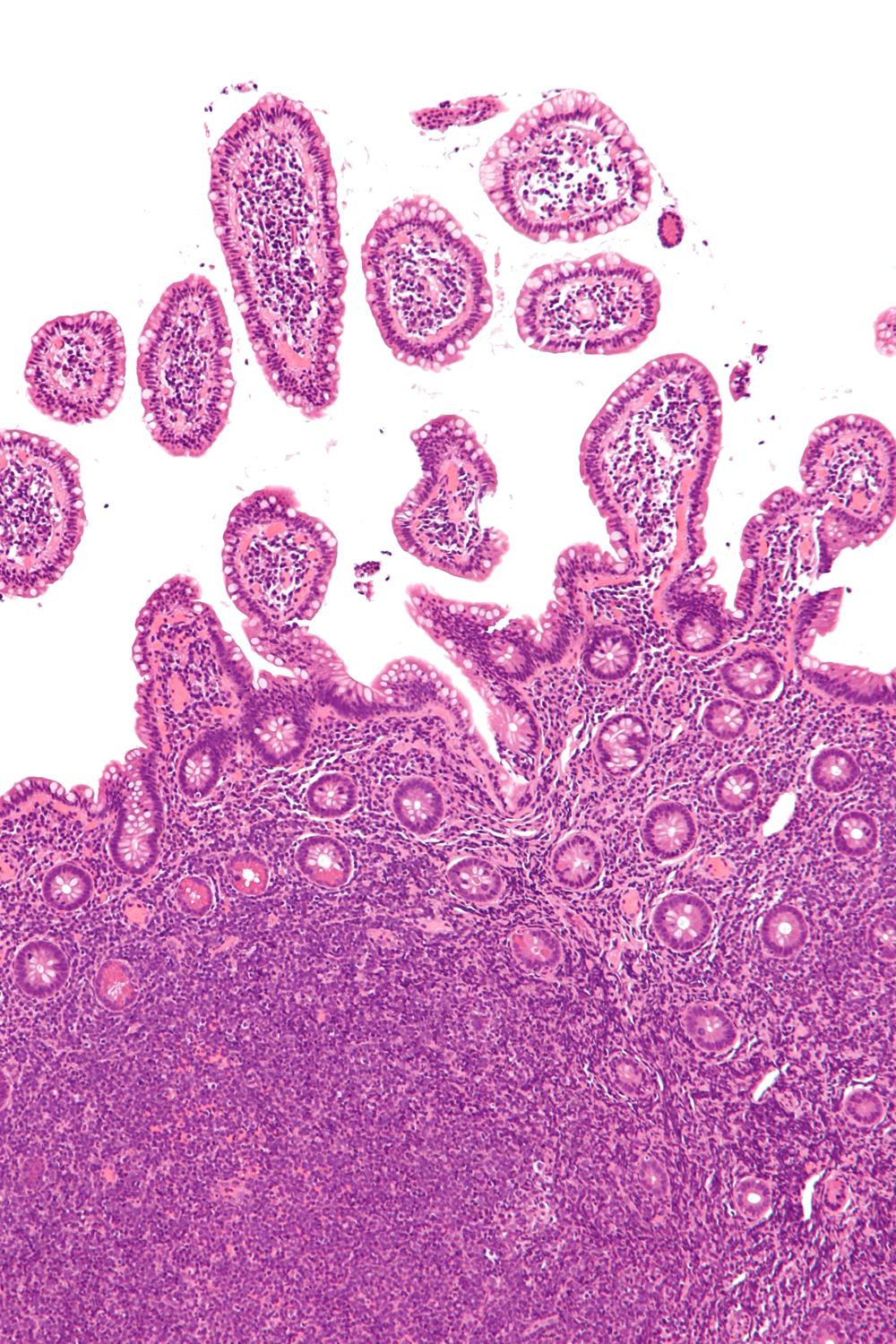
Micrografía de un linfoma de células del manto (zona inferior de la imagen)
Autor/a: Nephron
Fuente: Wikipedia
Con una media de seguimiento de 40 meses, la media de la SLP fue de 24,7 meses (VR-CAP) frente a 14,4 (R-CHOP) (RRI=0,63 [0,50, 0,79], P<0,001). La media de la supervivencia global (SG), un criterio de valoración secundario principal, no se alcanzó en los pacientes que recibieron VR-CAP, mientras que la media de la SG fue de 56 meses en los pacientes tratados con R-CHOP (RRI 0,80; P = 0,17). La tasa de respuesta global (TRG) fue del 92% en el grupo del tratamiento experimental y del 90% en el grupo de control (OR=1,4; P=0,275]. La tasa de respuesta completa (RC+RCu) fue del 53% en el grupo del tratamiento experimental y del 42% en el grupo de control (OR =1,7; P = 0,007].
Acontecimientos adversos graves relacionados con la medicación
Globalmente, se notificaron acontecimientos adversos graves relacionados con la medicación en el 38% de los pacientes tratados con VR-CAP y en el 30% de los pacientes tratados con R-CHOP, y acontecimientos adversos relacionados con la medicación de grado ≥3 en el 93% y el 85% de estos pacientes, respectivamente. Los resultados de otros criterios de valoración secundarios en los pacientes tratados con VR-CAP o R-CHOP fueron:
-La media de tiempo hasta la progresión fue de 30,5 y 16,1 meses, respectivamente (RRI 0,58; P < 0,001)
-La media de tiempo hasta el tratamiento posterior contra el linfoma fue de 44,5 y 24,8 meses, respectivamente (RRI 0,50; P < 0,001)
-La media del intervalo sin tratamiento fue de 40,6 y 20,5 meses, respectivamente (RRI 0,50; P < 0,001).
Aunque no era un criterio de valoración especificado de antemano, se obtuvo una tasa de supervivencia a los cuatro años del 64,4% en el grupo experimental y del 53,9% en el grupo de control.
El linfoma de células del manto, un cáncer sanguíneo poco frecuente
VELCADE® (bortezomib) es un medicamento aprobado actualmente en la Unión Europea para tratar el cáncer de la sangre denominado mieloma múltiple. VELCADE® cuenta con un perfil de seguridad predecible y favorable al ratio beneficio-riesgo. Los efectos secundarios más comunes que se ha registrado con VELCADE (bortezomib) son fatiga, eventos gastrointestinales, trombocitopenia transitoria y neuropatía. En Europa, VELCADE no cuenta en la actualidad con autorización para el tratamiento de linfoma de células del manto (LCM).
El linfoma de células del manto (LCM) es un tipo de cáncer sanguíneo poco frecuente y agresivo que suelen padecer personas mayores, y se diagnostica a partir de los 65 años. La enfermedad suele aparecer en los ganglios linfáticos, aunque puede expandirse a otros tejidos como la médula ósea, al hígado y al bazo. La tasa de incidencia entre hombres y mujeres en Europa es de aproximadamente 0,64 y 0,27 casos, respectivamente, por cada 100.000 personas al año. Los pacientes con LCM generalmente tienen un mal pronóstico. La mediana global de supervivencia suele ser de 3 a 4 años y solo de uno a 2 años en los pacientes que han sufrido una primera recaída.
Por ahora, el mieloma múltiple es un cáncer incurable
El mieloma múltiple es un cáncer de la sangre incurable que comienza en la médula ósea y se caracteriza por una proliferación excesiva de células plasmáticas anormales. Es la segunda forma más frecuente de enfermedad maligna de la médula ósea, y una forma relativamente rara de cáncer responsable de alrededor del uno por ciento de todos los cánceres y de alrededor del dos por ciento de las muertes por tumor. En Europa hay cerca de 60.000 personas con la enfermedad, y se producen 21.420 casos nuevos y 15.000 fallecimientos cada año.




