Las Enfermedades Inflamatorias Intestinales (EII) son un grupo de enfermedades autoinmunes/autoinflamatorias crónicas del tracto gastrointestinal que presentan características comunes como diarrea persistente, dolor abdominal y sangrado rectal, acompañadas de fatiga y pérdida de peso, y que afectan globalmente a más de 7 millones de personas. La incidencia más elevada de las EII se observa en los países industrializados, aunque estudios recientes indican una aceleración de su incidencia en los países en vías de desarrollo1. De hecho, se ha estimado una prevalencia de EII cercana a 1% de la población mundial hacia 2030.
Las manifestaciones más frecuentes de las EII son la enfermedad de Crohn (EC) y la colitis ulcerosa (CU). Ambas difieren en su presentación clínica; la EC puede abarcar todo el tracto gastrointestinal y la inflamación subyacente es irregular y transmural, mientras que la CU se suscribe al colon y recto, siendo el patrón inflamatorio más regular y localizado esencialmente en la mucosa epitelial.

Dr. Josep M. Aran
Dr. Aran
Se desconoce aún la etiología de las EII, si bien existen tres factores causales principales que determinan su incidencia. Por un lado, el acervo genético personal influye directamente en la aparición y gravedad de las EII. Así, mediante análisis GWAS y metaanálisis, se han identificado recientemente de manera fiable cerca de 300 loci asociados a EII, pertenecientes a diferentes genes relacionados con detección microbiana, autofagia, señalización mediada por citoquinas, barrera epitelial y regulación linfocitaria, cuyas variantes incrementarían la predisposición a padecer EC o CU, y el inicio o la gravedad de éstas2.
Por otro lado, se encuentran los factores epigenéticos como las condiciones ambientales (dieta y estilo de vida, polución …), determinantes psicosociales (estrés, burnout…) y, particularmente, el microbioma intestinal. Así, los últimos avances en clasificación y secuenciación del metagenoma, así como el análisis del metaboloma subyacente, han sugerido que la disbiosis intestinal es un determinante clave en la aparición, gravedad y evolución de las exacerbaciones recurrentes que padecen los individuos afectos de EII3.
Finalmente, otro factor fundamental en el desarrollo de las EII es el sistema inmune. Hay que destacar que aproximadamente el 70% del sistema inmune se asocia al tracto gastrointestinal, de ahí su enorme influencia en dichas patologías. Por lo tanto, la desregulación a nivel molecular de la compleja interacción entre los diferentes tipos celulares que componen el sistema inmune, además de un epitelio intestinal permeable y las bacterias que componen el microbioma, inducen el proceso inmunoinflamatorio que caracteriza a las EII4.
Las EII son muy incapacitantes: aparte de reducir sustancialmente la calidad de vida de las personas que las padecen, su impacto médico, social, laboral y emocional es enorme. Además, incrementan la probabilidad de padecer un cáncer colorrectal y suponen una carga sustancial para los sistemas nacionales de salud.
Estrategias terapéuticas para las EII
Las EII siguen siendo hoy en día incurables. Los fármacos convencionales para aliviar sus síntomas se utilizan dependiendo de la gravedad de los episodios. En los pacientes con EII leves o con tratamiento de mantenimiento, los salicilatos junto con otros antiinflamatorios y los antibióticos han mostrado eficacia, aunque limitada. En las EII que se presentan con una clínica moderada se dispone de corticosteroides y fármacos inmunosupresores como el metotrexato, las tiopurinas o la ciclosporina. Sin embargo, el tratamiento crónico con dichos fármacos, además de presentar una eficacia restringida, induce un amplio espectro de efectos adversos significativos, como alteraciones metabólicas, efectos óseos y trastornos neurológicos, gastrointestinales y endocrinos, así como mielotoxicidad, nefrotoxicidad, hipertensión o incremento del riesgo de infecciones y neoplasias, entre otros, que desaconsejan su uso prolongado. Alternativamente, para casos moderados a graves, la resección quirúrgica (colectomía) proporciona una alternativa, aunque dicha metodología es invasiva y no es universalmente aplicable.
Por lo tanto, se están invirtiendo grandes esfuerzos en Investigación y Desarrollo (I+D) para lograr fármacos que sean más seguros y efectivos a fin de mitigar o revertir los síntomas de las EII, tanto a nivel clínico como a nivel endoscópico e histológico. Existen dos grandes grupos de medicamentos dirigidos al tratamiento de las formas moderadas-graves de EII: las moléculas pequeñas, mayoritariamente de origen químico, y los biológicos, mayoritariamente anticuerpos monoclonales. En ambos casos las dianas respectivas están ligadas directa o indirectamente al sistema inmune, de ahí que, en términos generales, hablemos de inmunoterapia.
Actualmente se están investigando multitud de fármacos, aún en fase experimental o en ensayos clínicos, si bien resultaría imposible detallarlos todos en este artículo, por lo que me he centrado en los que, según mi opinión, podrían ser los más representativos y/o prometedores.
Entre los fármacos sintéticos químicos podemos destacar, en primer lugar, los inhibidores de las quinasas Janus (JAK), enzimas clave en la inducción de citoquinas proinflamatorias. Dichos medicamentos, entre los que se encuentran tofacitinib, filgotinib y upadacitinib, se administran por vía oral y han demostrado cierta eficacia induciendo remisión clínica y endoscópica. Sin embargo, pueden presentar también efectos adversos relevantes como infecciones, neoplasias, trombosis o eventos cardiovasculares, que hacen necesaria la estratificación y/o monitorización exhaustiva en pacientes de riesgo o de edad avanzada5.
Otro grupo a tener en cuenta son los moduladores de los receptores del fosfolípido esfingosina-1-fosfato (S1P), como el ozanimod, el etrasimod o el fingolimod, que, administrados por vía oral, reducen la migración de los linfocitos desde los nódulos linfáticos a la mucosa gastrointestinal, mitigando con ello la inflamación asociada a las EII. En determinadas condiciones, los moduladores de los receptores de S1P han mostrado una eficacia modesta a corto plazo, consiguiéndose aproximadamente un 50% de respuesta al tratamiento. Con todo, dichos moduladores presentan también efectos adversos como bradicardia, infecciones, cefaleas, hipertensión y hepatotoxicidad6.

Autor/a: YURIMA
Fuente: depositphotos.com
Dos ejemplos representativos de otros fármacos más recientes -aún en proceso de investigación- que pueden resultar prometedores para las EII son:
1) el péptido oral modulador del receptor de IL23 (IL23R) denominado icotrokinra, un potente inhibidor selectivo de la señalización de la citoquina proinflamatoria IL-23 en linfocitos T7. Se acaban de publicar los resultados de un ensayo de Fase 2 de eficacia terapéutica con este compuesto (ANTHEM-UC), que indican que la administración de una píldora diaria de 400 mg logra una respuesta clínica en adultos afectos de CU moderada-severa. Así, el 36,5% de los pacientes con icotrokinra versus el 14,3% de los pacientes con placebo alcanzaron una mejora a nivel endoscópico, con un perfil de seguridad favorable.
2) Los microRNAs (miRNAs) son un grupo de ARNs no codificantes de pequeño tamaño que tienen un papel clave en la regulación de diferentes procesos fisiológicos y patológicos, entre ellos los procesos inmunoinflamatorios. Obefazimod es una molécula química de pequeño tamaño (quinolina) que, administrada por vía oral, posee actividad antiinflamatoria al inducir la sobreexpresión selectiva del miR-124, un modulador endógeno de la inflamación y de la inmunidad innata, mediante un proceso de corte y empalme (splicing) selectivo8. Este novedoso fármaco se mostró efectivo reduciendo la inflamación y el daño intestinal en un modelo murino de CU mediado por el irritante sulfato de dextrano (DSS). Los resultados obtenidos recientemente en un ensayo clínico de Fase 3 en pacientes con CU moderada-severa a los cuales se les administró dicho fármaco por vía oral (una dosis diaria de 50 mg) (ABTECT) indican una tasa de remisión clínica ajustada a placebo del 16,4%, y una tolerabilidad favorable, si bien con algunos efectos secundarios como desórdenes gastrointestinales, fatiga, dolor de espalda y cefaleas9.
Fármacos biológicos
Aunque hace ya casi tres décadas que se incorporó el primer fármaco biológico para el tratamiento de las EII, el desarrollo, utilización y expansión terapéutica de estos medicamentos ha aumentado exponencialmente hasta el punto de que hoy en día acaparan más del 60% de la cuota de mercado en EII para el tratamiento de las condiciones moderadas-severas o refractarias a los tratamientos convencionales. Los medicamentos biológicos son en su mayoría anticuerpos monoclonales, si bien se han generado también proteínas quiméricas, sintetizados todos ellos mediante tecnología de ADN recombinante y producidos en células de mamífero. Están dirigidos contra dianas moleculares extracelulares o solubles que están relacionadas con el sistema inmune y que juegan un papel clave en el desarrollo y/o evolución del proceso inmunoinflamatorio incipiente en las EII.
Los fármacos biológicos presentan una serie de ventajas respecto a las moléculas pequeñas de origen químico, como una mayor eficacia y especificidad, acceso a dianas complejas y efectos adversos reducidos comparados con las moléculas de origen químico. Sin embargo, también pueden presentar limitaciones significativas, como la inmunogenicidad. Además, un porcentaje relevante de pacientes no responde a dichos tratamientos, o inicialmente responden, pero van perdiendo respuesta con el tiempo. Finalmente, los biológicos se administran como inyectables, por lo que, si su eficacia terapéutica es reducida, los pacientes con EII manifiestan falta de adherencia al tratamiento y hasta un 40% abandonan la terapia.
Los primeros biológicos que supusieron un gran avance en cuanto a mejora terapéutica y modificación del curso de la enfermedad estaban dirigidos contra una citoquina proinflamatoria clave en el desarrollo de las EII, el factor de necrosis tumoral alfa (TNF-α). Así, se dispone de biológicos como el infliximab (anticuerpo monoclonal quimérico aún muy utilizado), adalimumab y golimumab (anticuerpos monoclonales humanizados), y certolizumab pegol (fragmento de anticuerpo Fab humanizado y pegilado), la mayoría inyectados actualmente por vía subcutánea en pautas quincenales o mensuales de 100-400 mg. Todos ellos han demostrado una eficacia terapéutica significativa comparados con placebo, aunque inducen una susceptibilidad incrementada a infecciones bacterianas y fúngicas, o pueden empeorar la patología de infecciones víricas crónicas o latentes como la hepatitis B10.
Otros anticuerpos monoclonales humanizados que han demostrado también cierta eficacia terapéutica son los que, estando dirigidos contra integrinas, inhiben la migración de linfocitos T de memoria al tracto gastrointestinal (natalizumab, dirigido a la integrina α4; vedolizumab, que bloquea selectivamente a la integrina α4β7). Aunque con natalizumab persiste también el riesgo de infecciones serias o malignidad, dichos efectos adversos se reducen empleando vedolizumab, al actuar específicamente en el intestino11.
Autor/a: sciencepics
Fuente: depositphotos.com
Más recientemente se han introducido en la práctica clínica para CU y EC distintos biológicos dirigidos contra las citoquinas proinflamatorias IL-12 y/o IL-23. Estos medicamentos, aprobados previamente para otras enfermedades autoinmunes como la psoriasis, juegan también un papel esencial a la hora de actuar contra el inicio y perpetuación de las EII. Ustekinumab es un anticuerpo monoclonal dirigido contra la subunidad p40, compartida por IL-12 e IL-23, mientras que risankizumab, mirikizumab y guselkumab son anticuerpos monoclonales dirigidos específicamente contra la subunidad p19 de la citoquina IL-23. Los resultados disponibles hasta el momento indican que, si bien ustekinumab no se ha asociado con un riesgo incrementado de malignidad, sí puede inducir a un mayor riesgo de infecciones, mientras que los biológicos dirigidos exclusivamente contra IL-23 no se han asociado con un mayor riesgo ni de malignidad ni de infecciones12.
Otro avance significativo supone la irrupción de los biológicos dirigidos contra “tumor necrosis factor-like 1A” (TL1A). Dicha diana, miembro de la superfamilia de los factores de necrosis tumoral (codificada por el gen TNFSF15), es clave en la inducción tanto del proceso inmunoinflamatorio en la mucosa intestinal como de la fibrosis que caracteriza a las EII, de tal modo que su expresión se incrementa en células inmunes activadas mediante estímulos proinflamatorios. Tulisokibart es un anticuerpo monoclonal humanizado anti-TL1A que ha mostrado resultados prometedores en ensayos clínicos de fase 2 en cuanto a eficacia terapéutica y seguridad, tanto para CU como para EC, con una reducción de biomarcadores inflamatorios como la proteína C reactiva y la calprotectina fecal.
Afimkibart es otro anticuerpo humanizado anti-TL1A que bloquea la interacción TL1A-DR3 y que también ha mostrado hasta el momento resultados prometedores de eficacia terapéutica y un aceptable perfil de seguridad, si bien en este ensayo de fase 2 se apreció la inducción de una inmunogenicidad significativa con este biológico, con presencia de anticuerpos contra el fármaco en el 82% de los participantes. Se han iniciado ya ensayos clínicos de fase 3 evaluando ambos biológicos, tanto para CU como para EC13.
Duvakitug es otro anticuerpo monoclonal anti-TL1A en investigación. Para acelerar su desarrollo, dicha molécula está siendo evaluada en un novedoso ensayo clínico de fase 2 con pacientes de CU y de EC (RELIEVE UCCD basket trial), que compara placebo versus dos dosis de 450 mg y 900 mg de duvakitug, examinando la respuesta endoscópica en la semana 14, con el uso de análisis estadísticos bayesianos y frecuentistas. Los resultados iniciales tanto para el grupo de CU como para el grupo de EC parecen prometedores, mostrando una gran probabilidad de eficacia terapéutica posterior para ambas dosis13.
Mención aparte merece la terapia celular. El uso de células madre mesenquimales (MSCs), aunque prometedor, ha mostrado eficacia limitada en un ensayo clínico de fase 3 para fistulas perianales complejas en pacientes con EC14. Finalmente, las células CAR-T obtenidas mediante ingeniería genética, en desarrollo para diferentes enfermedades autoinmunes, pueden suponer una herramienta terapéutica prometedora para las EII, particularmente las células CAR-Tregs (IL23R-CAR-Tregs, …) y CAR-T capaces de eliminar células B (CD19-CAR-T, …), dado el papel central de IL-23, células B y circuitos reguladores en la patogénesis de las EII. Aun así, serán necesarios ensayos clínicos más amplios y exhaustivos para demostrar la eficacia y seguridad a largo plazo de este tipo de intervenciones, cuya implementación a nivel general sigue siendo muy discutible15.
No obstante, hasta el momento todos los fármacos biológicos comercializados o en fases clínicas han mostrado una eficacia terapéutica exigua y efectos adversos relevantes. Además, cerca del 30-40% de los pacientes con EII no responden o pierden respuesta a dichos tratamientos con el tiempo, lo cual acentúa una insuficiente adherencia a los mismos. Por otra parte, queda claro que dirigir los biológicos contra una sola molécula efectora o vía de señalización, por relevante que sea, no está siendo suficiente para controlar la inflamación e incrementar las remisiones clínicas definitivas y la curación de la mucosa intestinal, debido a la gran variedad de rutas de señalización del sistema inmune que juegan un papel relevante en las EII. Consecuentemente, se están ensayando anticuerpos biespecíficos contra, por ejemplo, IL-23 y TL1A y, aunque a nivel preclínico los resultados son esperanzadores, queda por demostrar sus ventajas a nivel clínico respecto a los actuales tratamientos biológicos13.
Por todo ello, se necesitan nuevos inmunomoduladores, dirigidos contra dianas terapéuticas más relevantes y capaces de romper el techo terapéutico actual, con el fin de poder controlar las EII a largo plazo e incrementar sustancialmente la calidad de vida de los pacientes que las padecen.
Heptammune, un nuevo inmunomodulador biológico para las EII
Teniendo en cuenta las anteriores limitaciones, en nuestro laboratorio estamos desarrollando un nuevo biológico inmunomodulador: Heptammune. Este fármaco, primero de su clase, se deriva de la isoforma minoritaria de la proteína humana inhibidora del complemento C4BP(β-), un homooligómero presente en la circulación sanguínea de 530 kilodalton (kDa). C4BP(β-) exhibe una estructura en forma de araña y está conformado por 7 cadenas α idénticas de 8 dominios CCP (“complement control protein”), unidas por su extremo C-terminal a un dominio de oligomerización.
Hace unos años, identificamos que, aparte de la actividad “canónica” inhibidora del sistema del complemento, C4BP(β-) poseía una nueva actividad inmunomoduladora para controlar la inflamación excesiva. Así, C4BP(β-), en contacto directo con células mieloides inflamatorias, inducía un fenotipo antiinflamatorio y tolerogénico a éstas16. Además, diseccionamos los dominios esenciales para preservar dicha actividad, que resultaron ser independientes de los implicados en la inhibición del complemento. A partir de dicha información, creamos Heptammune (PRP6-HO7) fusionando el dominio inmunomodulador (CCP6) y el dominio de oligomerización de C4BP(β-) mediante ingeniería genética, por lo que dicha molécula incluso mejora la actividad inmunomoduladora de la proteína original y carece de actividad inhibidora del complemento, lo que incrementa su seguridad17 (Figura 1).
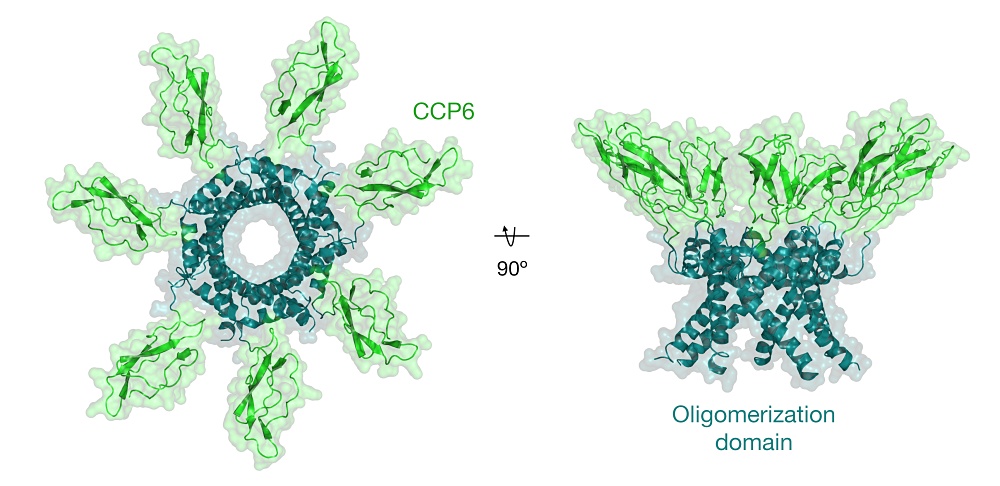
Figura 1. Representación gráfica de la estructura oligomérica de Heptammune (PRP6-HO7) predicha a partir de modelaje molecular. El dominio CCP6 N-terminal y el dominio de oligomerización C-terminal se muestran en verde y azul, respectivamente
Figura modificada de referencia 17
El homooligómero Heptammune posee, pues, un tamaño algo menor que un anticuerpo monoclonal y es una molécula compacta, muy estable y, según ensayos preliminares, carece de inmunogenicidad. Dicha proteína no está glicosilada y ha podido producirse tanto en sistemas de expresión procariota (E.coli) como eucariota (células CHO). Por otra parte, dicho biológico presenta un nuevo mecanismo de acción. A diferencia de los actuales biológicos, que bloquean o eliminan moléculas (citoquinas proinflamatorias, integrinas, ...) o células efectoras (linfocitos B, ...), Heptammune actúa de manera eficiente “reprogramando” células mieloides del sistema inmune innato, células que son claves en el desarrollo de las EII, pero que no están siendo abordadas por las terapias actuales.
Dicha “reprogramación” se induce a nivel metabólico y epigenético y, consecuentemente, afecta a múltiples vías de señalización en dichas células, revirtiendo un fenotipo proinflamatorio e inmunogénico, presente en la mucosa intestinal de los pacientes con EII, hacia un fenotipo antiinflamatorio, antioxidante y tolerogénico, capaz de generar células T reguladoras. Por lo tanto, Heptammune es un inmunomodulador, no un inmunosupresor.
En ensayos de prueba de concepto, hemos confirmado la eficacia terapéutica de Heptammune in vivo, en modelos murinos de CU, e in vitro en células inmunes de pacientes con EII. Así, en ratones a los que se les había inducido CU mediante el irritante DSS, la inmunomodulación mediada por Heptammune administrado por vía subcutánea atenuó significativamente los rasgos histopatológicos y preservó la integridad del epitelio intestinal. Dicho biológico disminuyó la expresión de transcritos inflamatorios, en particular los relacionados con la actividad de los neutrófilos, mitigó las citoquinas y quimioquinas efectoras inflamatorias circulantes, como CXCL13, clave en la generación de estructuras linfoides ectópicas, y, en general, previno la infiltración de células inmunitarias inflamatorias en el colon de ratones con CU18.
En un modelo de CU aguda en ratas, hemos demostrado también que una única administración subcutánea de Heptammune a una dosis de 2,5 mg/kg, cuando las ratas ya presentaban la enfermedad, fue capaz de resolver la inflamación subyacente y de preservar la integridad del epitelio intestinal (resultados aún no publicados). Finalmente, Heptammune fue capaz de reducir de manera significativa los marcadores inflamatorios intrínsecos e inducidos por receptores proinflamatorios (toll-like receptors; TLR) en células mieloides de pacientes con CU y EC, independientemente de su medicación18.
Asimismo, hemos diseñado un análisis de sangre predictivo que facilitaría la estratificación y/o monitorización de los pacientes con EII tratados con Heptammune hacia una medicina personalizada.
Conclusiones
Aun con el amplio abanico de fármacos disponibles actualmente frente a las EII, se ha estimado que solamente cerca del 25% de pacientes alcanza la remisión clínica después de un tratamiento de inducción. Teniendo en cuenta que la remisión clínica del tratamiento con placebo se aproxima al 10%, existe claramente un amplio margen de mejora terapéutica en los futuros fármacos para las EII. Además, mientras que algunos pacientes con estas patologías experimentan mejoras significativas, otros no responden al tratamiento.
Por lo tanto, hacen falta estrategias terapéuticas personalizadas y medicina de precisión, teniendo en cuenta las características ómicas (genoma, transcriptoma, proteoma, metaboloma, microbioma) y clínicas de cada paciente junto con las propiedades del fármaco o combinación de fármacos más adecuada, e integrando dicha información con otras bases de datos (ensayos clínicos ...) mediante la ayuda de la inteligencia artificial, para predecir la respuesta terapéutica y los posibles efectos adversos asociados en cada caso. Todo ello, con el fin de potenciar los medicamentos disponibles en el mercado y alcanzar la máxima eficacia terapéutica.
Aun así, para resolver las necesidades clínicas no cubiertas -y hacerlo de forma efectiva- en el máximo número posible de pacientes con EII, serán necesarios fármacos más seguros y eficaces y, en esta línea, que sean verdaderos modificadores del curso de la enfermedad. Heptammune es una molécula derivada de una proteína fisiológica, con un nuevo mecanismo de acción pleiotrópico capaz de restaurar la homeostasis de la mucosa intestinal reiniciando localmente el sistema inmune y resolviendo la inflamación subyacente sin causar daños colaterales. El desarrollo clínico de dicho biológico innovador podría romper el techo terapéutico que presentan los actuales medicamentos e inducir la remisión a largo plazo y el incremento de la calidad de vida en un amplio número de pacientes con EII.
Agradecimientos
Agradecemos al Programa CERCA/Generalitat de Catalunya el apoyo institucional. Este trabajo fue subvencionado por el Ministerio de Ciencia, Innovación y Universidades (FIS-ISCIII PI23/00285; PI20/00464 y DTS20/00016), y el “Departament de Recerca i Universitats de la Generalitat de Catalunya” (2019PROD00081, 2021INNOV00020 y 2021SGR00521), todo ello cofinanciado por fondos FEDER/Fondo Europeo de Desarrollo Regional (FEDER)-una manera de construir Europa-. Además, el proyecto que ha dado lugar a estos resultados ha recibido financiación y apoyo de la Fundación “la Caixa” a través de las ayudas CI22-00230 y CI24-30620.
Bibliografía
1. Hracs L, Windsor JW, Gorospe J, Cummings M, Coward S, Buie MJ, et al. Global evolution of inflammatory bowel disease across epidemiologic stages. Nature. 2025;642(8067):458-466.
2. Liu Z, Liu R, Gao H, Jung S, Gao X, Sun R, et al. Genetic architecture of the inflammatory bowel diseases across East Asian and European ancestries. Nat Genet. 2023;55(5):796-806.
3. Santana PT, Rosas SLB, Ribeiro BE, Marinho Y, de Souza HSP. Dysbiosis in Inflammatory Bowel Disease: Pathogenic Role and Potential Therapeutic Targets. Int J Mol Sci. 2022;23(7):3464.
4. Vindigni SM, Zisman TL, Suskind DL, Damman CJ. The intestinal microbiome, barrier function, and immune system in inflammatory bowel disease: a tripartite pathophysiological circuit with implications for new therapeutic directions. Therap Adv Gastroenterol. 2016;9(4):606-625.
5. Ahsan MU, Sajid SL, Balach R, Daniyal M, Ain NU, Mudasir M. Emerging role of Janus kinase inhibitors in ulcerative colitis management. World J Gastrointest Pharmacol Ther. 2025;16(4):110472.
6. Shields N, Colwill M, Raspa V, Twum-Danso Y, Poullis A, Patel K, et al. Sphingosine-1-Phosphate (S1P) Receptor Modulators for the Treatment of Inflammatory Bowel Disease (IBD): Mechanisms, Clinical Evidence, and Practical Insights. Biomedicines. 2025;13(11):2655.
7. Knight B, Tammara B, Modi NB, Dallas S, Mardirosian S, Wang J, et al. Translational Pharmacokinetics of Icotrokinra, a Targeted Oral Peptide that Selectively Blocks Interleukin-23 Receptor and Inhibits Signaling. Dermatol Ther (Heidelb). 2025;15(9):2495-2520.
8. Vermeire S, Solitano V, Peyrin-Biroulet L, Tilg H, Danese S, Ehrlich H, et al. Obefazimod: A First-in-class Drug for the Treatment of Ulcerative Colitis. J Crohns Colitis. 2023;17(10):1689-1697.
9. Scaldaferri F, Seidler U, Tretón X, D’Amico F, Armuzzi A, Howaldt S, et al. P1159 Pooled analysis of efficacy and safety of once-daily oral obefazimod in European patients from the ABTECT Phase 3, double-blind, placebo-controlled induction trials. J Crohns Colitis. 2026;20(Suppl_1):jjaf231.1340.
10. Orfanoudaki E, Foteinogiannopoulou K, Theodoraki E, Koutroubakis IE. Recent Advances in the Optimization of Anti-TNF Treatment in Patients with Inflammatory Bowel Disease. J Clin Med. 2023;12(7):2452.
11. Gubatan J, Keyashian K, Rubin SJS, Wang J, Buckman CA, Sinha S. Anti-Integrins for the Treatment of Inflammatory Bowel Disease: Current Evidence and Perspectives. Clin Exp Gastroenterol. 2021;14:333-342.
12. Pugliano CL, Liang RF, Ruffa A, Iacucci M, Ghosh S. Practical considerations for the use of IL-23p19 inhibitors in inflammatory bowel disease: how to choose between them and why it matters? J Crohns Colitis. 2025;19(8):jjaf144.
13. Estevinho MM, Noor NM. Innovative pipeline therapeutics in inflammatory bowel disease: Anti-tumor necrosis factor-like ligand 1A and bispecific antibodies. Curr Opin Pharmacol. 2025;86:102596.
14. Lightner AL, Reese JS, Ream J, Nachand D, Dadgar N, Adams A, et al. A phase IB/IIA study of ex vivo expanded allogeneic bone marrow-derived mesenchymal stem cells for the treatment of rectovaginal fistulizing Crohn’s disease. Surgery. 2024;175(2):242-249.
15. Neurath MF, Sands BE, Rieder F. Cellular immunotherapies and immune cell depleting therapies in inflammatory bowel diseases: the next magic bullet? Gut. 2024;74(1): 9-14.
16. Olivar R, Luque A, Naranjo-Gómez M, Quer J, García de Frutos P, Borràs FE, et al. The α7β0 isoform of the complement regulator C4b-binding protein induces a semimature, anti-inflammatory state in dendritic cells. J Immunol. 2013;190(6):2857-2872.
17. Serrano I, Luque A, Mitjavila F, Blom AM, Rodríguez de Córdoba S, Vega MC, et al. The Hidden Side of Complement Regulator C4BP: Dissection and Evaluation of Its Immunomodulatory Activity. Front Immunol. 2022;13:883743.
18. Serrano I, Luque A, Ruiz-Cerulla A, Navas S, Blom AM, Rodríguez de Córdoba S, et al. C4BP(β-)-mediated immunomodulation attenuates inflammation in DSS-induced murine colitis and in myeloid cells from IBD patients. Pharmacol Res. 2023;197:106948.




