Redacción Farmacosalud.com
Kisqali® (ribociclib), de la compañía Novartis, ha sido autorizado en España para dos nuevas indicaciones en cáncer de mama localmente avanzado o metastásico. Una de ellas, la que contempla el uso del fármaco en combinación con un análogo de LHRH en mujeres premenopáusicas, permite retrasar hasta 27 meses la administración de quimioterapia. La otra indicación, la que consiste en combinar ribociclib con fulvestrant, parte de la proyección de que pueda retrasar la aplicación de la ‘quimio’ durante dos años y medio e incluso tres en mujeres postmenopáusicas, notifica el Dr. José Ángel García Sáenz, oncólogo médico de la Unidad de Cáncer de Mama del Hospital Clínico San Carlos (Madrid) y vocal de la Junta directiva del Grupo GEICAM de Investigación en Cáncer de Mama.
Ribociclib ha sido autorizado en España en combinación con un agonista de hormona liberadora de la hormona luteinizante (LHRH) para mujeres premenopáusicas y perimenopáusicas con cáncer de mama localmente avanzado o metastásico HR+/HER2-. También ha sido autorizado en combinación con fulvestrant como terapia endocrina, para el tratamiento de mujeres premenopáusicas y postmenopáusicas con el mismo tumor mamario. Previamente a esas dos indicaciones, en España ribociclib ya tenía luz verde desde 2017 -en combinación con letrozol- para tratar el cáncer de mama en primera línea en mujeres postmenopáusicas. Cada año hay en España unos 32.000 nuevos casos de tumor mamario; se calcula que unas 2.000 mujeres (algo más del 6% del total de casos) podrían beneficiarse de las nuevas indicaciones de ribociclib.

Dr. José Ángel García Sáenz
Fuente: GEICAM
Un cambio de paradigma en el tratamiento del tumor mamario
Ribociclib es un inhibidor selectivo de las CDK4/6 que ayuda a retardar la progresión del cáncer mediante la inhibición de dos proteínas llamadas quinasas dependientes de ciclinas 4 y 6 (CDK4/6). Este complejo proteínico se ocupa de activar o desactivar el freno del ciclo celular, freno que depende de una proteína denominada retinoblastoma. Así, en condiciones de progresión de un cáncer, la proteína de la retinoblastoma está inactivada, con lo cual el ciclo celular es ‘eterno’ y hay proliferación tumoral y por tanto metástasis. Ribociclib actúa sobre las quinasas dependientes de ciclinas y evita que se inactive el agente retinoblastómico, lo que significa que se retrasa o para el crecimiento de la célula tumoral y se controla la enfermedad.
El nuevo fármaco ha supuesto un cambio de paradigma en el tratamiento del cáncer de mama. “Teníamos la sensación de que, en las mujeres premenopáusicas, la afección era biológicamente más agresiva que en las postmenopáusicas, y en todas ellas hasta hace pocos meses empezábamos el tratamiento con quimioterapia. Gracias la incorporación de ribociclib -particularmente en cáncer de mama premenopáusico- estamos retrasando mucho el inicio de la quimioterapia”.
“La mediana de control del cáncer de mama premenopáusico con el uso de ribociclib en combinación con goserelina (un análogo de LHRH) y letrozol es de aproximadamente 27 meses, o sea, es algo espectacular, porque una quimioterapia antineoplásica no te consigue un control de la enfermedad más allá de 7-8 meses. Y, cuando la terapia endocrina deja de actuar, estas mujeres tienen incluso una posibilidad de continuar con una segunda terapia hormonal que les puede dar algún mes adicional libre de quimioterapia, con lo cual podemos estar hablando de cerca de dos años y medio a tres años para el comienzo de una ‘quimio’, cuando antes, hace poco tiempo, se trataban con este procedimiento ya de inicio”. Para el Dr. García Sáenz, “la gran novedad es que ribociclib es el único fármaco de su clase que ha demostrado actividad en primera línea en una población premenopáusica con cáncer de mama metastásico”.
En cuanto a las pacientes postmenopáusicas, fulvestrant en monoterapia comporta un control de la patología durante un año y medio (18 meses). Al añadir ribociclib, ese período libre de ‘quimio’ aumenta: si bien la mediana de control de la afección todavía no se ha alcanzado en los estudios porque no ha habido eventos, hay que tener en cuenta que, en la fase ratio o de riesgo relativo, la mediana de retraso del evento gira en torno a un 45%, con lo que “la proyección de cuánto tiempo vamos a controlar la enfermedad con ribociclib + fulvestrant es espectacular”, asegura el facultativo. Tanto es así, que “cuando los datos sean ya maduros en los próximos meses, probablemente controlaremos la enfermedad más allá de los dos años y medio o cerca de tres”, pronostica.
Ribociclib + ‘quimio’, incompatibles si se administran de manera concomitante
Llegado el caso de tener que administrar quimioterapia, cabe destacar que la estrategia quimioterápica no es compatible con la administración de ribociclib de manera concomitante. Aunque se considera que el perfil de seguridad de ribociclib es bueno, cabe destacar que este fármaco produce neutropenia (predisposición a contraer infecciones por reducción de granulocitos de la sangre), si bien es diferente a la neutropenia causada por la quimioterapia. Sea como fuere, la combinación simultánea de ambos tratamientos está contraindicada. “Sin embargo -señala el vocal de GEICAM-, el uso de ribociclib no supone una contraindicación para que a los 2-3-4 años la paciente pueda recibir quimioterapia sin ningún problema… ribociclib no deja una secuela que haga perder la oportunidad de someterse a ‘quimio’ en caso de que fuera necesario recurrir a este tratamiento”.
Autor/a: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
Según el Dr. García Sáenz, los eventos adversos asociados a las dos nuevas indicaciones de ribociclib “son fáciles de manejar por parte del oncólogo”. Y, aunque es cierto que ahí está la neutropenia, ésta es diferente de la causada por la ‘quimio’, “ya que no se produce una apoptosis del granulocito amenazante para la vida”, sino que hay como un retraso en el crecimiento del granulocito, lo que comporta que la paciente se recupere rápidamente de la afección neutropénica, comenta el especialista. En el caso de la neutropenia febril -que es la que motiva el ingreso hospitalario de las personas sometidas a quimioterapia-, la causada por ribociclib “es una neutropenia más estética que amenazante para la vida, y además no tiene la toxicidad propia de la ‘quimio’ (alopecia, náuseas, etc)”, refiere.
El uso de ribociclib presenta tantas ventajas en términos de calidad de vida, que “cuando tratas en primera línea a una mujer con cáncer de mama y la paciente va a consulta acompañada por su hermana o por su madre, cuando se levantan no sabes quién es la enferma y quién es la acompañante. En cambio, las secuelas físicas de la quimioterapia son inequívocas. Incluso en mujeres premenopáusicas, ribociclib no sólo ha demostrado que no impacta negativamente en la calidad de vida, sino que la mejora notablemente, es decir, las pacientes controlan más la enfermedad y viven mejor. En definitiva, gracias a la introducción de estas dos nuevas indicaciones estamos consiguiendo un mayor bienestar, un mayor control de la enfermedad, un retraso en la aplicación de la quimioterapia, y todo ello, además, con un perfil de seguridad farmacológica bastante notable…estamos consiguiendo que las pacientes vivan más y mejor”.
La nueva autorización en España de ribociclib, tan solo un mes y medio después de la aprobación europea, se basa en los resultados de dos ensayos clínicos, MONALEESA-3 y MONALEESA-7.
‘Células asesinas naturales’ y el cáncer de mama más agresivo
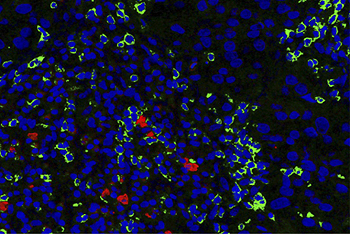
Linfocitos NK en tumor de mama HER2 positivo. Imagen de un carcinoma infiltrante de mama HER2 positivo, donde se muestra los linfocitos NK (en rojo) y los linfocitos T (verdes) presentes en el estroma tumoral. Imagen de pseudofluorescencia obtenida por técnicas de doble inmunohistoquímica y análisis de imagen asistida por ordenador
Fuente: Hospital del Mar
Por otro lado, las pacientes con uno de los tipos de cáncer de mama más agresivo, el HER2 positivo, tienen más opciones de obtener una respuesta completa al tratamiento si los tumores presentan niveles altos de un tipo concreto de linfocito, las llamadas células asesinas naturales, en inglés Natural Killer cells (NK). Es la primera vez que se evidencia esta relación en los tumores de personas con tumor mamario, lo que supone un paso de gran importancia para encontrar marcadores que indiquen el nivel de respuesta de las pacientes a los medicamentos que se utilizan. A la vez, este descubrimiento[1], que publica la revista ‘Clinical Cancer Research’, indica nuevas formas de reforzar la capacidad de los tratamientos existentes y de aquellos en fase de ensayo para acabar con los tumores, y abre la puerta a estudiar la posibilidad de trasplantar este tipo de célula en combinación con anticuerpos monoclonales.
El estudio lo han liderado investigadores del Hospital del Mar, del Instituto Hospital del Mar de Investigaciones Médicas (IMIM) y de la Universidad Pompeu Fabra, con la colaboración de profesionales de la Fundación Jiménez Díaz de Madrid y del Hospital Clínico de Valencia, así como del Institut de Recerca en Biomedicina (IRB) de Barcelona. En él, se han utilizado muestras de más de un centenar de pacientes con cáncer de mama HER2 positivo. Los resultados del estudio han permitido a los investigadores concluir que aquellas pacientes que presentaban niveles altos de células NK en el tumor, y que habían sido tratadas antes de la cirugía con anticuerpos monoclonales contra HER2, tenían más posibilidades de lograr una respuesta completa de la enfermedad al tratamiento. Por contra, en los casos con niveles bajos de NK, raramente se lograba una remisión completa.
Esta relación entre linfocitos NK y respuesta al tratamiento indica la posible participación del sistema inmunitario en la acción antitumoral de estos fármacos. “El anticuerpo monoclonal hace de puente entre la célula tumoral HER2 positiva y la célula NK, que, a través de esta unión, perfora las células tumorales y introduce material citotóxico que las destruye”, explica el Dr. Joan Albanell, jefe del Servicio de Oncología Médica del Hospital del Mar, investigador CIBERONC y director del Programa de investigación en cáncer del IMIM, último firmante del estudio conjuntamente con el Dr. Miguel López-Botet, jefe del Servicio de Inmunología del Hospital del Mar y coordinador del Grupo de investigación en Inmunidad e Infección del IMIM, ambos catedráticos de la Universidad Pompeu Fabra.

Firmantes del estudio (de izq. a dcha): Drs. Joan Albanell, Ignasi Tusquets, Miguel López-Botet, Sònia Servitja y Aura Muntasell
Fuente: Hospital del Mar
Tecentriq + abraxane para el cáncer de mama triple negativo
La compañía Roche ha anunciado que la Agencia Americana del Medicamento (FDA por sus siglas en inglés) ha otorgado la aprobación acelerada a la combinación de Tecentriq® (atezolizumab) más quimioterapia (Abraxane® [paclitaxel ligado a albúmina para suspensión inyectable; nab-paclitaxel]) para el tratamiento de pacientes adultos con cáncer de mama localmente avanzado irresecable o metastásico, en tumores con expresión PD-L1, determinado con una prueba FDA aprobada. Esta indicación tiene luz verde bajo el procedimiento acelerado en función de los datos de supervivencia libre de progresión (SLP) obtenidos en estas pacientes. La aprobación definitiva de la misma depende de la verificación de este beneficio clínico en un ensayo confirmatorio. El programa de aprobación acelerada de la FDA permite la comercialización condicional de un medicamento que satisface una necesidad médica no cubierta en una patología grave o potencialmente mortal.
Ingesta calórica elevada y cáncer de mama
Finalmente, cabe destacar que las mujeres españolas con una ingesta calórica por encima de sus requerimientos energéticos individuales presentan un mayor riesgo de padecer un cáncer de mama, mientras que una restricción calórica parece prevenir el riesgo de desarrollar este tumor. Así lo ha puesto de manifiesto un estudio[2] epidemiológico llevado a cabo por investigadores del Instituto de Salud Carlos III pertenecientes a CIBERESP y el grupo GEICAM de Investigación en Cáncer de Mama, y financiado por la Asociación Española Contra el Cáncer (AECC). Estos resultados han sido publicados recientemente en la revista ‘Scientific Reports’ del Grupo ‘Nature’.
El cáncer de mama, con 32.825 casos nuevos en 2018, es el tumor más frecuente en mujeres españolas. Constituye el 29% de los casos de cáncer en mujeres, por lo que se considera un problema importante de salud pública. Existe clara evidencia de que la obesidad y la ganancia de peso son importantes factores de riesgo del tumor mamario en mujeres postmenopáusicas.
Referencias
1. Aura Muntasell, Federico Rojo, Sonia Servitja, Carlota Rubio-Perez, Mariona Cabo, David Tamborero, Marcel Costa-Garcia, Maria Martinez-Garcia, Silvia Menéndez, Ivonne Vazquez, Ana Lluch, Abel Gonzalez-Perez, Ana Rovira, Miguel Lopez-Botet and Joan Albanell. NK cell infiltrates and HLA class I expression in primary HER2+ breast cancer predict and uncouple pathological response and disease-free survival. Clin Cancer Res December 6 2018 DOI: 10.1158/1078-0432.CCR-18-2365
2. Lope V, Martín M, Castelló A, Ruiz A, et al. Overeating, caloric restriction and breast cancer risk by pathologic subtype: the EPIGEICAM study. Sci Rep. 2019 Mar 7;9(1):3904. doi: 10.1038/s41598-019-39346-4. https://www.nature.com/articles/s41598-019-39346-4 www.ncbi.nlm.nih.gov/pubmed/30846706




