Introducción
La fibrosis intestinal en la enfermedad de Crohn (EC) es un proceso largo y continuo que se inicia con cambios moleculares proinflamatorios y profibróticos y que finalmente conduce a la aparición de estenosis intestinales que condicionan síntomas obstructivos en los pacientes. La aparición de estenosis intestinales empeora la calidad de vida de los pacientes secundariamente al dolor abdominal y las restricciones dietéticas, y obliga a la instauración de tratamientos endoscópicos y/o quirúrgicos1.
La fibrosis y, como consecuencia, las estenosis intestinales son tan frecuentes en la EC que, por sí mismas, originan un fenotipo específico de la enfermedad (fenotipo estenosante o B2 de la clasificación de Montreal), especialmente en pacientes no tratados o de más larga evolución2. En el estudio de Cosnes et al3 en 2002, en personas con EC la tasa de evolución a un fenotipo estenosante en 20 años fue del 18%, con mayor incidencia en los individuos con afectación ileal. Datos más recientes de un estudio prospectivo europeo confirman que los datos de progresión de la enfermedad son similares a los de las cohortes de hace más de 20 años. Así, un 21% de los pacientes con EC debutan con un fenotipo estenosante que se incrementa en un 10% 5 años después del diagnóstico4. La consecuencia más evidente, en último término, de la fibrosis intestinal es el daño intestinal y la discapacidad secundaria a las estenosis y resecciones quirúrgicas.

Dra. Natalia Borruel Sainz
Fuente: Dra. Borruel Sainz
El tratamiento de las estenosis intestinales ya establecidas y sintomáticas se basa fundamentalmente en la endoscopia y la cirugía. Las diferentes guías clínicas recomiendan el tratamiento con terapias avanzadas en los casos en los que en la estenosis coexista inflamación activa y tratamientos endoscópicos (dilatación con balón) o quirúrgicos (resección intestinal y/o estricturoplastia) en los pacientes con estenosis sintomáticas5,6. La resección intestinal, especialmente en pacientes con EC y afectación ileal, sigue siendo frecuente a pesar del uso cada vez mayor de tratamientos farmacológicos avanzados. En un estudio español publicado recientemente con datos de la base ENEIDA del Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa (GETECCU), en 17.292 pacientes con EC seguidos durante una mediana de 6 años, la tasa de cirugía en las formas ileales o ileocolónicas fue del 18% y 16%, respectivamente. La localización ileal se asociaba con una mayor probabilidad de requerir una cirugía que la localización exclusivamente colónica (HR 2.82,95%CI 2.45–3.25)7.
Fisiopatología de la fibrosis
En condiciones normales, la fibrosis, consecuencia del depósito de matriz extracelular (MEC), es un proceso bien regulado e imprescindible en la reparación tisular fisiológica en el que interactúan diferentes componentes tanto de la MEC como del sistema inmune8. Ante una agresión externa (infección, tóxico, fármacos, factores ambientales), el órgano afectado sufre una lesión tisular que a su vez induce el reclutamiento de macrófagos residentes (células presentadoras de antígenos) que secretan citoquinas que activan y amplifican la respuesta inflamatoria mediante el reclutamiento de otras células inmunes. Además, aumenta la producción de factores profibróticos que estimulan a los fibroblastos para producir y depositar MEC.
Cuando el depósito de MEC es suficiente, el sistema inmune adopta un fenotipo regulador que frena estas respuestas promoviendo la producción de citoquinas antiinflamatorias y metaloproteinasas para degradar el exceso de tejido fibrótico y, de este modo, conducir a la reparación del daño tisular. Por el contrario, en situaciones en las que una inflamación crónica, como en la EC, este proceso de inflamación-depósito de MEC no se frena, conduce a la fibrosis, la destrucción de la arquitectura tisular y la pérdida de función del órgano.
La fibrosis es, por tanto, un fenómeno complejo y multifactorial en el que están involucradas células inmunes y no inmunes (células mesenquimales, epiteliales, endoteliales) y diferentes mediadores solubles. En la Enfermedad Inflamatoria Intestinal (EII) -en la que se incluye la EC-, la fibrosis aparece en las zonas inflamadas y guarda relación con el grado de inflamación, ya que el medio inflamatorio es crítico para iniciar y perpetuar la fibrosis. Diferentes estudios han demostrado que en el tejido intestinal inflamado de pacientes con EC existe un aumento de células mesenquimales productoras de MEC que proliferan y migran. En el tejido, las células mesenquimales adoptan un fenotipo activado al exponerse a múltiples mediadores solubles (citoquinas, factores de crecimiento) liberados por células inmunes/no inmunes y, debido a su plasticidad, se diferencian en fibroblastos, miofibroblastos y células de músculo liso9.
Las células mesenquimales están expuestas no sólo al contacto directo con las células intestinales inmunes y no inmunes, sino también a sus mediadores. Entre los mediadores de la fibrosis intestinal destaca TGFβ1, factor de crecimiento profibrótico que está sobreexpresado en los miofibroblastos del tejido fibrótico intestinal de pacientes con EC, y que induce en estas células la expresión de α-actina, fibronectina y colágeno10. Los mecanismos moleculares implicados en la fibrosis son complejos e involucran a múltiples citoquinas, quimiocinas y otras moléculas como metaloproteinasas, TIMP1, cadherina 11, IL-11, IL-23, IL-17, IL-33, IL-34, IL-36 o TNF-like 1A (TL1A).
Autor/a: magicmine
Fuente: depositphotos.com
Estudios para profundizar en los mecanismos de la fibrosis intestinal han identificado nuevos actores involucrados como la microbiota intestinal, la “creeping fat” (tejido graso mesentérico patológicamente alterado) o la existencia de fibroblastos específicos fibrogénicos con capacidad no sólo como receptores, sino también como señalizadores de fibrosis por sí mismos. Además, una barrera epitelial 'permeable' debido al daño celular permite el contacto y activación de las células mesenquimales por la microbiota y sus productos a través de la interacción PAMPs-TLR (Patrones moleculares asociados a patógenos-“Toll like receptors”) o mediante la señalización a través del inflamasoma.
La inhibición de la señalización microbiana frena los procesos de fibrosis tanto “in vivo” como “in vitro”. La “creeping fat” adyacente a los segmentos intestinales afectados por la EC está fuertemente asociada con las estenosis de la EC. La “creeping fat” se asocia a un engrosamiento del músculo liso intestinal provocando estenosis de la luz y síntomas obstructivos, mediante la liberación de mediadores proinflamatorios y ácidos grasos libres que actúan sobre las células musculares lisas y los fibroblastos de la musculatura intestinal propia11.
Tratamiento de la fibrosis
El tratamiento actual de la EII se basa en la supresión de la inflamación para evitar las lesiones intestinales, los síntomas secundarios a las mismas y la progresión de la enfermedad. Dado que la inflamación y la fibrosis están relacionadas, teóricamente los tratamientos usados en la EC que controlan la inflamación intestinal, como los anticuerpos antiTNFα (anti factor de necrosis tumoral alfa), deberían tratar también la fibrosis. En un modelo animal de EC, el tratamiento con anticuerpos antiTNFα vía intraperitoneal reduce la presencia no sólo de inflamación, sino también de fibrosis histológica y disminuye la expresión en el tejido cecal de RNA de factores profibróticos como procolágeno I y III, IGF y TGFβ112.
Sin embargo, en la vida real, lo que sí sabemos es que la presencia de fibrosis empeora la respuesta a los tratamientos antiTNF. Así, en el estudio LIRIC se comparó la evolución de pacientes con enfermedad ileal activa randomizados a recibir tratamiento antiTNF o resección ileal. Los pacientes que fracasaban al tratamiento antiTNF y que, posteriormente, eran intervenidos, mostraban un mayor engrosamiento de la muscularis mucosae y un aumento del depósito de proteínas de la MEC como la fibronectina, el colágeno III o la peptidasa pro-colágeno13.
Para analizar el efecto del tratamiento antiTNF directamente en pacientes con enfermedad estenosante, el estudio STRIDENT comparó la eficacia de una pauta intensiva con adalimumab vs la pauta standard en 77 pacientes con EC y estenosis ileal inflamatoria sintomática14. El tratamiento con adalimumab mejoró los síntomas obstructivos a los 12 meses en el 79% de los sujetos, necesitando cirugía de resección 4 pacientes en cada grupo. Sin embargo, cuando se analizó la mejoría o resolución radiológica de la estenosis, los resultados fueron más discretos (mejoría/ resolución por ecografía 39/29%; mejoría/resolución por resonancia 29/22%)15. Además, en el seguimiento a largo plazo de los pacientes, más allá de los 12 meses, 22 pacientes más necesitaron cirugía y 12 dilatación endoscópica. La presencia sumatoria de determinados factores en la resonancia magnética basal o RMI-score (dilatación preestenótica > 30mm, longitud de la estenosis >50 mm y grosor de la pared intestinal > 10 mm) condicionan un riesgo incremental de cirugía de resección16.
Autor/a: ArturVerkhovetskiy
Fuente: depositphotos.com
Los datos extraídos de bases de datos de ámbito nacional también sugieren que la tasa de cirugía de resección en pacientes con EC no se está reduciendo en la llamada “era del tratamiento biológico”. Un estudio realizado en Estados Unidos analizó las tasas de resección intestinal en 4.254.447 personas con EC hospitalizadas entre los años 1998 y 2020. Mientras que la tasa global de hospitalizaciones por cirugía se redujo considerablemente (del 12% al 6.9%), la tasa de hospitalizaciones por una cirugía por obstrucción intestinal aumentó en los 20 años del periodo del estudio (del 1.3% al 2%). Así, la proporción de cirugías de resección por síntomas obstructivos aumentó del 10.9% al 29%17.
Por todo ello, da la impresión que existe una desconexión entre la inflamación y la fibrosis. Mientras que la inflamación puede ser importante como desencadenante inicial de la fibrosis, dicha fibrosis, una vez establecida, puede progresar de manera autónoma autoperpetuándose, lo que puede tener implicaciones terapéuticas relevantes9.
Tratamientos antifibróticos
El futuro, por tanto, del tratamiento de la fibrosis intestinal podría estar en el uso de terapias directamente antifibróticas que restablecieran el equilibrio homeostático entre el depósito y la degradación de la matriz extracelular. Actualmente, no existen tratamientos antifibróticos aprobados para tratar la fibrosis intestinal, pero lo previsible es que este campo avance rápidamente, ya que existen muchas moléculas que están siendo testadas para tratar la fibrosis en otros órganos como el pulmón, la piel o el hígado18.
Por el momento, y a pesar de los avances, los ensayos con nuevos fármacos antifibróticos en el intestino se retrasan por dos razones principales. Por una parte, no se han podido traducir los resultados experimentales en nuevos fármacos y, por otro lado, no existe un consenso sobre las definiciones y criterios de evaluación de la fibrosis en los ensayos clínicos. La endoscopia detecta la estenosis, pero no es capaz de determinar el grado de fibrosis, puesto que no evalúa la transmuralidad.
Las técnicas radiológicas [Resonancia Magnética (RM), Tomografía Computerizada (TC) y ultrasonidos (US)] son las técnicas más utilizadas para detectar las estenosis y sus complicaciones, pero no determinan con exactitud el grado de fibrosis. Así, el gold standard para la detección de la fibrosis intestinal sigue siendo la histología11. Existen varias iniciativas para la evaluación y definición de las estenosis intestinales, fundamentalmente a cargo de sociedades médicas [American Gastroenterological Association (AGA), European Crohn’s and Colitis Organisation (ECCO), European Society of Gastrointestinal and Abdominal Radiology (ESGAR), Society of Abdominal Radiology (SAR) y Society for Pediatric Radiology (SPR)], o consensos y paneles de expertos (CONSTRICT: CrOhN’s disease antifibrotic STRICTure therapies o STAR: Stenosis Therapy and Anti-fibrotic Research Consortium)19.

Autor/a: Maximusdn
Fuente: depositphotos.com
El futuro pasará por la validación y desarrollo de nuevas técnicas radiológicas (elastografía por ecografía o resonancia, magnetization transfer RM, intravoxel incoherent motion imaging, radiotrazadores por PET) o el uso de herramientas de Inteligencia Artificial20. Existe algún estudio que evalúa también la utilidad de marcadores séricos de fibrosis, ya que esta sería una aproximación menos invasiva y potencialmente menos costosa de seguimiento a los individuos con EC. En un estudio con 111 pacientes con EC (62 con fenotipo estenosante y 49 con fenotipo inflamatorio ileal), determinados marcadores de la matriz extracelular (PRO-C6, PRO-C3, PRO-C5, C4M, y PRO-C4) son capaces de discriminar pacientes con EC estenosante o luminal21.
Los fármacos, en este momento, más prometedores en el tratamiento de la fibrosis intestinal son ontunisertib y los inhibidores de TL1A.
Ontunisertib (AGMB-129) es una molécula oral pequeña inhibidora de la quinasa ALK5/TGF-β, diseñada para actuar localmente en el tracto gastrointestinal. Ontunisertib bloquea potentemente TGFβ1 y tiene un efecto local y no sistémico porque se absorbe en el intestino actuando directamente en la pared intestinal con el paso de metabolitos inactivos al torrente circulatorio, tras su alta metabolización en el hígado22. Ontunisertib ha completado con éxito un estudio de fase 1 en un total de 82 individuos sanos que fueron aleatorizados para recibir dosis orales diarias únicas o múltiples de ontunisertib, o un placebo equivalente. Ontunisertib fue bien tolerado en todas las dosis evaluadas y no se detectaron mayores efectos adversos que en el grupo placebo. Además, el ensayo mostró una alta exposición local a ontunisertib en el íleon, pero ninguna exposición sistémica clínicamente relevante, lo que demuestra que el mecanismo de restricción gastrointestinal funcionó eficazmente en humanos23.
Actualmente se está llevando a cabo un estudio fase 2a (STENOVA) en pacientes con EC fibroestenosante24. Un análisis provisional realizado en los primeros 44 pacientes tras 12 semanas de tratamiento y comunicado en la DDW (Digestive Disease Week) 2025, demostró que ontunisertib es un fármaco seguro y bien tolerado con las dosis testadas, y sin observarse efectos adversos de interés. Los datos de farmacocinética indicaron una exposición sistémica muy baja a ontunisertib y una exposición alta a su metabolito principal inactivo. Estos resultados concuerdan con datos previos en sujetos sanos y respaldan el perfil de restricción intestinal de ontunisertib en pacientes con EC. Asimismo, se detectaron datos favorables al medicamento en la transcriptómica de la mucosa ileal, en los resultados endoscópicos y en los Patient Reported Outcomes (PROMs)25.
Por otra parte, TL1A, un miembro de la superfamilia del TNF, también se ha implicado en la patogénesis de la EII a través de un doble efecto proinflamatorio y profibrótico. Mediante la interacción con D3 (superfamilia de receptores de TNF de muerte celular) promueve la activación de las células T induciendo respuestas inflamatorias y estimulando la fibrosis. Diferentes evidencias sugieren la relación entre la sobreexpresión de TL1A y la fibrosis intestinal en pacientes con EC. En modelos experimentales, los ratones que expresan TL1A presentan fibrosis intestinal y colónica, mientras que los pacientes con EC y aumento de TL1A en el tejido tienen mayor fibrosis e inflamación ileocecal26. En la actualidad hay diferentes estudios en marcha con diferentes inhibidores de TL1A en pacientes con EII (Tabla 1).
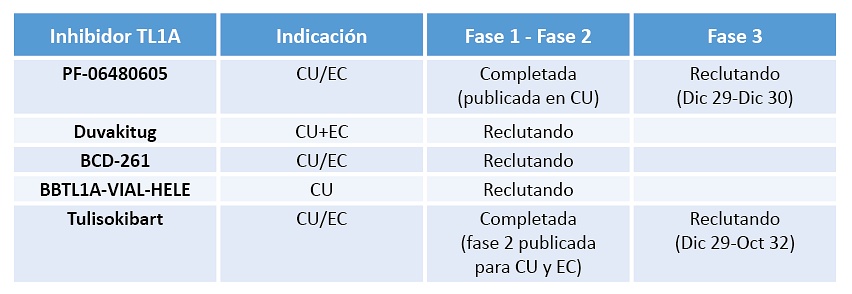
Tabla 1. Estudios en marcha con diferentes inhibidores de TL1A en pacientes con EII
CU: colitis ulcerosa; EC: enfermedad de Crohn
Elaboración propia a partir de https://clinicaltrials.gov/
En pacientes con EC, sólo se ha publicado el ensayo abierto fase 2 de inducción con tulisokibart (APOLLO), si bien el estudio no va dirigido específicamente a pacientes con estenosis intestinal, sino a pacientes con EC moderada-severamente activa27. El estudio de fase 3 está en este momento en fase de reclutamiento.
Conclusiones
La fibrosis y la estenosis intestinal secundaria siguen siendo un problema clínico relevante en el tratamiento de la EC al condicionar síntomas obstructivos en los pacientes, con la consiguiente disminución de su calidad de vida.
Actualmente, en los pacientes con EC tratamos principalmente la inflamación, no la fibrosis establecida, con lo que las tasas de cirugía no están reduciéndose significativamente a pesar del tratamiento biológico y avanzado.
Existe una necesidad de investigación en la detección rigurosa y temprana de la fibrosis, la definición de los objetivos de tratamiento y el desarrollo de terapias dirigidas.
Bibliografía
1. Solitano V, Dal Buono A, Gabbiadini R, Wozny M, Repici A, Spinelli A, et al. Fibro-stenosing Crohn’s disease: What is new and what is next? J Clin Med. 2023;12(9):3052. http://dx.doi.org/10.3390/jcm12093052
2. Torres J, Mehandru S, Colombel J-F, Peyrin-Biroulet L. Crohn’s disease. Lancet. 2017;389(10080):1741–55. http://dx.doi.org/10.1016/s0140-6736(16)31711-1
3. Cosnes J, Cattan S, Blain A, Beaugerie L, Carbonnel F, Parc R, et al. Long-term evolution of disease behavior of crohn’s disease. Inflamm Bowel Dis. 2002;8(4):244–50. http://dx.doi.org/10.1097/00054725-200207000-00002
4. Burisch J, Kiudelis G, Kupcinskas L, Kievit HAL, Andersen KW, Andersen V, et al. Natural disease course of Crohn’s disease during the first 5 years after diagnosis in a European population-based inception cohort: an Epi-IBD study. Gut. 2019;68(3):423–33. http://dx.doi.org/10.1136/gutjnl-2017-315568
5. Moran GW, Gordon M, Sinopoulou V, Radford SJ, Darie A-M, Vuyyuru SK, et al. British Society of Gastroenterology guidelines on inflammatory bowel disease in adults: 2025. Gut. 2025;74(Suppl 2):s1–101. http://dx.doi.org/10.1136/gutjnl-2024-334395
6. Lichtenstein GR, Loftus EV, Afzali A, Long MD, Barnes EL, Isaacs KL, et al. ACG clinical guideline: Management of crohn’s disease in adults. Am J Gastroenterol. 2025;120(6):1225–64. http://dx.doi.org/10.14309/ajg.0000000000003465
7. Giordano A, Pérez-Martínez I, Gisbert JP, Ricart E, Martín-Arranz MD, Mesonero F, et al. Ileal predominance in crohn’s disease is associated with increased intestinal surgery and biological therapy use, with lower treatment persistence. Am J Gastroenterol. 2025;120(1):194–203. http://dx.doi.org/10.14309/ajg.0000000000003207
8. Karsdal M, Cox TR, Parker AL, Willumsen N, Sand JMB, Jenkins G, et al. Advances in extracellular matrix-associated diagnostics and therapeutics. J Clin Med. 2025;14(6):1856. http://dx.doi.org/10.3390/jcm14061856
9. Rieder F, Mukherjee PK, Massey WJ, Wang Y, Fiocchi C. Fibrosis in IBD: from pathogenesis to therapeutic targets. Gut. 2024;73(5):854–66. http://dx.doi.org/10.1136/gutjnl-2023-329963
10. D’Alessio S, Ungaro F, Noviello D, Lovisa S, Peyrin-Biroulet L, Danese S. Revisiting fibrosis in inflammatory bowel disease: the gut thickens. Nat Rev Gastroenterol Hepatol. 2022;19(3):169–84
11. Rieder F, Nagy LE, Maher TM, Distler JHW, Kramann R, Hinz B, et al. Fibrosis: cross-organ biology and pathways to development of innovative drugs. Nat Rev Drug Discov. 2025;24(7):543–69.
12. Adler J, Rahal K, Swanson SD, Schmiedlin-Ren P, Rittershaus AC, Reingold LJ, et al. Anti-tumor necrosis factor α prevents bowel fibrosis assessed by messenger RNA, histology, and magnetization transfer MRI in rats with Crohn’s disease. Inflamm Bowel Dis. 2013;19(4):683–90.
13. De Bruyn JR, Becker MA, Steenkamer J, Wildenberg ME, Meijer SL, Buskens CJ, et al. Intestinal fibrosis is associated with lack of response to Infliximab therapy in Crohn’s disease. PLoS One. 2018;13(1):e0190999.
14. Schulberg JD, Wright EK, Holt BA, Hamilton AL, Sutherland TR, Ross AL, et al. Intensive drug therapy versus standard drug therapy for symptomatic intestinal Crohn’s disease strictures (STRIDENT): an open-label, single-centre, randomised controlled trial. Lancet Gastroenterol Hepatol. 2022;7(4):318–31.
15. Lovett GC, Schulberg JD, Hamilton AL, Wright EK, Sutherland TR, Ross AL, et al. Crohn’s disease stricture response to treatment assessed with magnetic resonance imaging and intestinal ultrasound: STRIDENT randomized trial. Inflamm Bowel Dis. 2025;31(10):2777–86.
16. Lovett GC, Schulberg JD, Hamilton AL, Wright EK, Holt BA, Sutherland TR, et al. Long-term results of drug treatment for Crohn’s disease strictures. Clin Gastroenterol Hepatol. 2025;S1542-3565(25)00805-5.
17. Fansiwala K, Spartz EJ, Roney AR, Kwaan MR, Sauk JS, Chen P-H, et al. Increasing rates of bowel resection surgery for stricturing Crohn’s disease in the biologic era. Inflamm Bowel Dis. 2025;31(4):935–43.
18. Lin S-N, Mao R, Qian C, Bettenworth D, Wang J, Li J, et al. Development of antifibrotic therapy for stricturing Crohn’s disease: lessons from randomized trials in other fibrotic diseases. Physiol Rev. 2022;102(2):605–52.
19. Dane B, Dillman JR, Fidler J, Anupindi SA, Fulmer CG, Gordon IO, et al. SAR consensus recommendations for defining small bowel Crohn disease strictures at CT and MR enterography. Radiology. 2025;316(1):e243123.
20. Rimola J, Beek KJ, Ordás I, Gecse KB, Cuatrecasas M, Stoker J. Contemporary imaging assessment of strictures and fibrosis in Crohn disease, with focus on quantitative biomarkers: From the AJR special series on imaging of fibrosis. AJR Am J Roentgenol. 2024;222(4):e2329693.
21. Poulsen A, Alexdóttir MS, Riis LB, Ovesen PD, Rasmussen J, Wewer MD, et al. Serum biomarkers of collagen remodeling are associated with intestinal fibrosis and differentiate stenotic from luminal Crohn’s disease patients: a pre- and post-resection longitudinal study. J Crohns Colitis [Internet]. 2025;19(6).
22. Ontunisertib. https://agomab.com/agmb-129/
23. Sáez-Borderías A, Van Kaem T, Alberti J, Stiers PJ, Sabadie C, Van Heeswijk R, et al. P0334 AGMB-129, an investigational ALK5 inhibitor for the treatment of Fibrostenosing Crohn’s Disease (FSCD), shows gastrointestinal (GI) restricted pharmacokinetics (PK) and a favorable safety profile in healthy subjects. J Crohns Colitis. 2025;19(Supplement_1):i796–i796.
24. STENOVA - A Study to Evaluate Safety, Tolerability, PK and PD of AGMB-129 in Patients with Fibrostenotic Crohn's Disease. https://clinicaltrials.gov/study/NCT05843578.
25. Rieder F, Panés J, Feagan BG, Heeren S, Kierkus J, Lu C, et al. 1118a: A Phase 2a, randomized, placebo-controlled, double-blind study to assess the safety, pharmacokinetics (PK) and pharmacodynamics (PD) of AGMB-129 in patients with fibrostenotic Crohn’s Disease: interim results from the STENOVA trial. Gastroenterology. 2025;169(1):S-2086.
26. Solitano V, Estevinho MM, Ungaro F, Magro F, Danese S, Jairath V. TL1A inhibition in inflammatory bowel disease: A pipeline review. BioDrugs. 2025;39(2):171–83.
27. Feagan BG, Sands BE, Siegel CA, Dubinsky MC, Longman RS, Sabino J, et al. Safety and efficacy of the anti-TL1A monoclonal antibody tulisokibart for Crohn’s disease: a phase 2a induction trial. Lancet Gastroenterol Hepatol. 2025;10(8):715–25.




