Redacción Farmacosalud.com
‘Actualmente la mayoría de los antimicrobianos no tradicionales, como la fagoterapia, la edición génica, las estrategias combinadas, la inmunoterapia o el trasplante fecal de microbiota, deben seguir los mismos procesos de desarrollo y autorización que los antibióticos convencionales. Sin embargo, los marcos regulatorios vigentes se diseñaron para fármacos y procedimientos convencionales, y no contemplan las particularidades biológicas, tecnológicas y de producción de los antimicrobianos no tradicionales que presentan mecanismos de acción radicalmente distintos’, sostiene el nuevo ‘Informe Anticipando’, centrado en esta ocasión en las ‘Estrategias Antimicrobianas en la Medicina del Futuro’.
‘Además, hay una falta de armonización en los requisitos para evaluar estas terapias y la generación de evidencia que permita comparar estos productos, entre ellos y con los fármacos tradicionales, lo que ralentiza su traslación a la práctica clínica’, se lee en el documento, que ha sido elaborado por el Observatorio de Tendencias en la Medicina del Futuro con el aval y el impulso de la Fundación Instituto Roche.

Fuente: Fundación Instituto Roche / BERBĒS
Sinergias fago-antibiótico
El uso inadecuado de antibióticos ha sido uno de los principales factores responsables del aumento de las resistencias antimicrobianas, fenómeno que ha comportado que se haya ido reduciendo progresivamente la eficacia de los tratamientos disponibles, hasta convertir el problema en una amenaza global para la salud pública. En este escenario, la Medicina Personalizada de Precisión abre nuevas oportunidades en el desarrollo de alternativas no-antibióticas frente a agentes infecciosos recalcitrantes, y de este modo avanzar hacia estrategias más eficaces y sostenibles como por ejemplo la fagoterapia, que está basada en el empleo de virus bacteriófagos o fagos para tratar infecciones resistentes a los antibióticos. En ese grupo terapéutico también figuran el trasplante fecal de microbiota, la edición génica, la inmunoterapia, las nuevas vacunas o las diferentes estrategias combinadas.
Una de las principales metodologías que se están desarrollando son las sinergias fago-antibiótico, que consisten en la aplicación de terapias combinadas entre bacteriófagos y antibióticos. Los antibióticos “pueden aumentar la replicación de fagos” y con ello mejorar “la eficacia antimicrobiana general y reducir las dosis necesarias y la probabilidad de aparición de nuevas resistencias”, argumenta la Dra. María Teresa Coque González, investigadora titular del Servicio de Microbiología del Hospital Universitario Ramón y Cajal y coordinadora del Área 2 de Investigación (Microbiología, Inmunidad e Infección) del Instituto de Investigación Biomédica Ramón y Cajal (IRYCIS) de Madrid.
Con respecto a la edición génica, la experta añade que los sistemas CRISPR-Cas permiten eliminar genes relacionados con resistencia o virulencia en bacterias. “Este conjunto de tecnologías utiliza enzimas guiadas para reconocer y cortar secuencias específicas de ADN o ARN en bacterias, re-sensibilizando cepas resistentes y modulando el microbioma con gran precisión”, explica la Dra. Coque, a su vez científica del Centro de Investigación Biomédica en Red de Enfermedades Infecciosas (CIBERINFEC).
‘Inequidad en el acceso a las estrategias antimicrobianas innovadoras’
Asimismo, la facultativa hace especial hincapié en el potencial de la inmunoterapia por ser un enfoque que trata de reforzar la capacidad natural del sistema inmune del paciente para controlar o eliminar infecciones. A juicio de Coque, la aplicación de estrategias como los anticuerpos monoclonales, los tratamientos híbridos que combinan anticuerpos y antibióticos, junto con las terapias CAR-T, “representan una nueva frontera en el tratamiento de infecciones al ofrecer alternativas y complementos a los antibióticos clásicos”, y contribuir así “a superar el desafío global que representa la resistencia antimicrobiana”.
La ‘inequidad en el acceso a las estrategias antimicrobianas innovadoras’ es otro de los temas abordados en el informe de la Fundación Instituto Roche: ‘la implementación de estrategias antimicrobianas innovadoras se enfrenta a una marcada inequidad en el acceso, tanto entre países como dentro de los propios sistemas sanitarios. Tecnologías avanzadas como la secuenciación masiva, el análisis metagenómico o las plataformas de diagnóstico molecular tienen costes aún elevados y requieren infraestructuras altamente especializadas. En consecuencia, su aplicación clínica se limita a contextos con mayores recursos, donde se prioriza su uso en función de la gravedad de la enfermedad o del riesgo individual del paciente. Esta desigualdad tecnológica y económica genera una brecha global que amenaza con perpetuar las diferencias en la capacidad de detección, respuesta y control de las enfermedades infecciosas’.
Más de 17 millones de muertes anuales en el mundo provocadas por patologías infecciosas
Las patologías infecciosas, causadas por organismos como bacterias, virus, hongos o parásitos, son responsables de más de 17 millones de muertes anuales en todo el mundo, según estimaciones de la Organización Mundial de la Salud (OMS). Esta clase de afecciones representan una amenaza global en continuo ascenso debido a los patógenos emergentes y reemergentes y el incremento de las resistencias antimicrobianas. En este marco, la Medicina Personalizada de Precisión propone un cambio de paradigma: evolucionar de un modelo centrado únicamente en el patógeno hacia una visión más amplia que integre datos detallados tanto del agente infeccioso como de las particularidades del paciente.
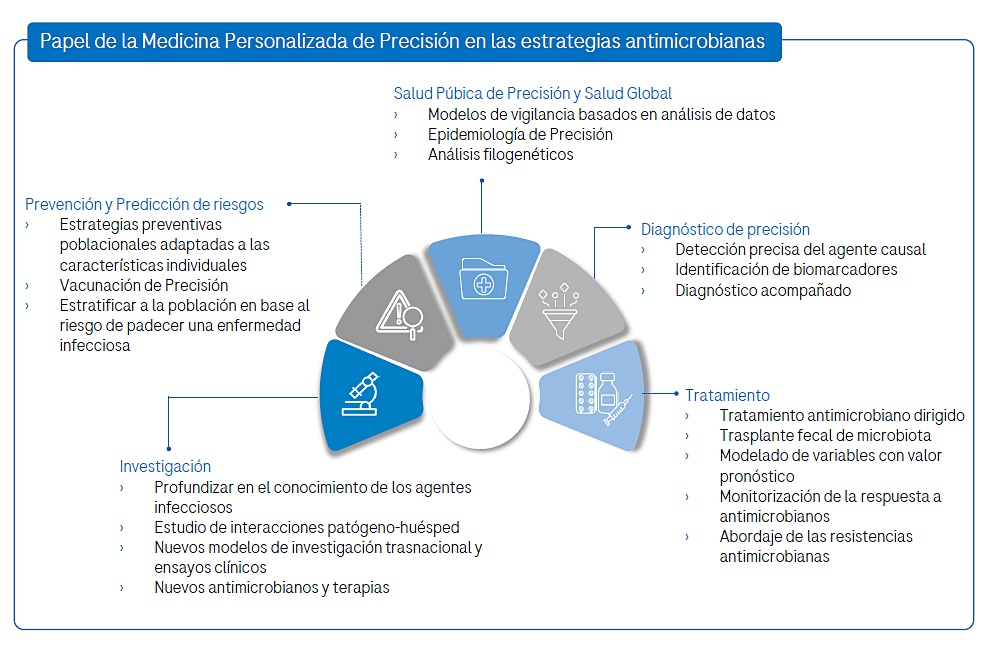
La Fundación Instituto Roche, en línea con los intereses y preocupaciones de la sociedad y los desafíos en el campo de las patologías infecciosas, ha impulsado la publicación del nuevo documento sobre Medicina Personalizada de Precisión y los avances que su práctica aporta a la hora de enfocarse en el abordaje de las enfermedades infecciosas. De este modo, el manual incide en la prevención y predicción de riesgos, el desarrollo de una Salud Pública de Precisión y de un Diagnóstico de Precisión, el impulso a estrategias terapéuticas antimicrobianas personalizadas y el abordaje innovador de las resistencias antimicrobianas.

Autor/a: Elnur_
Fuente: depositphotos.com
Tecnologías ómicas, ciencias de datos…
Las estrategias antimicrobianas, como es lógico, persiguen mejorar los resultados clínicos. En palabras de la coordinadora del informe, la Dra. Coque, la Medicina Personalizada de Precisión no sólo ayuda a identificar el agente causal de forma más rápida y precisa, sino que también permite predecir el riesgo individual de infección y adaptar las terapias a las particularidades genómicas de cada enfermo. De acuerdo con la especialista, los avances en tecnologías ómicas, ciencias de datos, Inteligencia Artificial (IA) y técnicas diagnósticas avanzadas “están haciendo posible caracterizar con mayor exactitud los mecanismos de virulencia y resistencia, y comprender mejor la interacción entre el patógeno y el huésped”.
En el marco de las más modernas investigaciones, la aplicación de la Medicina Personalizada de Precisión da la oportunidad de profundizar en el conocimiento, tanto a nivel molecular como sistémico, de los agentes infecciosos y entender mejor la interacción entre patógeno-huésped. Y es que comprender en detalle cómo actúan los microorganismos dentro del cuerpo sigue siendo un gran desafío científico. En esta línea -declara la Dra. Coque-, “la investigación avanza apoyándose en tecnologías de vanguardia como la bioimpresión, que permite crear organoides y plataformas 'organ-on-a-chip'. Estas herramientas reproducen con gran fidelidad los tejidos humanos permitiendo estudiar las infecciones y evaluar la eficacia de tratamientos de una forma mucho más eficaz y cercana a la realidad del paciente”.
Proyecto MePRAM
Otras líneas clave de trabajo se centran en el diseño de nuevos modelos de ensayos clínicos en el campo de las enfermedades infecciosas, como los estudios adaptativos, además del desarrollo de nuevos antimicrobianos para hacer frente a las bacterias multirresistentes. En este contexto, se están desarrollando programas y proyectos de investigación colaborativa que combinan datos clínicos y genómicos con modelos experimentales. El objetivo es generar antimicrobianos más eficaces y dirigidos, como prioridad para prevenir y mitigar la aparición y propagación de resistencias y garantizar opciones terapéuticas sostenibles. Entre estas iniciativas, se encuentra el Proyecto MePRAM (2023-2025).
MePRAM, que es la primera iniciativa española de medicina de precisión frente a la resistencia a antimicrobianos, se basa en el estudio de las resistencias a estos fármacos mediante un enfoque integral de Medicina Personalizada de Precisión. Tal y como precisa Coque, el programa incorpora tecnologías ómicas, algoritmos de IA y machine learning con el propósito de diseñar un abordaje integral que posibilite “personalizar la prevención, el diagnóstico y el tratamiento de pacientes afectados por microorganismos multirresistentes”.
En el ámbito de la prevención y predicción de riesgo, la Medicina Personalizada de Precisión está transformando la forma en la que se previenen y vigilan las infecciones. Concretamente, gracias al análisis de datos ómicos, es posible estratificar a la población en base al riesgo de padecer uno de estos problemas de salud. “Se ha visto que pacientes con alteraciones en la composición del microbioma intestinal, acompañadas de una respuesta inmune innata desregulada, tienen una predisposición de infección seis veces mayor, especialmente en pacientes ingresados en Unidades de Cuidados Intensivos (UCI)”, resalta.
Fuente: Fundación Instituto Roche / BERBĒS
Este hallazgo consolida el valor de la composición y diversidad del microbioma como biomarcador temprano de riesgo de infección, y lo consolida hasta tal punto que la nueva metodología tiene el potencial de poder “orientar intervenciones personalizadas para restaurar la salud intestinal” y, de este modo, optimizar la función inmune con el fin de prevenir infecciones mortales, guiando con todo ello “el diseño de estrategias preventivas personalizadas”.
Secuenciación en tiempo real
En el terreno de la Epidemiología de Precisión, la secuenciación genómica y el avance de la ciencia de datos, IA y machine learning, así como el interés de agencias y organismos internacionales en crear una estructura regional y global de vigilancia de amenazas sanitarias, ha revolucionado la respuesta frente a epidemias causadas tanto por virus (tipo coronavirus SARS-CoV), como por patógenos bacterianos. A diferencia de los métodos tradicionales, la secuenciación en tiempo real permite rastrear mutaciones como marcadores de transmisión y reconstruir la dinámica de los brotes. “Estos análisis han servido, por ejemplo, para enfocar intervenciones específicas contra el VIH o determinar la contribución de viajeros en la expansión del virus del Zika, así como para reconocer, investigar y reducir el impacto de brotes alimentarios y brotes hospitalarios, o la evolución dentro de hospedadores”, subraya la investigadora del CIBERINFEC.
El éxito del tratamiento depende de la rapidez con la que se identifique la causa de la infección. Frente a los métodos tradicionales, que pueden tardar días, la Medicina Personalizada de Precisión introduce herramientas revolucionarias, “como los paneles de diagnóstico rápido 'sindrómicos', que han supuesto un gran avance dado que permiten identificar, en una sola prueba, agentes microbianos causantes de cuadros clínicos similares; por ejemplo, determinar si el paciente sufre gripe, COVID-19 u otra infección, agilizando la decisión médica”, destaca Coque.
Asimismo -prosigue la científica del IRYCIS- las posibilidades potenciales que ofrece la metagenómica conducen hasta los “detectives genéticos”, que son capaces de leer todo el material genético de una muestra para identificar virus, bacterias u hongos, incluso aquellos desconocidos o difíciles de cultivar. La tecnología CRISPR, remarca la coordinadora del informe, “actúa como un 'buscador' molecular que detecta infecciones en menos de una hora, de forma barata y sin necesidad de grandes laboratorios”.
Por su parte, la directora gerente de la Fundación Instituto Roche, Consuelo Martín de Dios, apunta “que la Medicina Personalizada de Precisión está marcando un antes y un después en la lucha contra las resistencias antimicrobianas. Integrar la genómica del patógeno con el perfil del paciente permite avanzar hacia una estrategia diagnóstica y terapéutica mucho más inteligente, precisa y personalizada”.




