Redacción Farmacosalud.com
La Agencia del Medicamento de Estados Unidos (FDA) ha dado ya luz verde a dos anticuerpos monoclonales para la enfermedad de Alzheimer, lecanemab y donanemab, medicamentos que tienen la capacidad de retrasar la progresión de la demencia en las fases iniciales del Alzheimer. A la espera de saber qué decisión tomará la Agencia Europea del Medicamento (EMA) con respecto a esas dos terapias biológicas, como muy pronto -y si se cumple el más optimista de los escenarios-, lecanemab y donanemab (o al menos uno de los dos fármacos) podrían llegar a España a finales del próximo año, en 2025.
Ambos tratamientos están actualmente en proceso de evaluación por parte de la EMA. Sin la aprobación de la agencia reguladora europea, ninguno de los dos fármacos podrá ser comercializado en territorio español, ni por canales públicos ni por canales privados. En el caso concreto de lecanemab, estaba previsto que la EMA diera a conocer su resolución el pasado mes de marzo, pero el trámite se retrasó debido a unos cambios normativos. Se habló de un pronunciamiento en junio, pero al final tampoco se concretó nada en tal fecha y ahora habrá que ver si el organismo europeo toma una decisión antes de que acabe este mes de julio. Donanemab también está siendo evaluado por la EMA, si bien en este caso la documentación se ha presentado más tarde y por el momento no se ha establecido una fecha para el pertinente dictamen de resolución.

Dra. Raquel Sánchez del Valle
Fuente: SEN
“La AEMPS es bastante más lenta que otras agencias”
Si la decisión de la EMA fuera de aprobación, comenzaría la negociación con la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) para determinar en qué condiciones y a qué precios se comercializarían ambos tratamientos en España. “Por desgracia, últimamente estamos observando que el tiempo transcurrido desde que la EMA da su visto bueno a un fármaco hasta que los pacientes españoles pueden disponer de la novedad farmacológica es bastante largo; de hecho, es un período que se ha ido alargando a lo largo de los años”, afirma la Dra. Raquel Sánchez del Valle, coordinadora del Grupo de Estudio de Conducta y Demencias de la Sociedad Española de Neurología (SEN).
A lo que añade: “la AEMPS es bastante más lenta que otras agencias con respecto a los trámites de aprobación-financiación y establecimiento de precio de los medicamentos, con lo cual, salvo que den un trato preferente a lecanemab y donanemab por ser fármacos que tratan una ‘enfermedad huérfana’ -cabe recordar que para el Alzheimer hasta ahora no había ningún tratamiento modificador del curso evolutivo de la afección-, estaríamos hablando de más de un año hasta que ambos medicamentos o alguno de los dos lleguen a territorio español”. Y luego están los trámites que deben seguir las comunidades autónomas (CCAA) para regularizar la distribución y administración de un fármaco en su territorio… hay algunas CCAA que se caracterizan por la agilidad a la hora de cursar este tipo de procedimientos, pero hay otras que no actúan con tanta celeridad.
Entre un 24% y un 35% de retraso en la progresión de la enfermedad
Lecanemab y donanemab han revolucionado el abordaje terapéutico del Alzheimer. Y, si bien los datos disponibles sobre su eficacia proceden de ensayos clínicos y no todavía de la vida real, se ha demostrado que retrasan la progresión de la enfermedad en un 24% (lecanemab) o en un 35% (donanemab). Es decir, son terapias que no consiguen parar totalmente la evolución del Alzheimer, pero sí que enlentecen el empeoramiento de los pacientes en las fases iniciales de la patología, un efecto hasta ahora nunca logrado. Ambos tratamientos son muy similares y presentan únicamente una serie de pequeñas diferencias.
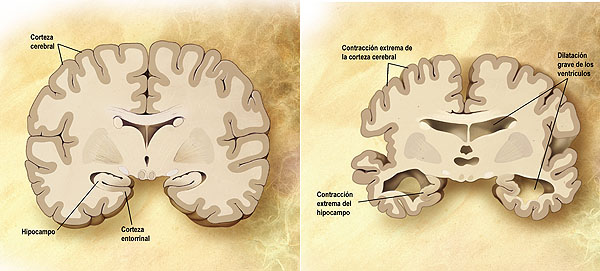
Comparación entre un cerebro normal y un cerebro afectado de Alzheimer. Esquema de un corte frontal de dos cerebros. El de la izquierda es un cerebro sano y el de la derecha uno que padece dicha enfermedad neurológica
Autor/a de la imagen: COMPARISONSLICE_HIGH.JPG: *derivative work: Garrondo (talk) SEVERESLICE_HIGH.JPG: ADEAR: "Alzheimer's Disease Education and Referral Center, a service of the National Institute on Aging." PRECLINICALSLICE_HIGH.JPG: ADEAR: "Alzheimer's Disease Education and Referral Center, a service of the National Institute on Aging." - COMPARISONSLICE_HIGH.JPG
Fuente: Wikipedia
El acúmulo en el cerebro de la proteína amiloide es una de las alteraciones principales de las fases iniciales del Alzheimer. No obstante, a medida que evoluciona la enfermedad se van sumando otras anomalías neuropatológicas. Desde finales de los años 90 del siglo pasado, los tratamientos experimentales han intentado eliminar la proteína amiloide “con la teoría de que, si se ‘limpiaba’ el cerebro de esta proteína, la neurodegeneración se enlentecería o se reduciría. Sin embargo, esos fármacos no fueron capaces de suprimir las placas amiloides”, expone la Dra. Sánchez del Valle.
En cambio, los medicamentos antiamiloides de segunda generación, lecanemab y donanemab, “han demostrado por primera vez que son capaces realmente de eliminar la placa amiloide -efecto observado por técnicas de neuroimagen- en un porcentaje muy importante de pacientes, al tiempo que se produce un enlentecimiento del empeoramiento clínico. No conseguimos parar el Alzheimer al 100%, pero los pacientes que reciben estos fármacos durante 18 meses empeoran entre un 24% y un 35% menos que los que no los reciben”, sostiene la especialista.
“Lo que nos interesaría saber es qué pasa con estos pacientes a los 5 años”
Ahora bien, lo que ocurre aquí es que los neurólogos sólo disponen de datos terapéuticos de 18 meses (los correspondientes a los ensayos clínicos), cuando “lo que nos interesaría saber es qué pasa con estos pacientes a los 5 años”, remarca la coordinadora del Grupo de Estudio de Conducta y Demencias de la SEN. Lo que los expertos calculan es que, a 5 años vista, cabría la posibilidad de que se magnifique el efecto de esos medicamentos porque previamente lecanemab y donanemab ya han conseguido eliminar la placa amiloide, lo que a su vez también podría ir asociado a un cambio del curso de la enfermedad. “Claro que eso, por ahora, es teoría, porque no tenemos esos datos a 5 años”, insiste la Dra. Sánchez del Valle.

Autor/a: stephen bowler
Fuente: Flickr / Creative Commons
En cuanto a la relevancia que puedan tener en la vida real los mencionados porcentajes de entre un 24% y un 35% de enlentecimiento del Alzheimer, la facultativa recuerda que, en función de cada caso y de la fase de la patología en que se encuentre cada enfermo, un retraso de tal calibre en la progresión del Alzheimer puede suponer la diferencia entre conducir o tener que dejar de conducir, o de ir solo al banco o bien necesitar ir acompañado, por poner dos ejemplos.
Riesgo de rotura de vasos sanguíneos cerebrales e inflamación del cerebro
Uno de los problemas vinculados a lecanemab y donanemab es la posible aparición de efectos secundarios graves, como son la rotura de vasos sanguíneos o la inflamación del cerebro. Ello se explica porque la proteína amiloide se acumula en el parénquima cerebral, pero también lo hace en la pared de los vasos sanguíneos del cerebro. Al suprimirse la placa amiloide, los vasos sanguíneos puede romperse y generar con ello microhemorragias (que es lo más habitual en estos casos). “Si son ‘micros’ se ven en la resonancia y no tendrían ninguna consecuencia clínica; no obstante, si se rompe un vaso de mayor calibre puede haber un sangrado mayor o hemorragia cerebral. Es poco frecuente, pero es un riesgo que pueden correr hasta un 3% de estos pacientes”, precisa.
Por otro lado, al eliminarse bruscamente la placa amiloide, el cerebro puede reaccionar porque, al final, la sustancia amiloide es una proteína que está ahí dentro y que forma parte de la composición cerebral, por lo que este órgano puede acabar provocando una inflamación a modo de respuesta.
Asimismo, hay que resaltar que la amenaza de aparición de estos graves eventos adversos obliga a realizar resonancias magnéticas seriadas para detectar esas posibles alteraciones y decidir, si fuera necesario, la interrupción de la terapia con el fin de evitar más complicaciones para el enfermo.
Autor/a de la imagen: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
Otros efectos secundarios derivados del uso de lecanemab y donanemab, en este caso frecuentes pero que preocupan menos a los neurólogos, son la sensación de escalofrío o de malestar que sufren los pacientes cuando les inyectan las dosis de los medicamentos, dado que ambos tratamientos se administran por vía intravenosa. Así, hay un porcentaje de enfermos que padecen ese tipo de molestias durante un par de horas.
Donanemab parece que elimina más rápidamente la placa amiloide que lecanemab, pero ello también comporta que “el porcentaje de eventos adversos graves con donanemab sea un poco mayor que con lecanemab. Es un efecto que parece estar relacionado con la velocidad e intensidad con que se suprime el acúmulo amiloide en el cerebro: si lo haces de una forma más rápida e intensa, el fármaco es más eficaz, pero también pueden aparecer más efectos secundarios”, subraya la Dra. Sánchez del Valle.
Fármacos con un coste de entre 26.000 y 32.000 dólares al año
Para la experta, lecanemab y donanemab “realmente cambian el paradigma del tratamiento de la enfermedad de Alzheimer, ya que empezamos a tratar las causas y no -como hacen los fármacos de que disponemos actualmente- los síntomas de la afección. Y, si bien lecanemab y donanemab no son tan eficaces, ni tan seguros ni tan fáciles de administrar (por ser intravenosos) como nos gustaría, son medicamentos que abren la puerta a la futura aparición de tratamientos más eficaces, más seguros y también más fáciles de aplicar (que no sean intravenosos). De hecho, ya se están estudiando preparaciones subcutáneas… Y, por otro lado, si son medicamentos más seguros, habrá menos necesidad de monitorización, a diferencia de lo que ocurre con los dos fármacos antiamiloides de segunda generación”.
Finalmente, Sánchez del Valle no quiere obviar el siempre espinoso tema del precio de los tratamientos: “lecanemab y donanemab tienen un coste no despreciable, de entre 26.000 y 32.000 dólares al año… por lo tanto, son costes elevados. Ahora bien, la FDA considera que el riesgo-beneficio presenta un balance positivo en ambos casos, por lo que creo que son unas terapias que abrirán la puerta a otras moléculas más eficaces, más seguras, más fáciles de aplicar y, probablemente, más baratas. Estoy convencida de que será así”.




