Redacción Farmacosalud.com
La apuesta de la Unidad Intercentros de Anatomía Patológica de la provincia de Granada por la digitalización y la patología computacional ha dado uno de sus primeros frutos: la validación e integración en el flujo de trabajo de un algoritmo, primero de su tipo en España, para analizar las muestras de biopsias con el fin de detectar la presencia de la bacteria Helicobacter pylori, causa frecuente de úlceras pépticas y un importante factor de riesgo en determinados tipos de cáncer de estómago. Este algoritmo pretende ser una herramienta de ayuda al patólogo a la hora de realizar un diagnóstico de mayor calidad y precisión, con consecuencias directas en la reducción de los tiempos de diagnóstico y en una mejor atención a los pacientes afectados por H. pylori.
“Decidimos desarrollar un algoritmo para contribuir a un diagnóstico más eficiente, preciso y estandarizado de la infección por Helicobacter pylori, un problema clínico recurrente en los servicios de Anatomía Patológica”, declaró el Dr. Alvaro Berbís, gerente de Cells IA, la empresa que ha desarrollado el algoritmo. “Gracias a herramientas como el Big Data, la Inteligencia Artificial (IA) o el Machine Learning podemos establecer nuevos parámetros de análisis del tejido que, de otra manera, podrían pasar desapercibidos para el patólogo”, explica el Dr. Raimundo García del Moral, director de la Unidad de Anatomía Patológica de Granada.
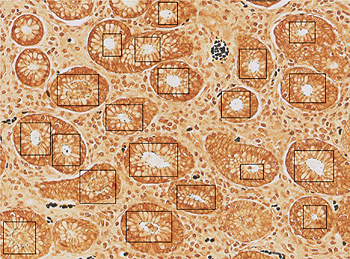
Detección automática de infección por Helicobacter pylori en una sección de biopsia gástrica procesada con tinción de Warthin-Starry
Fuente: Royal Philips / Cells IA / Europa Press Comunicación
Modelos matemáticos capaces de hacer una predicción sobre la imagen generada de la muestra
La validación e implementación de este algoritmo ha sido posible gracias a la participación de empresas como Philips Ibérica, Vitro y Cells IA, que han colaborado con el Servicio de Anatomía Patológica de Granada en un proceso integral de digitalización que arrancó hace ya varios años, pionero en España y que permite el análisis 100% digital de muestras de tejido para una población de más de un millón de habitantes.
“Cuando entra una muestra de un paciente en nuestro servicio, arranca el proceso de patología computacional que recoge la información clínica del paciente y que, mediante modelos matemáticos, es capaz de hacer una predicción sobre la imagen generada de la muestra”, apunta el Dr. José Aneiros, responsable de Patología Computacional en el Servicio de Anatomía Patológica de Granada. Las ventajas de la digitalización de la anatomía patológica son evidentes para García del Moral: “Evita tareas rutinarias, objetiva los datos de las muestras, reduce los tiempos de realización de los análisis y libera a los patólogos para hacer tareas más relevantes y de mayor valor añadido”.
La digitalización de las muestras se realiza mediante escáneres ultrarrápidos, cuyo uso se acompaña de un visor web para el examen de las biopsias. Para conseguir la excelencia, este proceso está integrado en el Sistema de Información de Laboratorio (SIL), que garantiza que los patólogos pueden acceder a todas las muestras en tiempo real incluso desde sus hogares.
Dos y tres terabytes de datos diarios con las muestras escaneadas
“Nuestro servicio genera entre dos y tres terabytes de datos diarios con las muestras escaneadas, una gran cantidad de datos esperando a ser analizados, y ahí es donde entra la patología computacional, el análisis a gran escala de esos datos mediante herramientas de Big Data e IA”, precisa García del Moral, quien pronostica que en un futuro no tan lejano la patología computacional no solo será un apoyo al patólogo, “sino que incluso podrá hacer sus propios diagnósticos”.
Este experto destaca que, precisamente, una de las áreas terapéuticas que más se benefician de la patología computacional es la oncología. “El cáncer es la patología que requiere más parámetros cuantificables hoy en día, como el tamaño del tumor, el volumen de células tumorales, el tamaño del citoplasma y del núcleo de las células, el número de mitosis… Y todo esto un ordenador lo hace miles de veces más rápido que el ser humano”. Según El Dr. Aneiros, las ventajas de la patología computacional son claras: “La incorporación de algoritmos en el diagnóstico de patologías concretas hace incrementar la eficiencia del patólogo, ya que le permite procesar un mayor número de muestras e incrementa la seguridad en el diagnóstico”.

Fuente: Archivo
“En muchas ocasiones un porcentaje específico de un determinado marcador tumoral condiciona el poder tratarlo de una manera o de otra y, por tanto, la incorporación de algoritmos que cuantifiquen de forma más exacta esos marcadores hace que el diagnóstico sea mucho más preciso y esa enfermedad sea tratada de la mejor manera posible”, continúa el responsable de patología computacional.
Por último, García del Moral comenta que la patología computacional proporciona una cantidad enorme de parámetros de diagnóstico que, de otra forma, sería imposible obtener. Esto es especialmente útil para oncólogos y cirujanos que tienen que planificar un tratamiento. “Y en el futuro les vamos a aportar la interpretación de nuevos parámetros que podrán repercutir en la eficacia de los tratamientos y en la supervivencia de los pacientes”, concluye.




