Redacción Farmacosalud.com
Un estudio internacional revela que las poblaciones de ancestría americana y europea tienen un mayor riesgo de sufrir toxicidad asociada al consumo de fármacos, mientras que los individuos con ascendencia del este de Asia, y en menor medida, de las poblaciones de Oceanía, muestran un riesgo más bajo. Con independencia de que unos colectivos humanos estén más o menos expuestos a tales eventos adversos, el líder la nueva investigación, el Dr. Òscar Lao, considera que los resultados obtenidos evidencian que los ensayos clínicos deberían tener en cuenta los condicionantes genéticos a la hora de evaluar los medicamentos en fase de experimentación: “nuestros resultados sugieren que, a la hora de testar nuevos fármacos, se debería tener la mejor representación posible de la diversidad genética presente en las poblaciones donde luego se van a usar tales moléculas”.

Dr. Òscar Lao
Fuente: IBE
“Dado que la mayoría de medicamentos son de uso universal, sería una buena política el hecho de poder realizar los ensayos en diferentes poblaciones y continentes. Evidentemente, eso puede encarecer el desarrollo de la terapia”, advierte Lao desde www.farmacosalud.com.
No obstante, el científico puntualiza a renglón seguido que la Inteligencia Artificial (IA) -usada ya para la elaboración del mencionado estudio- podría reducir el coste de los futuribles e innovadores ensayos farmacogenéticos. “Dado que la IA puede predecir efectos adversos durante el desarrollo del tratamiento, podría abaratar sustancialmente todo el proceso al lograr disminuir la cantidad de tiempo necesaria para desarrollar nuevos medicamentos y maximizar la especificidad de los mismos a la diana terapéutica”, argumenta Lao, a su vez investigador principal del Grupo de Algoritmos para la Genómica de Poblaciones del Instituto de Biología Evolutiva (IBE).
Las reacciones adversas a los medicamentos, una de las principales causas de mortalidad
A pesar de que los sapiens compartimos más del 99,9% de nuestro genoma, cada individuo es único. Nuestras diferencias genéticas se reflejan de muchas formas: desde el color de los ojos o el cabello hasta la predisposición a padecer enfermedades o cómo reaccionamos a los fármacos que consumimos. Por ejemplo, personas con deficiencia del gen G6PD pueden sufrir fatiga o dolores abdominales, entre otros eventos, si toman aspirina, informan desde el IBE. De hecho, las reacciones adversas a los medicamentos (RAM) son una de las principales causas de afección y mortalidad en todo el mundo, situándose entre la cuarta y sexta causa de muerte más comunes. Y, si bien la genética puede influir en la seguridad y eficacia de los tratamientos farmacológicos, en muchas ocasiones esta información no se tiene en cuenta a la hora de prescribir medicamentos.
Pero ahora, el nuevo estudio internacional -liderado por el IBE, un centro mixto del Consejo Superior de Investigaciones Científicas (CSIC) y la Universidad Pompeu Fabra (UPF, en Barcelona)- ha puesto de manifiesto datos clave sobre la influencia de la herencia genética en la toxicidad de los tratamientos. Mediante el uso de la IA, como decíamos, el equipo ha analizado 1.136 variantes genéticas ligadas a la toxicidad de algunos grupos de fármacos en 3.714 individuos de todo el mundo.
Para llevar a cabo este análisis, el grupo de científicos ha estudiado los genes con funciones clave para la absorción y transporte de los medicamentos en el cuerpo. En particular, ha utilizado herramientas ultraavanzadas que se sirven de algoritmos de aprendizaje automático para llevar a cabo un examen genómico a gran escala. Mediante técnicas de ‘text mining’ o minería de textos, el equipo de investigación ha agrupado estas variantes y las ha relacionado con la ascendencia genética de regiones geográficas en todo el mundo, lo que ha permitido desarrollar una herramienta que desvela el papel clave de la genética poblacional en el efecto de los fármacos.
Europeos: más probabilidad de toxicidad por uso de terapias cardiovasculares y antimicrobianas
El equipo analizó la frecuencia de alelos (formas alternativas de un gen) implicados en la aparición de efectos secundarios en seis grupos de medicamentos distintos. Los resultados indican que las poblaciones americanas y europeas tienen mayor riesgo de toxicidad con los fármacos cardiovasculares y antimicrobianos. Las poblaciones americanas también muestran mayor peligro con respecto a los antidepresivos y analgésicos, mientras que para las europeas son más tóxicos los tratamientos inmunosupresores y los anticancerosos. Por otra parte, los colectivos asiáticos y de Oceanía mostraron un menor riesgo en todos los grupos terapéuticos, a excepción de algunos individuos de Asia central, que presentan un riesgo elevado para los analgésicos.
Cabe precisar que en este trabajo no se ha abordado el grado de severidad de los efectos secundarios (leves, moderados o graves). “Manualmente -precisa el Dr. Lao-, categorizamos los fármacos según el sistema/fenotipo al que se referían (por ejemplo, antidepresivos, analgésicos, etc). Idealmente, se deberían haber estratificado también por la gravedad de los efectos secundarios. Ahora bien, la información sobre este tipo de eventos no siempre está disponible en esta base de datos, o bien es críptica, por lo que decidimos no intentar hacer ningún tipo de clasificación bajo ese criterio”.
“Muchos de los medicamentos del estudio se han probado en individuos de ancestría europea antes de ser comercializados. Si hubiera un sesgo debido a esta estrategia, esperaríamos que los fármacos fueran más seguros en estas poblaciones que en otras, pero lo que vemos es lo contrario, por lo que podemos excluir un sesgo médico como motivo de esos resultados. Todo apunta a que las distintas frecuencias entre poblaciones pueden tener una explicación evolutiva”, sostiene Lao a través de un comunicado.
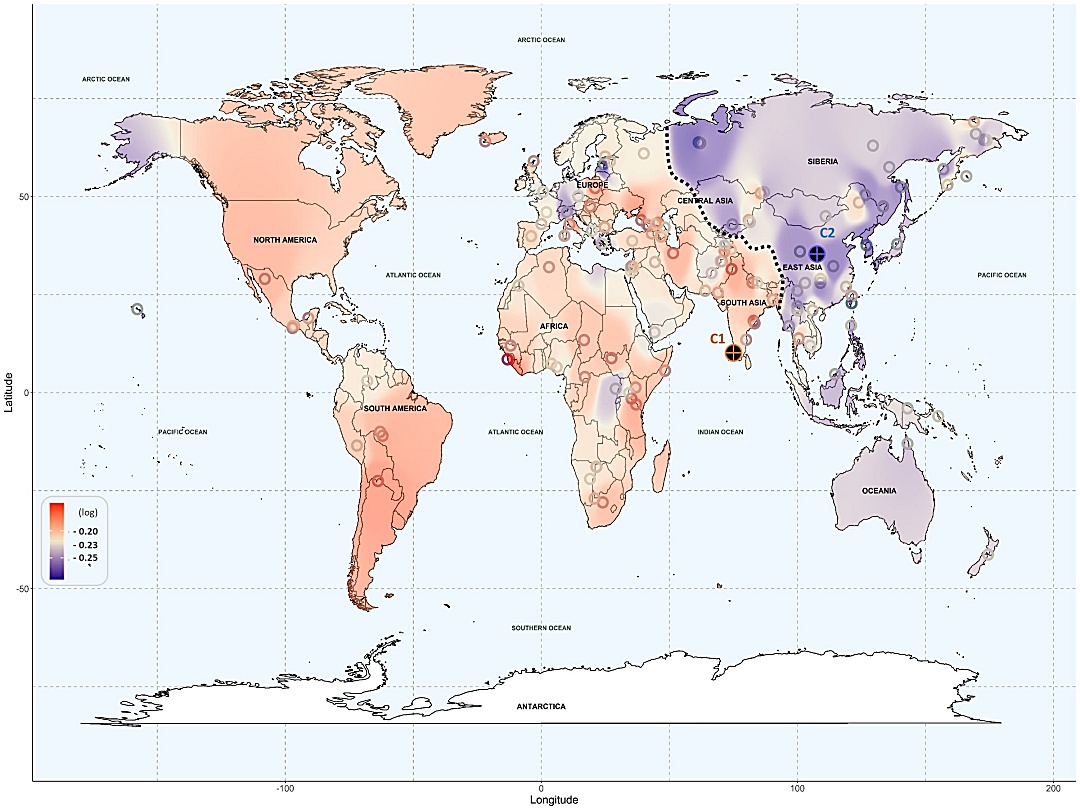
Un mapa global predictivo de la diversidad genética revela distintos patrones geográficos relacionados con los efectos adversos de los medicamentos. Cada región de muestreo se ha representado en el mapa mediante puntos de datos circulares, y los colores (azul oscuro o rojo claro) indican la estimación del riesgo dentro de las respectivas regiones. En rojo se muestran las regiones con mayor riesgo y en azul las regiones con menor riesgo
Autor/a de la imagen: Kariofyllis Karamperis y Òscar Lao
Difusión: IBE
Así pues, la nueva investigación destaca el potencial de la información genética de individuos y colectivos demográficos como un recurso clave en el diseño de estrategias de medicina personalizada. Dicho de otro modo, que el estudio señala a la farmacogenética como herramienta clave para el abordaje médico individualizado o realizado a medida, es decir, planificado y aplicado en función de cada paciente.
“El hecho de que observemos diferencias entre poblaciones por estas variantes sugiere que sería interesante incluir la ancestría genética del individuo a la hora de realizar tratamientos más personalizados”, subraya el experto. En el futuro, podrían desarrollarse unas sencillas pruebas genéticas que, combinadas con la IA, permitieran identificar a los pacientes vulnerables a efectos secundarios graves de algunos medicamentos. En última instancia, podría plantearse incluir un perfil farmacogenético y de ancestría de cada sujeto como parte de su historial clínico.
Los ensayos farmacogenéticos no fomentarían lo que podría denominarse egoísmo zonal
Trabajos anteriores -basados en el estudio de la metabolización de los medicamentos en las personas- ya sugerían la posibilidad de tener en cuenta la singularidad genética a la hora de fomentar una medicina más individualizada. Ahora bien, uno se pregunta si con estudios como el liderado por el IBE se corre el peligro de que, de ahora en adelante, la investigación de los laboratorios se centre sólo en los mercados más -por decirlo de algún modo-rentables o más afines por razones de proximidad sociocultural (por ejemplo, un laboratorio europeo centrándose básicamente en rebajar los eventos adversos asociados a los tratamientos más tóxicos para los europeos)… “más bien, creo que ocurriría lo contrario -matiza Lao-. Los laboratorios buscan vender sus productos al mayor número posible de personas”.
“Si un medicamento funciona bien para algunos, pero mal para otros debido a que durante su desarrollo no se consideraron diferencias genéticas en ciertos grupos de individuos, es algo que representa un riesgo para los laboratorios; esta situación podría exponerlos a problemas legales. Yo lo que creo es que este tipo de estudios pueden servir para que se ponga mayor esfuerzo en incluir a la mayor cantidad de etnias posible en los ensayos sobre nuevos fármacos”, concluye el especialista del IBE.
Artículo de referencia:
Karamperis, Kariofyllis & Katz, Sonja & Melograna, Federico & Ganau, Francesc & Steen, Kristel & Patrinos, George & Lao, Oscar. (2024). Genetic ancestry in Population Pharmacogenomics unravels distinct geographical patterns related to drug toxicity. iScience. 27. doi: 10.1016/j.isci.2024.110916




