Redacción Farmacosalud.com
Alexion Pharma Spain, el grupo de enfermedades raras de la compañía AstraZeneca, anuncia que el Ministerio de Sanidad, Consumo y Bienestar Social de España ha incluido en el Sistema Nacional de Salud (SNS) ravulizumab (Ultomiris®), un inhibidor de C5 de acción prolongada para el tratamiento de la Hemoglobinuria Paroxística Nocturna (HPN) y el Síndrome Hemolítico Urémico atípico (SHUa). El nuevo fármaco destaca por su mayor comodidad de uso, ya que requiere 7 infusiones al año frente a las 26 anuales de la actual opción terapéutica para ambas afecciones, eculizumab. Ravulizumab también tiene potencial para reducir la mortalidad en HPN y suspender el tratamiento en determinados pacientes de SHUa.

(de izq. a dcha): Dr. Manuel Praga, Carlos Macedo, director Médico de Alexion para España y Portugal, y la Dra. Mónica Ballesteros
Fuente: Alexion / AstraZeneca / Edelman
Ravulizumab está indicado para adultos y niños con HPN que presentan hemólisis con síntomas clínicos indicativos de alta actividad de la enfermedad, y también para adultos clínicamente estables tras haber sido tratados con eculizumab durante al menos los últimos seis meses1. Ravulizumab, asimismo, está disponible para el tratamiento de adultos y niños con 10 kg o más con SHUa que no hayan recibido tratamiento con inhibidores del complemento o que hayan recibido eculizumab durante al menos tres meses y tengan evidencia de respuesta a eculizumab1. Ravulizumab se administra cada ocho semanas para pacientes con peso ≥ 20 kg, o cada cuatro semanas para niños de entre 10 kg y < 20 kg.
Este medicamento actúa inhibiendo la proteína C5 de la cascada terminal del denominado ‘sistema del complemento’, una parte del complejo inmunológico, o lo que es lo mismo, las defensas del organismo. Cuando la cascada del complemento se activa de forma incontrolada ataca a sus propias células sanas, siendo la causa principal de estas dos enfermedades raras, la HPN y el SHUa.
HPN
La HPN es un trastorno sanguíneo crónico, progresivo y potencialmente mortal. Se caracteriza por la destrucción de los glóbulos rojos (hemólisis intravascular) y la activación de los glóbulos blancos y las plaquetas, lo que puede dar lugar a coágulos sanguíneos (trombosis). Convivir con HPN puede ser debilitante, y los síntomas pueden incluir fatiga, dificultad para tragar (disfagia), problemas para respirar (disnea), dolor abdominal, disfunción eréctil y orina de color oscuro (hemoglobinuria)2-4.
“El 93% de los pacientes prefirieron ravulizumab al actual inhibidor del complemento”
De acuerdo con la Dra. Mónica Ballesteros, especialista en Hematología y Hematoterapia, médica adjunta del Hospital Gregorio Marañón (Madrid) y responsable de enfermos HPN en dicho centro hospitalario, ravulizumab logra reducir “claramente” la mortalidad en esta patología, mostrando por ahora resultados “muy similares” a los obtenidos en las personas que reciben eculizumab. Además, ravulizumab proporciona una inhibición completa del complemento desde la primera infusión tanto en adultos como en niños5. “Reducir a un máximo de 7 infusiones de mantenimiento al año para pacientes con un peso corporal ≥ 20 kg permite minimizar el impacto de la patología en la vida de los pacientes. En este sentido, según un estudio realizado, el 93% de los pacientes prefirieron ravulizumab al actual inhibidor del complemento”, manifiesta la Dra. Ballesteros.
SHUa
El SHUa es una afección rara que puede deteriorar progresivamente órganos vitales como los riñones, debido al daño en las paredes de los vasos sanguíneos y a la formación de trombos. El SHUa puede afectar a adultos y niños. Se presenta en estado crítico en muchos sujetos, quienes, a menudo, requieren cuidados de apoyo, incluyendo la diálisis, en una unidad de cuidados intensivos. El 56% de los adultos y el 29% de los niños acaban desarrollando una enfermedad renal terminal o fallecen en el plazo de un año tras el diagnóstico, recibiendo únicamente cuidados paliativos6. Un diagnóstico correcto y precoz, además del inicio temprano del tratamiento, son fundamentales para mejorar el pronóstico de los enfermos.

Fuente: Archivo
"Los resultados de los ensayos clínicos de fase III demuestran que ravulizumab produce una respuesta completa de la microangiopatía trombótica (MAT), una mejora de la función renal y la suspensión de la diálisis en la mayoría de los pacientes tratados, tanto en adultos como en niños”, refiere el Dr. Manuel Praga, nefrólogo del Hospital Universitario 12 de Octubre y catedrático de Medicina de la Universidad Complutense (Madrid).
Posible suspensión del tratamiento, sobre todo si no hay mutaciones en genes del complemento
Por otro lado, la eficacia de la nueva terapia puede dar lugar a la suspensión del tratamiento en determinados pacientes de SHUa. En el ámbito del SHUa primario, el riesgo de recaídas va a depender sobre todo de la presencia de mutaciones en genes del complemento. En pacientes con mutaciones genéticas el riesgo de recaída es más alto, de ahí que en individuos que no las presenten -aproximadamente un 40% de los enfermos- se pueda suspender la administración de este fármaco "después de un período de tiempo de tratamiento y una vez que el paciente esté estable. Eso se ha estudiado con eculizumab y lógicamente será aplicable también a ravulizumab”, arguye el Dr. Praga.
De todos modos, “hay que individualizar cada caso” a partir del tipo de mutación para poder valorar el riesgo de recaída, aduce Praga. “Pero bueno -agrega-, en principio con ravulizumab se podría también suspender” el tratamiento, especialmente en los casos en que no haya mutaciones genéticas. Sea como fuere, en todos los enfermos en los que se interrumpa la administración de ravulizumab, y al igual que se ha venido haciendo con eculizumab, “hay que estar encima, tener cuidado sobre todo al principio, por la posible reaparición de la enfermedad. Y si reapareciera, hay estudios que muestran que la rápida reinstauración del tratamiento permite controlar la enfermedad”, comenta el nefrólogo.
"Estamos encantados de anunciar la disponibilidad de ravulizumab en España. En Alexion, nuestro objetivo es seguir mejorando la vida de las personas y familias afectadas por el SHUa y la HPN. Este tratamiento ofrece la comodidad de una dosificación menos frecuente sin comprometer la eficacia ni la seguridad. Esto les proporciona una mayor flexibilidad para sus vidas, al mismo tiempo que reduce la carga del sistema sanitario", sostiene por su parte Carlos Macedo, director médico de Alexion para España y Portugal.
Las aprobaciones de la Comisión Europea para el nuevo medicamento se basan en los datos de cuatro ensayos clínicos: dos ensayos fase III para HPN, que representan el mayor programa de ensayos clínicos en esta patología1,7,8, y dos estudios globales, abiertos, de un solo brazo, de ravulizumab; uno en adultos y otro en niños con SHUa8-11.
HPN: 30 años, la edad media de diagnóstico
La HPN es un trastorno sanguíneo crónico, progresivo y potencialmente mortal. Se caracteriza por la destrucción de glóbulos rojos (hemólisis intravascular) y la activación de los glóbulos blancos y las plaquetas, lo que puede dar lugar a coágulos de sangre (trombosis).
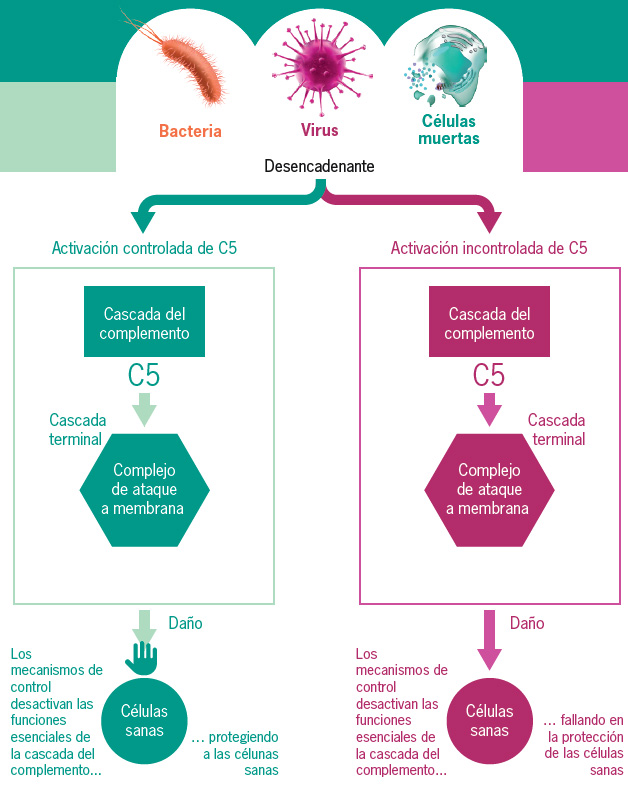
El sistema del complemento forma parte del sistema inmune y es esencial para la defensa del organismo contra las infecciones
En verde: cuando el sistema del complemento funciona correctamente
En fucsia: cuando el sistema del complemento se desregula
Adaptado de las referencias 17-19
Difusión: Alexion / AstraZeneca / Edelman
La HPN está causada por una mutación genética adquirida (no heredada) que puede producirse después del nacimiento y que da lugar a la producción de células sanguíneas anormales sin proteínas protectoras de la superficie. La ausencia de estas proteínas protectoras permite que el sistema del complemento, que forma parte del sistema inmunológico, esencial para la defensa del organismo contra las infecciones, ‘ataque’ y destruya o active estas células sanguíneas anormales2,12,13. Puede presentarse en niños y adultos de cualquier edad, siendo los 30 años la edad media de diagnóstico. Esta patología afecta tanto a hombres como a mujeres y a personas de todos los grupos raciales y étnicos14. Convivir con HPN puede ser debilitante y los síntomas pueden incluir fatiga, dificultad para tragar (disfagia), problemas para respirar (disnea), dolor abdominal, disfunción eréctil, y orina de color oscuro (hemoglobinuria y anemia)2-4.
SHUa: las pruebas disponibles ayudan a distinguirlo de otras enfermedades hemolíticas
El SHUa es un trastorno potencialmente letal que puede dañar progresivamente órganos vitales, como los riñones, a causa de los daños en las paredes de los vasos sanguíneos y la formación de coágulos de sangre. El SHUa se produce cuando el sistema del complemento, una parte del sistema inmune del organismo, se activa de forma incontrolada y ataca a sus propias células sanas15. El SHUa puede provocar un fallo repentino de los órganos o una disfunción progresiva a lo largo del tiempo, lo que puede derivar en la necesidad de un trasplante renal. En algunos casos, puede provocar la muerte.
El SHUa afecta tanto a adultos como a niños. Se presenta en estado crítico en muchas personas que, a menudo, requieren cuidados paliativos, como diálisis y trasplante renal, en una unidad de cuidados intensivos16. En muchos casos, el desarrollo de la afección impacta negativamente en la vida de los pacientes, por lo que un diagnóstico precoz y correcto, además del inicio temprano del tratamiento, es fundamental para mejorar los resultados terapéuticos. Las pruebas disponibles pueden ayudar a distinguir el SHUa de otras enfermedades hemolíticas con síntomas similares15.
Ravulizumab es un inhibidor de C5 de acción prolongada que proporciona una inhibición inmediata, completa y sostenida del complemento. El medicamento actúa inhibiendo la proteína C5 de la cascada terminal de esta parte del sistema inmune del organismo. Cuando se activa de forma incontrolada, la cascada del complemento responde en exceso, lo que lleva al organismo a atacar a sus propias células sanas.
Ultomiris se administra por vía intravenosa cada ocho semanas en adultos, tras una dosis inicial de carga. Está aprobado en EE.UU. para el tratamiento de determinados adultos con miastenia gravis generalizada (MGg). También está aprobado en Estados Unidos, la UE y Japón para el tratamiento de adultos y niños con HPN. Además, ravulizumab tiene luz verde en EE.UU., la UE y Japón para adultos y niños con SHUa para inhibir la microangiopatía trombótica mediada por el complemento. Como parte de un amplio programa de desarrollo, ravulizumab está siendo evaluado para el tratamiento de otras indicaciones hematológicas y neurológicas.
Referencias
1. Ficha técnica Ultomiris. Alexion Europe SAS. Abril de 2022.
2. Brodsky RA. Paroxysmal nocturnal hemoglobinuria. Blood. 2014;124(18):2804-2811.
3. Hillmen, P., et al. (2007). Effect of the complement inhibitor eculizumab on thromboembolism on patients with paroxysmal nocturnal hemoglobinuria. Blood, 110(12), 4123-4128.
4. Kulasekararaj AG, Hill A, Rottinghaus ST, Langemeijer S, Wells R, Gonzalez-Fernandez FA, et al. Ravulizumab (ALXN1210) vs eculizumab in C5-inhibitor-experienced adult patients with PNH: the 302 study. Blood 2019;133(6):540–9.
5. Peffault de Latour R, Brodsky R, Ortiz S, Risitano A, Jang J, Hillmen P et al. Pharmacokinetic and pharmacodynamic effects of ravulizumab and eculizumab on complement component 5 in adults with paroxysmal nocturnal haemoglobinuria: results of two phase 3 randomised, multicentre studies. British Journal of Haematology. 2020;191(3):476-485.
6. Fremeaux -Bacchi, V, et al. Genetics and outcomes of atypical HUS in Children and Adults: A Nationwide French Series Comparing Children and Adults. Clin J Am Soc Nephrol. April 2013, 8 (4) 554-562;
7. Lee JW, Jang JH, Kim JS, Yoon S-S, Lee J-H, Kim Y-K, et al. Clinical signs and symptoms associated with increased risk for thrombosis in patients with paroxysmal nocturnal hemoglobinuria from a Korean Registry. Int J Hematol. 2013;97(6):749–57.
8. Kulasekararaj A, Hill A, Rottinghaus S, Langemeijer S, Wells R, Gonzalez-Fernandez F et al. Ravulizumab (ALXN1210) vs eculizumab in C5-inhibitor–experienced adult patients with PNH: the 302 study. Blood. 2019;133(6):540-549.
9. Ariceta G, Dixon B, Kim S, Kapur G, Mauch T, Ortiz S et al. The long-acting C5 inhibitor, ravulizumab, is effective and safe in pediatric patients with atypical hemolytic uremic syndrome naïve to complement inhibitor treatment. Kidney International. 2021;100(1):225-237.
10. Tanaka K, Adams B, Aris A, Fujita N, Ogawa M, Ortiz S et al. The long-acting C5 inhibitor, ravulizumab, is efficacious and safe in pediatric patients with atypical hemolytic uremic syndrome previously treated with eculizumab. Pediatric Nephrology. 2020;36(4):889-898.
11. Kulasekararaj A, Hill A, Rottinghaus S, Langemeijer S, Wells R, Gonzalez-Fernandez F et al. Ravulizumab (ALXN1210) vs eculizumab in C5-inhibitor–experienced adult patients with PNH: the 302 study. Blood. 2019;133(6):540-549.
12. Holguin MH, et al. Isolation and characterization of a membrane protein from normal human erythrocytes that inhibits reactive lysis of the erythrocytes of paroxysmal nocturnal hemoglobinuria. J Clin Invest. 1989;84(1):7 17.
13. Jang, J. H., et al. (2016). Predictive Factors of Mortality in Population of Patients with Paroxysmal Nocturnal Hemoglobinuria (PNH): Results from a Korean PNH Registry. Journal of Korean medical science, 31(2), 214–221.
14. Hillmen, P., et al. (1995). Natural history of paroxysmal nocturnal hemoglobinuria. The New England journal of medicine, 333(19), 1253–1258.
15. Fakhouri F, Zuber J, Fremeaux-Bacchi V, et al. Haemolytic uraemic syndrome. Lancet. 2017 Aug 12; 390: 681-696
16. Yan K, Desai K, Gullapalli L, et al. Epidemiology of Atypical Hemolytic Uremic Syndrome: A Systematic Literature Review. Clin Epidemiol. 2020;12:295-305.
17. Walport MJ. Complement. First of two parts. N Engl J Med [Internet]. 2001 [citado el 14 de junio de 2022];344(14):1058–66. Disponible en: https://pubmed.ncbi.nlm.nih.gov/11287977/
18. Murphy K, Travers P, Walport M. Janeway’s Immunobiology. 8th ed. New York, NY: Garland Science; 2012:37-73.
19. Kelly R, Richards S, Hillmen P, Hill A. The pathophysiology of paroxysmal nocturnal hemoglobinuria and treatment with eculizumab. Ther Clin Risk Manag [Internet]. 2009 [citado el 14 de junio de 2022];5:911–21. Disponible en: https://pubmed.ncbi.nlm.nih.gov/20011245/2.




