Redacción Farmacosalud.com
Un análisis exhaustivo realizado in silico de emparejar los 64 agentes terapéuticos desarrollados para tratar el cáncer de mama -la mitad en uso y la mitad en fase clínica- ha permitido a investigadores del Instituto de Investigación Biomédica (IRB Barcelona) identificar 10 combinaciones completamente nuevas, nunca probadas y con alto potencial para combatir el tumor mamario. El trabajo[1] liderado por el investigador ICREA Patrick Aloy se ha basado en el estudio de las redes de señalización celular, es decir, teniendo en cuenta las señales celulares que los fármacos alteran al tocar las moléculas diana donde van dirigidas. 7 de las 10 combinaciones testadas en células de cáncer de mama in vitro han mostrado un buen grado de sinergia, es decir, que el efecto conjunto es más potente que la suma de los efectos individuales, y una de ellas ha sido validada en ratones. Los resultados en modelos murinos indican que la combinación de raloxifene y cabozantinib, dos fármacos usados hoy en día por los oncólogos, potencia "drásticamente" el efecto antitumoral de los dos fármacos por separado, como escriben los autores en ‘Cancer Research’, revista científica de la Asociación Norteamericana de Enfermos de Cáncer.
Aloy, jefe del laboratorio de Bioinformática estructural y biología de redes en el IRB Barcelona, resume: "Encontramos muchas más combinaciones sinérgicas in silico que las surgidas de ensayos combinatorios hechos hasta ahora en laboratorio con técnicas de alto rendimiento, y damos detalle experimental de las mismas. Esto significa que los análisis computacionales previos se traducen en mejores resultados y que son más fiables". Los investigadores indican que para el 70% de las combinaciones testadas, el efecto conjunto de los dos fármacos es "mucho mayor" que el efecto individual y, por lo tanto, "para conseguir los mismos efectos terapéuticos se podrían reducir mucho las dosis".
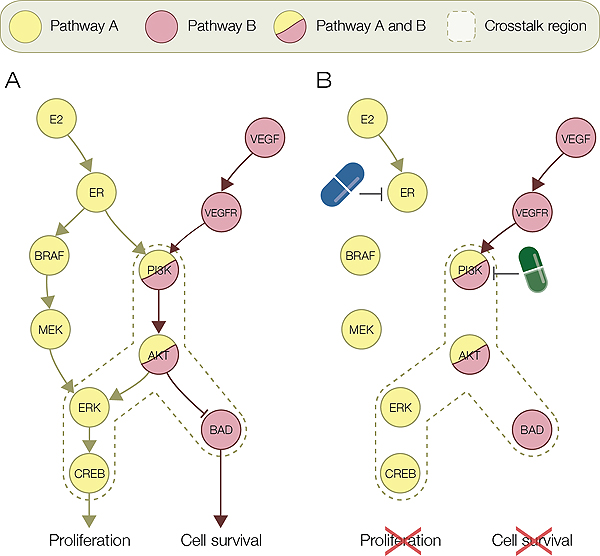
La terapia combinada de dos fármacos es una aproximación prometedora para combatir la resistencia en cáncer. Análisis computacionales en el IRB ayudan a detectar nuevas combinaciones para el cáncer de mama, como la combinación de raloxifene y cabozantinib (Gráfico: Samira Jaeger, IRB Barcelona)
Fuente: IRB Barcelona
Combinar raloxifene y cabozantinib reduce el tumor en un 60%
En el caso concreto de combinar raloxifene y cabozantinib testado en ratones, los científicos ven que el tumor se reduce en un 60%, mientras que el efecto individual de los fármacos sólo consigue detener el crecimiento del tumor. Además, pueden usarse 3 veces menos dosis de un fármaco y 25 veces menos del otro que las cantidades que se prescriben actualmente. "Esto por sí solo ya es muy importante, dado que los fármacos no dejan de ser veneno para matar células. Si con menos dosis consigues más o -aunque sea el mismo efecto quimioterapéutico- es una gran ventaja para los pacientes de cara a mitigar los efectos secundarios", dice Aloy. "Además, y en principio, se evitaría o aplazaría la aparición de resistencias", prevé. En el tratamiento del cáncer, también en el de mama, uno de los problemas con que se enfrentan pacientes y oncólogos es la aparición de resistencias al tratamiento. Las células cancerosas se vuelven "insensibles" a los fármacos que las deberían matar.
Estas resistencias se deben a que la célula cancerosa, mediante la aparición de mutaciones aleatorias, aprende a sortear la acción del fármaco. En un 15% de los casos, la finta se produce porque se ponen en funcionamiento señales moleculares alternativas que permiten a las células tumorales reactivar la división celular o evitar la muerte celular programada. La terapia combinada de dos o más fármacos se presenta como una vía prometedora para combatir este tipo de resistencia. "Nuestros análisis nos han permitido predecir las vías de señalización que quedan inhibidas con la acción conjunta de dos fármacos", indica Samira Jaeger, investigadora posdoctoral y primera autora del trabajo. Los científicos validaron a nivel molecular que, efectivamente, se neutralizan las moléculas que predecía el modelo in silico. "Nuestro objetivo combinando fármacos es atacar la célula tumoral por varios puntos a la vez que haga muy difícil que resista al tratamiento porque tendrá incapacitadas al mismo tiempo las vías que le permiten sobrevivir y proliferar", indica.
Fuente: IRB Barcelona
Tres líneas de investigación abiertas
Ahora, con el modelo computacional de redes validado, los científicos tienen abiertas tres líneas de investigación. En primer lugar y para avanzar hacia la clínica, probarán la combinación de raloxifene y cabozantinib en tumores de pacientes implantados en ratones. Para dicho objetivo, como en el trabajo ya realizado, cuentan con la colaboración del investigador ICREA del programa de Oncología, Angel R. Nebreda, también del IRB Barcelona. En segundo lugar, y con el mismo objetivo de encontrar tratamientos más potentes para el cáncer de mama, el laboratorio se centrará en emparejar un antitumoral y fármacos prescritos para otras alteraciones, como antidiabéticos o antihipertensivos. En último lugar, el laboratorio de Aloy está poniendo a punto la metodología experimental que ha de permitir comprobar que las terapias combinatorias son eficientes para combatir la resistencia a largo plazo.
Este estudio ha contado con financiación del Consejo Europeo de Investigación (ERC Consolidator grant), el Ministerio de Economía y Competitividad y fondos FEDER, una beca EU Marie Curie COFUND y de la Generalitat de Catalunya.
Pertuzumab, con buenos resultados en cáncer de mama her2+
Por otro lado, la compañía Roche informa que el anticuerpo monoclonal Pertuzumab (Perjeta®) se confirma como la opción que aporta más eficacia de forma segura y bien tolerada cuando se combina con Trastuzumab (Herceptin®) y con cualquiera de los taxanos (quimioterapias) o terapia hormonal estándar en cáncer de mama HER2+ avanzado y también en fases iniciales antes de la cirugía (neoadyuvancia). Así lo sugieren nuevos datos de los estudios BERENICE, PERTAIN y PERUSE, que se han presentado en el último San Antonio Breast Cancer Symposium (SABCS, San Antonio-Texas).
Desde la aprobación de Trastuzumab hace más de 15 años, Pertuzumab es la terapia que ha mostrado el mayor beneficio clínico en los casos avanzados en este tipo de tumor HER2+, que representa aproximadamente el 18% de todos los casos de tumor mamario.
Referencias
1. Samira Jaeger, Ana Igea, Rodrigo Arroyo, Victor Alcalde, Begoña Canovas, Modesto Orozco, Angel R. Nebreda and Patrick Aloy. Quantification of pathway crosstalk reveals novel synergistic drug combinations for breast cancer. Cancer Research (2016) DOI: 10.1158/0008-5472.CAN-16-0097




