Redacción Farmacosalud.com
La compañía MSD ha anunciado que el Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento ha emitido una opinión positiva recomendando la aprobación de KEYTRUDA® (pembrolizumab), la terapia anti-PD-1 de la compañía, como primera línea de tratamiento del cáncer de pulmón no microcítico (CPNM) metastásico en adultos cuyos tumores tienen una elevada expresión de PD-L1 (proporción de células tumorales positivas [TPS, por sus siglas en inglés] del 50% o más) sin mutaciones positivas de EGFR o ALK. La Comisión Europea revisará ahora la recomendación para obtener la autorización de comercialización en la Unión Europea. Se espera que se anuncie su decisión final en el primer trimestre de 2017. Actualmente, KEYTRUDA está aprobado en Europa como segunda línea de tratamiento para los pacientes con CPNM localmente avanzado o metastásico cuyos tumores expresen PD-L1 y que hayan recibido al menos un tratamiento de quimioterapia previo. Los pacientes con mutaciones positivas de EGFR o ALK también deben haber recibido un tratamiento dirigido antes de recibir KEYTRUDA.
La opinión positiva está basada en datos procedentes del KEYNOTE-024, un estudio pivotal que demostró una supervivencia global (SG) y una supervivencia libre de progresión (SLP) superior de KEYTRUDA (pembrolizumab) en comparación con la quimioterapia en los pacientes cuyos tumores expresan altos niveles de PD-L1 sin mutaciones positivas de EGFR o ALK. KEYNOTE-024 es un estudio aleatorizado, abierto, de fase 3 que evalúa KEYTRUDA como monoterapia con una dosis fija de 200 mg en comparación con el tratamiento habitual de quimioterapia basado en platino para el tratamiento de los pacientes con CPNM escamoso y no escamoso metastásico. En el estudio participaron pacientes que no habían recibido un tratamiento previo de quimioterapia sistémica para su enfermedad metastásica y cuyos tumores tenían una elevada expresión de PD-L1 sin alteraciones en los genes EGFR o ALK.
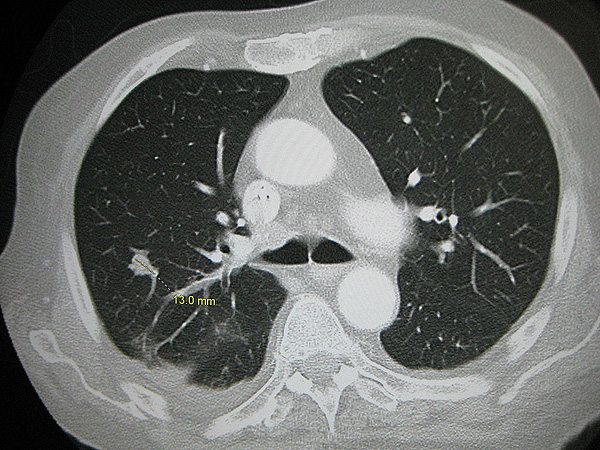
Metástasis pulmonar
Autor/a de la imagen: James Heilman, MD
Fuente: Wikimedia Commons
Un bloqueador de la interacción entre PD-1 y sus ligandos, PD-L1 y PD-L2
KEYTRUDA® es un anticuerpo monoclonal humanizado que bloquea la interacción entre PD-1 y sus ligandos, PD-L1 y PD-L2. Por la unión al receptor PD-1 y el bloqueo de la interacción con sus ligandos, KEYTRUDA® libera la inhibición mediada por vía PD-1 de la respuesta inmune, incluyendo la respuesta inmune antitumoral. En España KEYTRUDA en monoterapia está indicado en el tratamiento de melanoma avanzado (irresecable o metastásico) en adultos. KEYTRUDA está indicado para el tratamiento del cáncer de pulmón no microcítico (CPNM) localmente avanzado o metastásico en adultos cuyos tumores expresen PD-L1 y que hayan recibido al menos un tratamiento de quimioterapia previo. Los pacientes con mutaciones positivas de EGFR o ALK también deben haber recibido tratamiento aprobado para estas alteraciones antes de recibir KEYTRUDA a la dosis recomendada de 2 mg/kg administrados por vía intravenosa durante 30 minutos cada tres semanas. La aprobación de pembrolizumab es efectiva en los 28 países miembros de la Unión Europea (UE).
El cáncer de pulmón, el cual se forma en el tejido pulmonar, normalmente dentro de las células que revisten las vías respiratorias, es la principal causa de muerte por tumor en el mundo. De hecho, cada año mueren más personas de cáncer de pulmón que de cáncer de colon, mama y próstata en conjunto. Los dos principales tipos de cáncer de pulmón son el cáncer de pulmón no microcítico (CPNM) y el cáncer de pulmón de células pequeñas (CPCP). El CPNM es el cáncer de pulmón más frecuente y representa alrededor del 85 % de todos los casos. La supervivencia a 5 años para los pacientes que padecen cáncer de pulmón avanzado o metastásico (fase IV) se sitúa en el 2%.
Con ceritinib, SPL de 16,6 meses en CPNM avanzado ALK+
Por su parte, Novartis ha anunciado los resultados de su estudio de Fase III abierto, aleatorizado, controlado con fármaco activo, multicéntrico, ASCEND-4 que reveló que los pacientes con cáncer de pulmón no microcítico (CPNM) avanzado, positivo para la quinasa del linfoma anaplásico (ALK) tratados en primera línea con Zykadia® (ceritinib) presentaron una mediana de supervivencia libre de progresión (SLP) de 16,6 meses (intervalo de confianza [IC] del 95%: 12,6, 27,2), en comparación con 8,1 meses (IC95%: 5,8, 11,1) en pacientes tratados con quimioterapia estándar de primera línea con mantenimiento. Esto equivale a una reducción del 45% en el riesgo de progresión de la enfermedad (hazard ratio [HR] = 0,55, P <0,001)[1]. "Estos datos demuestran el potencial de aumentar en más del doble la supervivencia libre de progresión de un paciente cuando toma Zykadia como su primer inhibidor de ALK en lugar de someterse a tratamiento con quimioterapia", explica el investigador principal, el Dr. Gilberto de Castro Jr., jefe de oncología torácica y cáncer de cabeza y cuello en el Servicio de Oncología Clínica del Instituto del Cáncer de San Pablo (ICESP), en São Paulo, Brasil. "Para los médicos, que trabajan constantemente para ampliar la respuesta de un paciente al tratamiento en la primera línea, los resultados de ASCEND-4 son muy convincentes", agrega.
Lobectomías VATS: muy usada en tumor pulmonar
Un quirófano
Autor/a de la imagen: E. Arandes / www.farmacosalud.com
Fuente: Gentileza del Hospital Sagrat Cor de Barcelona (Archivo)
“Con la lobectomía VATS el paciente puede incorporarse a su vida más rápido, con menos secuelas y con una calidad global de la asistencia muy superior a los tradicionales abordajes abiertos, que se llevan a cabo mediante la separación de las costillas, siendo esta la diferencia principal entre la lobectomía toracoscópica VATS y la lobectomía abierta”, explica el Dr. Nicolás Moreno Mata, expresidente de la Sociedad Española de Cirugía Torácica (SECT) y responsable de Cirugía Torácica en el Hospital Virgen del Rocío, de Sevilla. La cirugía torácica mínimamente invasiva, lobectomía VATS, consiste en un abordaje mediante una pequeña incisión en el tórax sin separación de las costillas y la visión toracoscópica a través de un monitor. Esta técnica, que se ha impuesto en muchos países desarrollados y cuyo uso está en continua expansión, se utiliza en numerosos procedimientos quirúrgicos, siendo la elegida para el abordaje del cáncer de pulmón en muchos centros, indican desde la firma Johnson and Johnson Medical Devices Companies.
“La mortalidad en general de la lobectomía pulmonar por cáncer de pulmón, que es la más habitual, se sitúa por debajo del 3%. Por su parte la lobectomía VATS, al realizarse mediante un abordaje menos invasivo, presenta una morbimortalidad menor, aclara el doctor Moreno. Según cifras oficiales del Ministerio, se realizan en España unas 4.000 lobectomías al año, a las que habría que sumar las intervenciones que se realizan en cirugía privada, mientras que por cirugía mínimamente invasiva “se realizan entre un 25 y un 30% aproximadamente, por lo que existe un margen de mejora de incorporar a nuevos pacientes a este procedimiento”, manifiesta el especialista.
Referencias
1. De Castro, G Jr., et al. First-line Ceritinib Versus Chemotherapy in Patients With ALK-rearranged (ALK+) NSCLC: A Randomized, Phase 3 Study (ASCEND-4). Abstract # PL03.07. IASLC World Conference on Lung Cancer. Vienna, 6 December 2016.




