Redacción Farmacosalud.com
Roche ha anunciado datos de su estudio fase II NOBILITY, que investiga la seguridad y eficacia de Gazyvaro® (obinutuzumab) en adultos con nefritis lúpica proliferativa[1]. El estudio alcanzó el objetivo primario con Gazyvaro® en combinación con la terapia estándar (micofenolato de mofetilo o ácido micofenólico y corticosteroides), demostrando su superioridad frente a placebo más la terapia estándar. Los pacientes tratados con el fármaco mostraron un incremento de las tasas de respuesta renal completa (RRC) desde la semana 52 a la 76. Concretamente, un 40% de los pacientes del grupo Gazyvaro® alcanzó RRC en la semana 76 de tratamiento (p=0,007), frente a un 18% del grupo placebo. Además, Gazyvaro® cumplió con los criterios secundarios clave de eficacia que muestran una mejor respuesta renal general (respuesta renal completa o parcial) y mejores marcadores serológicos de la actividad de la enfermedad en comparación con placebo.

Fuente: www.farmacosalud.com / IMAGEN DE ARCHIVO
Gentileza del Centro Nacional de Microbiología. Instituto de Salud Carlos III de Madrid
No se registraron nuevos hallazgos de seguridad con Gazyvaro® hasta el momento del análisis. Hasta la semana 76, los eventos adversos serios (24% vs 29% en el grupo placebo) y las infecciones graves (6% vs 18% en el grupo placebo) no se incrementaron con Gazyvaro®. Estos datos se han dado a conocer en el Congreso de la American Society of Nephrology (ASN) Kidney Week 2019 en Washington (Estados Unidos) y en el Encuentro Anual del American College of Rheumatology (ACR) en Atlanta, Estados Unidos[2]. Gazyvaro es un anticuerpo monoclonal anti-CD20 humanizado tipo II que se une a la proteína CD20 de ciertas células B. Se cree que funciona atacando las células objetivo de manera directa y junto con el sistema inmune del organismo.
La nefritis lúpica es una manifestación grave y potencialmente mortal del lupus eritematoso sistémico (LES), que se produce como resultado de la inflamación de los riñones. Su forma proliferativa es la más grave y está asociada con un alto riesgo de enfermedad renal en etapa terminal y muerte[3,4]. En septiembre de 2019, la Agencia Americana del Medicamento (FDA, por sus siglas en inglés) otorgó a Gazyvaro® la condición de Breakthrough Therapy Designation como tratamiento para adultos con nefritis lúpica y lo hizo basándose en los datos del estudio de fase II NOBILITY.
Sobre el estudio Nobility
El estudio Nobility (NCT02550652) es un ensayo clínico fase II, multicéntrico, aleatorizado, doble ciego, controlado con placebo, que comparó la seguridad y eficacia de Gazyvaro®, en combinación con mofetil micofenolato (MMF) o ácido micofenólico (MPA) y corticoides, en pacientes adultos con nefritis lúpica proliferativa clase III o IV ISN/RPS 2003. El estudio reclutó a 125 personas que fueron asignadas al azar para recibir infusiones de Gazyvaro® o placebo en los días 1, 15, 168 y 182. El objetivo primario fue la proporción de pacientes que alcanzaron una remisión renal completa definida por protocolo (RRC) a la semana 52 de tratamiento.
Los principales criterios secundarios incluyeron respuestas renales (completas o parciales) y marcadores serológicos de la actividad de la enfermedad en comparación con placebo. A los pacientes se les hizo un seguimiento ciego durante 104 semanas y los que presentaban una disminución persistente de las células B están siendo seguidos por razones de seguridad y se les somete a mediciones de estas células.
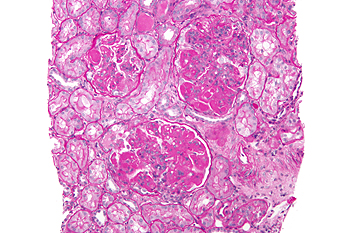
Biopsia con nefritis lúpica difusa
Autor/a de la imagen: Nephron - Trabajo propio. High magnification micrograph of diffuse proliferative lupus nephritis, class IV. PAS stain. Related images High mag. Very high mag. Very high mag
Fuente: Wikipedia
La nefritis lúpica es un trastorno renal grave y potencialmente mortal. Se trata de una de las manifestaciones más graves del lupus eritematoso sistémico (LES), una enfermedad autoinmune en la que el propio sistema inmunológico de la persona ataca a las células y órganos sanos, incluyendo, en el caso de la nefritis lúpica, los riñones[3]. Esto provoca inflamación de estos órganos y puede llegar a provocar la aparición de sangre y/o proteína en la orina, hipertensión, función renal deficiente o insuficiencia renal. Se estima que el LES afecta a 24 de cada 100.000 personas en el mundo[5], calculándose que hasta el 60% de ellas desarrollarán nefritis lúpica, y el 25% de las personas con LES que manifiestan esta afección desarrollan enfermedad renal en etapa terminal[3,4].
El lupus tiene un gran impacto en las mujeres, lo que hace que constituyan el 90% de la población con esta enfermedad. Las mujeres de grupos étnicos africanos, hispanos y asiáticos tienen de dos a tres veces más probabilidades de ser diagnosticadas de lupus que las caucasianas[6]. En la actualidad, no existe cura para esta patología ni para la nefritis lúpica.
Referencias
1. Rovin B, Aroca G, Alvarez A, et al. A Phase 2 Randomized, Controlled Study of Obinutuzumab with Mycophenolate and Corticosteroids in Proliferative Lupus Nephritis. Presented at the ASN Kidney Week, Washington, DC, 5 - 10 November 2019. Abstract FR-OR136.
2. Furie R, Aroca G, Alvarez A et al. A Phase 2 Randomized, Controlled Study of Obinutuzumab with Mycophenolate and Corticosteroids in Proliferative Lupus Nephritis [abstract 939]. Arthritis Rheumatol. 2019; 71 (suppl 10).
3. A. de Zubiria Salgado and C. Herrera-Diaz. Lupus Nephritis: An Overview of Recent Findings. Autoimmune Diseases. 2012; 2012: 221.
4. R. Saxena et al. Lupus Nephritis: Current Update. Arthritis Research & Therapy. 2011; 13:240.
5. Lupus UK. Epidemiology of Lupus.[Internet; cited May 2019]. Available from: https://www.lupusuk.org.uk/medical/gp-guide/introduction-to-lupus/epidemiology-of-lupus/. (Last accessed 11 November 2019)
6. Lupus Research Alliance. Lupus Fact Sheet. [Internet; cited May 2019]. Available from: http://www.lupusresearch.org/wp-content/uploads/2017/09/Lupus-Fact-Sheet.pdf. (Last accessed 11 November 2019)




