Redacción Farmacosalud.com
Roche ha anunciado que el Comité Europeo de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) ha emitido una opinión positiva para el uso de Obinutuzumab (Gazyvaro®) en combinación con quimioterapia, seguido de una terapia de mantenimiento con Obinutuzumab, como nueva opción de tratamiento frente al linfoma folicular avanzado no tratado previamente. La recomendación del CHMP se basa en los resultados del estudio fase III GALLIUM. El linfoma folicular es el tipo más frecuente de los linfomas no Hodgkin indolentes (de lento crecimiento). Se considera incurable y es frecuente que los pacientes sufran recaídas[1,2]. Se espera que, tras la recomendación de CHMP, Obinutuzumab sea aprobado por la Comisión Europea en un futuro próximo.
GALLIUM es el primer ensayo fase III en pacientes con linfoma folicular que no han sido tratados previamente que muestra un SLP superior a Rituximab, la actual terapia estándar. Sus resultados muestran que Obinutuzumab reduce el riesgo de progresión de la enfermedad o muerte (SLP), según la evaluación del investigador, en un 34% (HR=0,66; 95% IC 0,54-0,93, P=0,001) en comparación con Rituximab. Según la evaluación de un comité de revisión independiente (CRI), el riesgo de progresión de la enfermedad o fallecimiento se redujo un 29% (HR=0,71; 95% CI 0,54-0,93, P=0,014) en comparación con el tratamiento basado en Rituximab. Aún no se ha alcanzado la media de SLP en ninguno de los dos grupos de tratamiento. La evaluación del investigador mostró que a los tres años, el 80% de los pacientes que recibieron tratamiento con Obinutuzumab estaban libres de progresión en comparación con el 73,3% de los que recibieron Rituximab. Los efectos secundarios con ambos fármacos fueron similares a los observados en estudios previos.
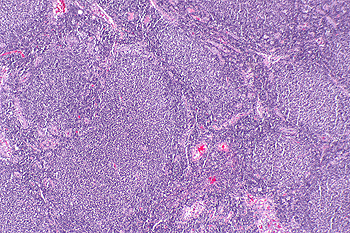
Microfotografía de linfoma folicular, que muestra los característicos folículos linfoides que le dan el nombre a la enfermedad. Tinción H&E
Autor/a de la imagen: Nephron
Fuente: Wikipedia
Acerca del estudio GALLIUM
GALLIUM (NCT01332968) es un estudio internacional fase III, abierto, multicéntrico, aleatorizado, con dos brazos, dirigido a comparar la eficacia y seguridad de Obinutuzumab, combinado con quimioterapia, seguido de Obintuzumab solo durante dos años, en comparación ‘head-to-head’ con Rituximab combinado con quimioterapia, seguido de Rituximab en monoterapia durante dos años o hasta progresión de la enfermedad (lo que sucediera primero). Los tipos de quimioterapia empleados fueron CHOP, CVP o bendamustina, a elección de cada uno de los centros participantes en el estudio antes de comenzar el reclutamiento de pacientes. Participaron 1401 pacientes con LNHi que no habían sido tratados previamente, de los que 1202 tenían linfoma folicular. El objetivo primario del estudio era la SLP evaluada por los investigadores en pacientes con linfoma folicular, mientras que los secundarios incluían la SLP según un comité de valoración independiente, la SLP en todos los pacientes del estudio (con cualquier forma de LNHi), la tasa global de respuesta (tasa de respuesta completa y respuesta completa), la supervivencia global y la seguridad.
El estudio GALLIUM se ha llevado a cabo en colaboración con el Grupo Alemán para el Estudio de Linfomas de Bajo Grado de Malignidad (GLSG, Alemania), el Grupo de Estudio de Hematología y Oncología del Este de Alemania (OSHO, Alemania) y el Instituto Nacional de Investigaciones Oncológicas (NCRI, Reino Unido).
Obinutuzumab es el primer anticuerpo monoclonal de tipo II anti-CD20 modificado por glicoingeniería, que se une a la proteína CD20 de las células B cancerosas, causantes de ciertas formas de linfoma no Hodgkin (LNH) y de leucemia linfática crónica. Se ha diseñado específicamente para potenciar la destrucción de las células cancerosas, bien activando otras células inmunitarias para que ataquen a las malignas, bien induciendo directamente la muerte celular. Actualmente está aprobado en más de 80 países en combinación con clorambucilo para pacientes con leucemia linfática crónica que no han sido tratados previamente, y en combinación con bendamustina para pacientes con ciertos tipos de LF previamente tratados. La autorización para LLC se ha basado en los datos del estudio CLL11, que ha mostrado una mejora significativa con Obinutuzumab más clorambucilo en los diferentes resultados clínicos, incluyendo SLP, tasa de respuesta global, tasa de respuesta completa, y enfermedad mínima residual (EMR), cuando se compararon ‘head-to-head’ frente a Rituximab más clorambucilo.
Una patología por ahora incurable
La aprobación para ciertos tipos de LF previamente tratados se basaron en el estudio fase III GADOLIN en pacientes con LF que no han respondido o que han progresado durante o dentro de los seis meses al tratamiento previo con Rituximab, mostrando una mejora significativa en la SLP y en la SG con el tratamiento con Obinutuzumab frente a bendamustina en monoterapia. Gazyva® se comercializa con el nombre de Gazyvaro® en la UE y en Suiza. Asimismo, están en marcha diferentes estudios adicionales de combinación que investigan Obinutuzumab con otras terapias, ya aprobadas o en investigación, incluyendo inmunoterapias contra el cáncer y moléculas inhibidoras de tamaño pequeño, para una amplia gama de tumores de la sangre.
El linfoma folicular es el tipo de LNH indolente (de crecimiento lento) más frecuente, que representa cerca de uno de cada cinco casos de LNH[1]. Se considera incurable y es frecuente que los pacientes tengan recaídas. Se estima que cada día, más de 50 personas en Europa son diagnosticadas de un tipo de LNH[2]. Se estima que en todo el mundo cerca de 75.000 personas/año son diagnosticadas de un linfoma folicular.
Referencias
1. Shankland KR, Armitage JO, Hancock BW: Non-Hodgkin lymphoma. Lancet 380 (9844): 848-57, 2012.
2. Ferlay J, et al. GLOBOCAN 2012 v1.0, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11 [Internet]. Lyon, France: International Agency for Research on Cancer; 2013. Available from: http://globocan.iarc.fr/old/summary_table_pop-html.asp?selection=224900&title=World&sex=0&type=0&window=1&sort=0&submit=%C2%A0Execute (accessed on 14/03/2016).




