Redacción Farmacosalud.com
Los pacientes que debido a un accidente cerebrovascular o ictus presentan 'hemiparesia', aunque en realidad todavía tienen movilidad en la parte afectada, con frecuencia la infrautilizan con el inconveniente añadido de que un período de tiempo prolongado de no utilizarla puede conducir a una mayor pérdida de su función. "Podemos decir que el cerebro, con el ictus, ha perdido la confianza en el uso de la extremidad afectada", comenta Belén Rubio, primera autora de una investigación[1] publicada en el ‘Journal of NeuroEngineering and Rehabilitation’ que muestra las ventajas de la realidad virtual en la rehabilitación de pacientes después de un ictus. Este llamado 'no uso aprendido' es un fenómeno bien conocido en pacientes con accidente cerebrovascular y conlleva una reducción de su calidad de vida. La nueva propuesta de rehabilitación basada en la realidad virtual se llama Reinforcement-Induced Movement Therapy (RIMT).
Algunas terapias de rehabilitación empleadas para superar el efecto de "no uso aprendido" consisten en forzar al paciente a utilizar la extremidad afectada para restringir el movimiento de la extremidad sana. Estrategia de tratamiento conocida como terapia de movimiento inducido por restricción del lado sano (del inglés Constraint-Induced Movement Therapy, CIMT). Sin embargo, este método tiene varias limitaciones y la alta exigencia en el cumplimiento de sus protocolos compromete gravemente el correcto seguimiento de la rehabilitación.
Nuevo método RIMT: realidad virtual para recuperar funcionalidad tras un ictus
Fuente: UPF
Estimulación visual y motora a través de la realidad virtual
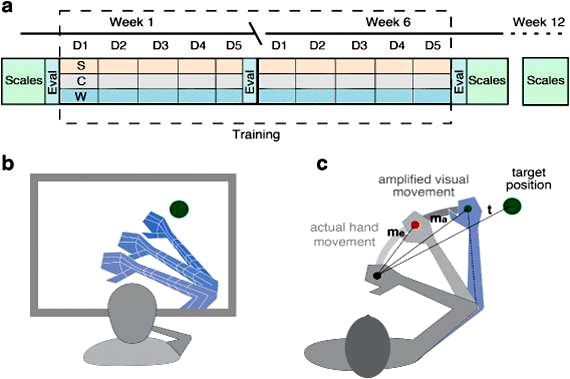
Miembros del Grupo de Investigación Synthetic, Perceptive, Emotive and Cognitive (SPECS), del centro de Neurorobótica y Sistemas Autónomos (N-RAS) que dirige el profesor de investigación ICREA Paul Verschure, en el Departamento de Tecnologías de la Información y las Comunicaciones (DTIC) de la UPF, han propuesto un método alternativo para fomentar el uso de la extremidad parética. El nuevo método de rehabilitación propuesto es el Reinforcement-Induced Movement Therapy (RIMT) y está basado en la estimulación visual y motora a través de la realidad virtual.
La eficacia en la rehabilitación post-ictus del RIMT se presenta en un trabajo publicado en el ‘Journal of NeuroEngineering and Rehabilitation’, del que Belén Rubio es la primera autora y Paul Verschure el investigador principal, hecho en colaboración con expertos clínicos del Hospital Joan XXIII de Tarragona. En este estudio los investigadores han logrado en pacientes con accidente cerebrovascular crónico restablecer la confianza en la movilidad de la parte afectada y maximizar su funcionalidad creando la sensación virtual que los movimientos del paciente son más rápidos y más precisos, revirtiendo el "no uso aprendido" y favoreciendo mejoras motoras a largo plazo. Para ponerlo de manifiesto, los autores del trabajo llevaron a cabo un estudio clínico longitudinal y controlado en 18 pacientes con accidente cerebrovascular crónico, quienes realizaron durante seis semanas 30 minutos de entrenamiento de rehabilitación de la extremidad superior. El grupo experimental y el control emplearon el sistema de realidad virtual RGS (Rehabilitation Game System) desarrollado por el grupo SPECS, pero sólo los pacientes del grupo experimental tuvieron opción a amplificación visual de los movimientos del brazo afectado.
Aunque ambos grupos mostraron mejoras motoras significativas a las 6 semanas después de la rehabilitación, sólo el grupo experimental continuó exhibiendo mayores ganancias en la función motora del brazo afectado a las 12 semanas de seguimiento. Esta mejora fue acompañada por un aumento significativo del uso del brazo afectado en el grupo experimental. Los autores concluyen que el sistema de rehabilitación alternativo propuesto, el RIMT, parece ser beneficioso para inducir a una mejora significativa en pacientes con accidente cerebrovascular crónico. Este proyecto ha contado con el apoyo del European Research Commission proyecto cDAC, (FP7- IDEAS-ERC 341.196) EC H2020, proyecto socSMCs (H2020-EU.1.2.2. 641321) y proyecto SANAR de MINECO (Gobierno de España), han apuntado desde la Universidad Pompeu Fabra (UPF) de Barcelona.
Tras un ictus, las neuronas afectadas pueden ser la fuente de síntomas inexplicables
La visión tradicional de cómo afecta un accidente cerebrovascular en la función cerebral es a través de la pérdida de función, tales como la alteración del control motor, del habla, o de la memoria, según sea la zona cerebral lesionada. Sin embargo, pacientes que han sufrido un ictus también muestran síntomas de localización difícil tales como el dolor crónico o la depresión, los llamados déficits no específicos. ¿Cómo se pueden entender estos síntomas? Unos investigadores demuestran en un artículo[2] publicado en ‘PLoS Computational Biology’ que el trauma cortical afecta a redes neuronales distribuidas, es decir, afecta a múltiples regiones distribuidas en el cerebro, informa la Universidad Pompeu Fabra de Barcelona (UPF).
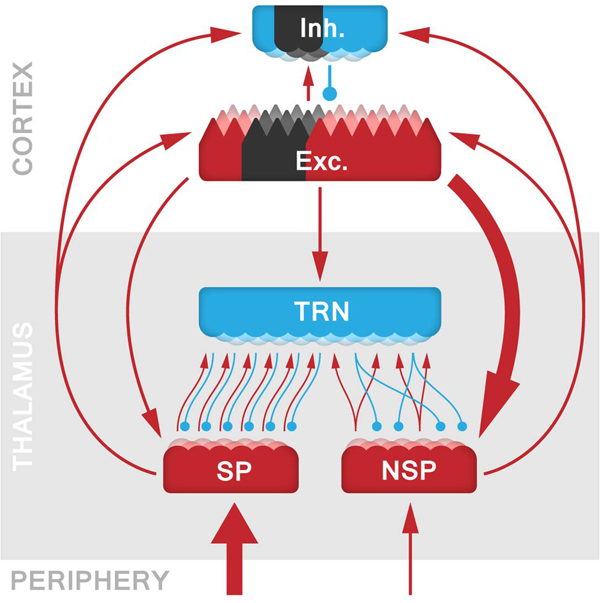
Fuente: UPF
Los autores del trabajo centraron su estudio en dos estructuras cerebrales: el neocórtex y el tálamo. El tálamo es la principal puerta de entrada de información para el neocórtex y estas dos estructuras se acoplan bidireccionalmente a través de una multitud de vías directas e indirectas. En un estudio teórico previo, Verschure y sus colaboradores identificaron el mecanismo subyacente a los déficits que se producen en estas estructuras anatómicas en la enfermedad de Parkinson (EP). En este caso se demostró que la desaceleración característica del EEG que se correlaciona con el temblor podría ser debido a un cambio patológico en el tálamo, que a su vez arrastraría al neocórtex. Estas interrupciones se conocen como disrítmias tálamo-cortical (DTC).
En este estudio, los autores se plantearon si las lesiones en el córtex cerebral podrían inducir déficits comparables y así dar cuenta de los síntomas no específicos de dolor crónico y depresión. Para ello analizaron los datos obtenidos por electroencefalograma (EEG) de los pacientes con accidente cerebrovascular al poco tiempo desde el inicio del infarto cerebrovascular. Buscaron rastros de actividad neural específicos en los EEG y los compararon con EEG obtenidos de otros grupos de pacientes que sufren de la enfermedad de Parkinson o del Síndrome de Dolor neurogénico (NP). Observaron que "el EEG de pacientes con ictus muestra un notable parecido con los EEG correspondientes pacientes con enfermedad de Parkinson y Síndrome de Dolor neurogénico, lo que sugiere que la actividad del tálamo está fuertemente afectada por lesiones de la corteza cerebral", concluyen los autores.
Así, los científicos han podido identificar específicamente las propiedades celulares, circuitos y redes locales que contribuyen al desarrollo del derrame cerebral inducido. En conjunto, estos resultados permite avanzar en la comprensión del impacto adverso del ictus en la funcionalidad de las redes neuronales cerebrales, así como de los síntomas indirectos, aún poco conocidos de la apoplejía, como el abandono hemiespacial o el dolor posterior al accidente cerebrovascular, lo que sugiere nuevas vías posibles de tratamiento del ictus y de las enfermedades neurológicas asociadas. Además, estos nuevos conocimientos pueden ayudar en la monitorización cerebral y en un futuro no muy lejano mejorar el diagnóstico desde esta nueva perspectiva emergente de la medicina basada en la funcionalidad de las redes cerebrales.
Fuente: Archivo
Tener diabetes y fibrilación auricular implica un mayor riesgo de ictus
Los pacientes con diabetes y fibrilación auricular tienen un mayor riesgo de sufrir un accidente cerebrovascular o ictus, según los datos del registro Prevención de eventos tromboembólicos–Registro Europeo en Fibrilación Auricular (PREFER en FA), presentado por el grupo Daiichi Sankyo Europa en el Congreso de la Sociedad Europea de Cardiología, ESC 2016, que se ha celebrado en Roma (Italia). PREFER en FA es un registro de pacientes que revela las lagunas de tratamiento actuales en el manejo de la fibrilación auricular (FA) en grupos de riesgo y las tendencias asociadas a las características específicas del paciente[3,4]. Este registro proporciona una información única sobre la reciente evolución del tratamiento de la FA en Europa y los desafíos a los que se enfrenta y ayuda a reforzar la evidencia de los resultados del paciente con FA en un entorno clínico.
Los resultados demuestran que los pacientes de FA con diabetes y tratamiento con insulina tienen un riesgo significativo mayor de padecer un accidente cerebrovascular (ictus) o embolismo sistémico en el primer año de seguimiento comparado con los pacientes de FA no diabéticos (5,2% contra 1,9% respectivamente; Hazard Ratio [HR] 2.89, 95% intervalo de confianza [CI] 1.67-5.02; P=0.0002) y comparado con aquellos diabéticos pero que no siguen un tratamiento de insulina (5.2% contra 1.8% respectivamente; HR 2.96, 1.49-5.87; P=0.0019)[3]. Los pacientes diabéticos que no reciben un tratamiento de insulina tienen una incidencia de eventos tromboembólicos similar a los pacientes sin diabetes (HR 0.97, 0.58-1.61; P=0.9)[3].
El registro ha demostrado que las mujeres experimentan una mayor carga de los síntomas en comparación con los hombres y que el tratamiento con anticoagulación oral fue similar en ambos géneros[4]. En comparación con los hombres, se demostró que las mujeres, con independencia de la edad y el país, tienen un riesgo un 65% menor de revascularización coronaria durante un año (95% CI [0.22, 0.56]), un 40% menos de síndrome coronario agudo (0.38 frente 0.93) y un 20% menos insuficiencia cardíaca crónica / fracción de eyección ventricular izquierda reducida (0.68, 0.96)[4]. No hay evidencia que demuestre que hombres y mujeres difieran en accidentes cerebrovasculares, ataques isquémicos transitorios, eventos tromboembólicos arteriales o sangrados mayores durante un año[4]. Aunque los resultados proporcionan una indicación de las diferencias de género, indican que es necesario investigar más para establecer si esto se puede utilizar para mejorar la gestión de la FA y la determinación de las necesidades de prevención y tratamiento.
La fibrilación auricular (FA) es una enfermedad en la que el corazón late de forma irregular y rápida. Cuando ocurre, la sangre puede acumularse y espesarse en las aurículas del corazón, lo que provoca un aumento del riesgo de sufrir un coágulo sanguíneo. Estos coágulos pueden romperse y viajar en el riego sanguíneo hacia el cerebro (o en ocasiones a otra parte del cuerpo), lo que puede provocar un ictus o accidente cerebrovascular[5].
Referencias
1. Belén Rubio Ballester, Martina Maier, Rosa María San Segundo Mozo, Victoria Castañeda, Armin Duff and Paul FMJ Verschure (2016),"Counteractinglearned non-use in chronic stroke patients with Reinforcement-induced movimientotherapy", Journal of NeuroEngineering and Rehabilitation, 9 de agosto.
2. van Wijngaarden JBG, Zucca R, Finnigan S, Verschure PFMJ (2016),"The Impact of Cortical Lesions on thalamo-Cortical Network Dynamics after Acute Ischaemic Stroke: A Combined Experimental and Theoretical Study, PLoS Comput Biol 12 (8): e1005048 . doi: 10.1371 / journal.pcbi.1005048.
3. Ricottini E et al. Insulin-requiring versus non-insulin requiring diabetes and thromboembolic risk in patients with atrial fibrillation: a PREFER in AF Registry substudy. [Abstract accepted for presentation at European Society of Cardiology Congress, August 2016].
4. Schnabel RB et al. Gender differences in clinical Presentation and predictors of one-year outcomes in atrial fibrillation. [Abstract accepted for presentation at European Society of Cardiology Congress, August 2016].
5. National Heart, Lung and Blood Institute – What is Atrial Fibrillation. Available at: http://www.nhlbi.nih.gov/health/dci/Diseases/af/af_diagnosis.html. Last accessed: July 2016.




