Dra. Carmen Guaza Rodríguez / Redacción Farmacosalud.com
La esclerosis múltiple (EM) es una enfermedad inflamatoria crónica del sistema nervioso central (SNC) de carácter autoinmune que ocasiona desmielinización y daño axonal. De etiología desconocida, es la segunda causa de discapacidad en adultos jóvenes en los países desarrollados, siendo más frecuente en mujeres que en varones1. El hecho de que se trate de una patología autoinmune desmielinizante con un componente neurodegenerativo hace que no se pueda hablar de una única causa responsable de su desarrollo. No es una enfermedad hereditaria, pero sí que existe una predisposición genética de susceptibilidad a padecer esta afección.
“Los pacientes con EM muestran diferencias con los controles sanos en algunos genes relacionados especialmente con el complejo principal de histocompatibilidad, además de otros implicados en los mecanismos regulatorios de la respuesta inmunitaria, entre los que se encuentran los que codifican para algunas citoquinas y sus receptores. Pienso que los mecanismos epigéneticos juegan un papel muy importante”, explica la Dra. Carmen Guaza Rodríguez, Profª de Investigación del CSIC (Consejo Superior de Investigaciones Científicas) jubilada y directora del Grupo de Neuroinmunología del Instituto Cajal del CSIC, en Madrid.

Dra. Carmen Guaza
Fuente: Dra. Guaza
Deficiencia en vitamina D, tabaquismo, infección con el virus de Epstein Barr…
De hecho, la epigenética* "brinda una oportunidad única para explicar la interacción entre los genes y el ambiente, de manera primordial, en una enfermedad tan heterogénea como la EM -prosigue la experta-. Así, tenemos que considerar una gran diversidad de factores ambientales tanto desencadenantes como moduladores de su evolución. La predisposición genética se debe acompañar de algún componente ambiental, entre los que destaco la deficiencia en vitamina D, el tabaquismo, la infección con el virus de Epstein Barr, la obesidad temprana y la alta ingesta de sal, entre muchos otros, para que debute la EM".
* Epigenética: estudio de los mecanismos que regulan la expresión de los genes sin una modificación en la secuencia del ADN
En la actualidad, la microbiota intestinal se considera un nuevo factor de riesgo, en el ámbito de la influencia ambiental, sobre la susceptibilidad a padecer enfermedades autoinmunes como la EM2. En esta línea, cabe señalar que “alteraciones en el equilibrio de las poblaciones microbianas que conforman la microbiota intestinal se consideran como un factor de riesgo en el inicio de los procesos de autoinmunidad”, argumenta la Dra. Guaza. Y es que la microbiota es clave en el desarrollo de la tolerancia inmunológica, es decir, en el entrenamiento del sistema inmune para discriminar lo propio de lo ajeno.
“En el caso de la EM, es importante subrayar que la microbiota influye en las respuestas inmunitarias distantes de la mucosa intestinal. La investigación en modelos preclínicos de EM con ratones libres de gérmenes y la manipulación de determinadas poblaciones bacterianas ha revelado la importancia de la microbiota en la autoinmunidad aberrante que conduce a la destrucción de la mielina que recubre los axones de las neuronas del Sistema Nervioso Central, distorsionando su capacidad de transmisión de señales nerviosas”, detalla.
Varios subtipos de esclerosis múltiple
La EM se clasifica en varios subtipos basándose en el curso clínico: a) remitente-recurrente (cuadros agudos de síntomas neurológicos con recuperaciones) b) secundariamente progresiva (las remisiones se vuelven infrecuentes y por lo general son remplazadas por un empeoramiento gradual) c) primariamente progresiva (síntomas neurológicos progresivos y graduales sin remisiones desde el inicio) d) progresiva-recurrente (subtipo de la forma primaria progresiva que puede tener recaídas raras sobreimpuestas a una progresión lenta)3.
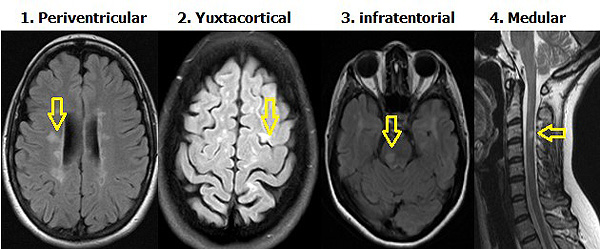
Esclerosis múltiple. Localización más frecuente de lesiones desmielinizantes en imagen IRM Periventricular (alrededor de sistema ventricular), yuxtacortical (junto a corteza cerebral), infratentorial (debajo de la tienda del cerebelo)
Autor/a de la imagen: DraazucenaDL
Fuente: Wikipedia
La esclerosis múltiple es una de las patologías más heterogéneas del SNC, siendo extremadamente variable tanto su sintomatología como la evolución de la misma. “En modelos animales de EM, sí sabemos que la manipulación de la microbiota intestinal modifica el curso de la Encefalomielitis Autoinmune Experimental (EAE) tanto en modelos de recaídas y remisiones como en la EAE progresiva, también en modelos transgénicos de EAE espontánea. Además, nuestro grupo ha demostrado el impacto de la microbiota en modelos virales de EM progresiva. A día de hoy, lo que sabemos es que los pacientes con EM muestran cambios en la microbiota intestinal respecto a los individuos sanos y que las alteraciones en las poblaciones microbianas que muestran los pacientes se modifican o se corrigen con los tratamientos terapéuticos; ello es muy clarificador en cuanto a la interacción microbiota-EM”, expone la Dra. Guaza.
“Debo decir, sin embargo -agrega-, que la mayoría de los estudios clínicos están realizados en pacientes con EM remitente-recurrente. Otro tipo de paradigmas que podemos considerar mixtos implican el trasplante fecal de pacientes con EM a ratones libres de gérmenes y los resultados son claros: se produce un aumento en la incidencia y severidad de la EAE en comparación con el trasplante fecal procedente de individuos controles sanos. Aunque no podamos definir de manera precisa cómo influye la microbiota intestinal en los diferentes subtipos de EM, me gustaría destacar que existe un gran interés en responder a esta pregunta. Se está avanzando de manera notable no sólo en el conocimiento de lo que significa la comunicación intestino-cerebro en EM y otras enfermedades, sino también sobre los mecanismos involucrados, es decir, cómo y a través de qué mediadores se produce esta apasionante conexión”.
“En EM, hay evidencias sólidas del papel beneficioso de múltiples cepas probióticas”
A todo esto, se han registrado mejoras cognitivas en pacientes con enfermedad de Alzheimer tras haber sido tratados con probióticos durante tres meses, y también se han observado reducciones de crisis en personas con epilepsia farmacorresistente que tomaron estos complementos nutricionales4. Estos resultados apoyan la idea de que los probióticos podrían ser en un futuro otro tratamiento para enfermedades neurológicas4.

Fuente: www.farmacosalud.com / Archivo
Gentileza del Centro Nacional de Microbiología. Instituto de Salud Carlos III de Madrid
“Existen un buen número de estudios sobre los efectos beneficiosos de los probióticos, no sólo en la enfermedad de Alzheimer y en la epilepsia refractaria, dado que también los hay sobre la enfermedad de Parkinson, patologías del espectro autista y muchas otras patologías neurológicas o psiquiátricas. Podríamos añadir los efectos beneficiosos de una dieta saludable, lo cual tiene su razón de ser y conecta directamente con el equilibrio microbiano deseable en nuestra microbiota”, remarca Guaza.
“En el caso de la EM, existen evidencias sólidas reveladoras del papel beneficioso de múltiples cepas probióticas y, por tanto, de su utilidad terapéutica como tratamientos coadyuvantes”, afirma la directora del Grupo de Neuroinmunología del Instituto Cajal.
Con todo, se requieren estudios traslacionales clínicos muy bien diseñados para conocer cómo se mantienen en el tiempo las poblaciones microbianas tras el tratamiento con probióticos. “Es decir, hay que establecer pautas y protocolos concretos de tratamiento, ya que todavía se tiene que trasladar a la clínica de la EM los enormes avances conseguidos. Esperamos que el consorcio internacional sobre el estudio del microbioma humano en la EM (www.imsms.org) ayude en este proceso en un futuro cercano”, apunta la especialista.
“El trasplante fecal se considera ya una posible opción terapéutica en EM”
Asimismo, se ha contemplado el uso de prebióticos o de otro tipo de complementos nutricionales -incluso el trasplante fecal- para tratar la EM. “Se trata de un campo amplio; el uso de prebióticos y de complementos nutricionales forma parte de la batería de ‘ayudas complementarias’ a la terapia farmacológica prescrita por el neurólogo. El trasplante fecal se considera ya una posible opción terapéutica en EM”, declara la Dra. Guaza. Sin embargo, todavía existe información limitada al respecto; faltan estudios originales con un mayor número de pacientes, no sólo como prueba de concepto, sino también para poner tener una visión real sobre la utilidad terapéutica del trasplante fecal en esta afección.
“Por último -manifiesta Guaza-, una reflexión: no debemos olvidar que en el diálogo bidireccional y cruzado entre la microbiota intestinal y el cerebro están involucradas señales neurales, inmunes y endocrinas que crean una extensa red de modo, y que la microbiota y sus metabolitos interactúan con el huésped a múltiples niveles. Esto impacta en la homeostasis y en la fisiología del individuo y, por tanto, en la conservación de una buena salud y en los procesos patológicos que subyacen en las enfermedades, incluida la EM”.
Referencias
1. Povedano Margarit B, Carvalho Monteiro G, Sánchez Herán I, Romero Delgado F, Yusta Izquierdo A. Esclerosis múltiple. Medicin Program Formac Med Contin Acred. 2019;12(78):4587-4597.
2. Guaza C. Microbiota y esclerosis múltiple. An Microbiota Probióticos Prebióticos. 2021;2(2):159-162.
3. Domínguez Moreno R, Morales Esponda M, Rossiere Echazarreta NL, Olan Triano R, Gutiérrez Morales JL. Esclerosis múltiple: revisión de la literatura médica. Rev. Fac. Med. (Méx.) [Internet]. 2012;55(5):26-35. Disponible en: http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0026-17422012000500005&lng=es.
4. Gómez-Eguílaz M, Ramón-Trapero JL, Pérez-Martínez L, Blanco JR. The microbiota-gut-brain axis and its great projections. Rev Neurol. 2019;68(3):111-117.




