En el paciente inmunodeprimido confluyen diversos mecanismos que pueden causar dolor. Por un lado, el dolor asociado a las enfermedades causantes de esta inmunosupresión (HIV, trasplantes, enfermedades autoinmunes, cáncer y efecto inmunosupresor de los tratamientos utilizados para el tratamiento de estas patologías). Por otra parte, las personas con una respuesta inmunológica deficiente son susceptibles de presentar infecciones y desarrollar nuevas enfermedades, muchas de las cuales también cursan con dolor y son a veces difícil de tratar por su componente neuropático asociado. La neuralgia postherpética y el dolor relacionado con el HIV son las entidades más representativas de este grupo.
A esto debemos sumarle la menor capacidad o resistencia al dolor básicamente debido al fallo del sistema inhibitorio endógeno, haciendo a estos pacientes más susceptibles de padecer dolor osteomuscular.
Estos pacientes encajan perfectamente en el concepto de paciente crónico complejo (PCC) dada la dificultad en el manejo de su proceso crónico. Ello es debido a la coexistencia de varias patologías crónicas al mismo tiempo relacionadas con la alteración de su inmunidad (comorbilidad) o por otras causas (multimorbilidad).
El manejo del PCC en esta situación es complicado porque frecuentemente está polimedicado, se visita con profesionales de diferentes especialidades, generalmente con escasa coordinación entre ellos, y presenta una elevada utilización de los recursos sanitarios. El paciente inmunocomprometido tiene unes características especiales, a menudo es un paciente joven, que a pesar de presentar múltiples comorbilidades no tiene el mismo perfil que otros PCC, cuya complejidad suele asociarse a las patologías propias de su edad (Tabla 1).

El papel del sistema inmune en el dolor y sus comorbilidades
La etiopatogenia de las enfermedades asociadas al dolor es multifactorial. La alteración de los mecanismos inmunológicos relacionados con el dolor podrían representar una mala adaptación de la respuesta inmune central sana, constituyendo un factor de mayor riesgo para el desarrollo de estas enfermedades asociadas.
Está demostrado que una lesión nerviosa conduce a la activación de la glía en la médula espinal (1). Los dos tipos celulares predominantes que la constituyen (microglía y astrocitos) contribuyen a la nocicepción y son inmunocompetentes, es decir, son capaces de reconocer y responder a señales inmunes (2). La microglía produce elevadas cantidades de citoquinas que participan en diversas patologías del sistema nervioso central (SNC), así como en comorbilidades directamente relacionadas con el dolor, como la depresión, ansiedad y abuso de drogas. En el SNC, las citoquinas forman parte de una red celular que incluye neuronas, microglías y astrocitos, los cuales activan la producción de citoquinas y amplifican sus señales. Estas señales actúan sobre el eje hipotálamo-hipofisario y producen cambios en el metabolismo de aminas fundamentales (serotonina, dopamina y glutamato).
Considerando estos mecanismos subyacentes comunes en el cerebro y la médula espinal en el dolor crónico y sus comorbilidades, tal vez estas alteraciones deberían ser entendidas como que suceden en “tierra fértil” en vez de que una enfermedad conduce a la otra, lo que podría constituir una vía interesante para futuras investigaciones.
Manejo del dolor en pacientes con HIV/SIDA
El dolor es el síntoma más frecuente que experimentan las personas con HIV/SIDA, con una tasa de prevalencia entre el 54 y el 83 % según las conclusiones de una reciente revisión sobre este tema (3). El enfoque en el manejo de este dolor varía según el tipo y la etiología del mismo (Tabla 2). En la mayoría de los casos se trata de un dolor moderado-intenso, con diversos factores que contribuyen y con la presencia de diferentes sitios anatómicos afectados, lo que sugiere que hay diferentes procesos patológicos que contribuyen al dolor al mismo tiempo.

Los avances farmacológicos producidos en los últimos años en el tratamiento del HIV no se han traducido en una mejoría en los niveles de dolor que sufre el paciente. Además, el dolor sigue estando infratratado por diferentes causas (3). Por parte del paciente, puede existir una dificultad para relacionar el dolor con la enfermedad y para comprender el alcance de otros tratamientos disponibles además de los retrovirales y, en relación al médico, el principal obstáculo sigue siendo la falta de reconocimiento del dolor como un problema importante.
La polineuropatía simétrica distal (PSD) es la complicación neurológica más frecuente pudiendo llegar a afectar hasta el 50 % de los pacientes (4). Se debe fundamentalmente a la afectación de pequeñas fibras nerviosas y aparece en fases avanzadas de la enfermedad, asociándose a una elevada morbilidad. Se caracteriza por presentar síntomas sensoriales con afectación simétrica de extremidades distales y disminución de la sensibilidad en una distribución en media de guante. Otros trastornos del sistema nervioso periférico que también cursan con dolor en estos pacientes se detallan en la Tabla 3.
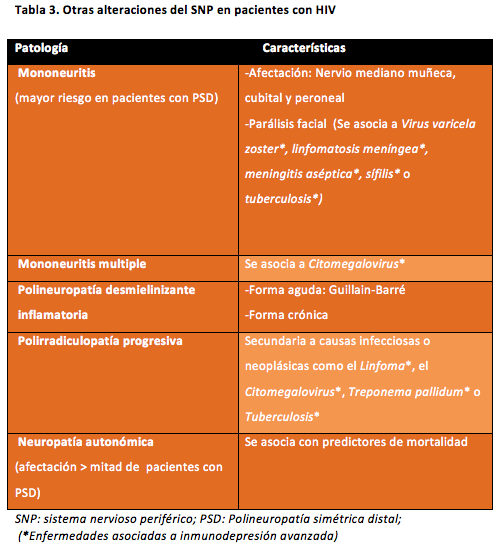
El tratamiento de la PSD sigue siendo complejo y difícilmente los pacientes alcanzan una resolución completa de sus síntomas. Actualmente no existe un tratamiento aprobado por la FDA para la neuropatía por HIV. Para el control sintomático del dolor neuropático se han utilizado los anticonvulsivantes, tratamientos tópicos, antidepresivos y analgésicos, cuya eficacia ha sido demostrada en el tratamiento del dolor neuropático de otras etiologías.
Sin embargo, muchos de estos fármacos no han demostrado su superioridad respecto al placebo en la polineuropatía por HIV (5). Los medicamentos tópicos, tales como parches de capsaicina a dosis altas y los anticonvulsivantes, son los que tienen los resultados más prometedores. Según los resultados obtenidos en estudios recientes, una sola aplicación de un parche de capsaicina al 8% puede aliviar el dolor durante varias semanas (6) y esta reducción tiene tendencia a ser mayor con estas dosis altas de capsaicina comparándolo con dosis bajas (0,04%) (7). No existen suficientes ensayos para determinar si los parches de lidocaína podrían ayudar a controlar el dolor en estos pacientes.
En los pacientes HIV y neuritis, la gabapentina ha mostrado una disminución significativa del dolor (8) y la pregabalina de la hiperalgesia (9). En cambio, la amitriptilina se mostró menos eficaz en la neuropatía por HIV en comparación con los resultados obtenidos con este fármaco en la neuropatía diabética (10).
Por último, el manejo médico debe optimizarse considerando todas las comorbilidades asociadas a estos pacientes como Diabetes mellitus, deficiencias vitamínicas o el abuso de alcohol u otros tóxicos. Se debe ser especialmente prudente con las prescripciones de opioides. No se recomienda el uso concomitante de estos fármacos ni los antidepresivos con alcohol por el alto riesgo de la potenciación de los efectos depresores. Los antirretrovirales y los antidepresivos tricíclicos (ADT) pueden presentar interacciones porque ambos se metabolizan en el hígado por el citocromo P-450. Es preciso manejar el dolor ajustándose a los fármacos adecuados y que han demostrado ser eficaces, evitando la polimedicación por el riesgo de interacciones medicamentosas y efectos secundarios en un paciente que ya está recibiendo otros tratamientos por las patologías asociadas a su enfermedad.
Manejo del dolor en pacientes con Neuralgia Postherpética
En pacientes jóvenes la neuralgia postherpética (NPH) aparece fundamentalmente en inmunodeprimidos (HIV, esclerosis múltiple, procesos oncológicos). En inmunocompetentes la incidencia de NPH aumenta con la edad llegando a alcanzar el 20 % en individuos mayores de 80 años (11).
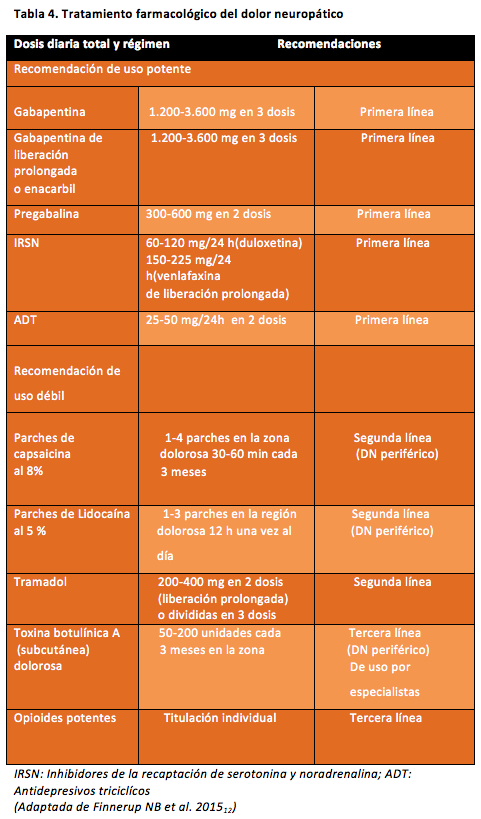
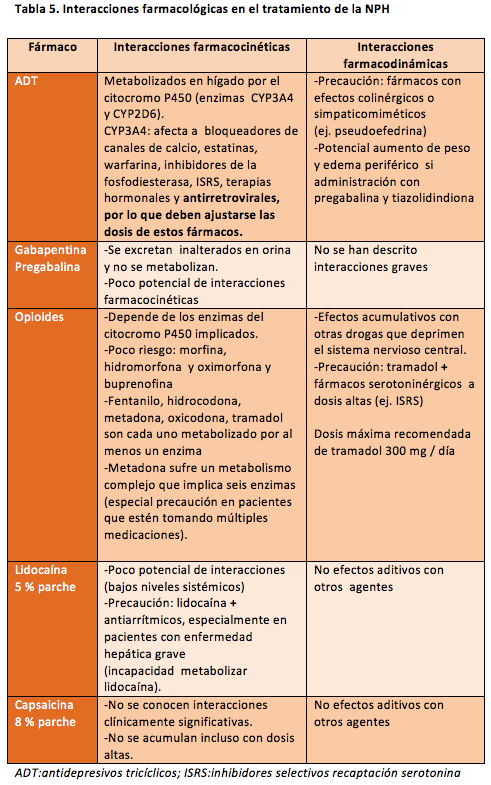
En la Tabla 4 se muestran las recomendaciones para el tratamiento farmacológico del dolor neuropático según una revisión sistemática y metaanálisis publicada en el 2015 por Finnerup et al. (12). La eficacia de los ADT o duales y gabapentinoides está bien establecida. Sin embargo, los efectos adversos asociados a estos fármacos se incrementan en el PCC polimedicado y con afectación de diferentes órganos, presentando un mayor riesgo de interacciones farmacocinéticas y farmacodinámicas (11) (Tabla 5).
Las terapias tópicas son mejor toleradas en estos pacientes y han probado su eficacia en el dolor neuropático localizado característico de la NPH. El parche de capsaícina 8% ha mostrado una mejoría en la escala numérica del dolor >30% a los 3 meses con una sola aplicación (13) y el de lidocaína al 5 % del 36-40% en las escalas del dolor durante 4 semanas de tratamiento con el fármaco (14). Según un reciente estudio pueden existir diferencias en la efectividad en relación al fenotipo del paciente. El bloqueo tópico de los canales de sodio producido por la lidocaína puede ser más eficaz en pacientes con fenotipo “nociceptor irritable” (determinados por test cuantitativos sensoriales) en los que se constató una mayor disminución del dolor paroxístico y del dolor continuo de características profundas (15).
El tratamiento del dolor neuropático, en general, debe basarse en las recomendaciones propuestas por las últimas guías.
Manejo del paciente oncológico inmunodepimido
La mayoría de pacientes con dolor de origen neoplásico que han recibido tratamiento con quimioterapia o radioterapia, o tras cirugía oncológica, requieren un opioide potente.
La mayoria de los opioides poseen efectos inmunomoduladores que se podrían producir tanto a nivel periférico, por interacción con los receptores mu, como a nivel central, puesto que los opioides que cruzan la barrera hematoencefálica son menos inmunosupresores. La morfina puede modular la función inmune a través de varias vías indirectas, como la inducción de corticoesteroides. Si bien este efecto inmunomodulador se ha demostrado con la morfina tanto in vivo como in vitro, varía con otros opioides. Por ejemplo, el efecto es transitorio con el fentanilo e inexistente con la buprenorfina y el tramadol. Aunque no se sabe con certeza si ello es clinicamente relevante, parecería prudente tenerlo en cuenta cuando se requiere un tratamiento a largo plazo. La buprenorfina constituye una buena opción en pacientes previamente inmunodeprimidos por la enfermedad o el tratamiento (16).
Conclusiones
Las comorbilidades asociadas al PCC inmunocomprometido pueden afectar a diferentes órganos, alterando la eficacia o la tolerabilidad de los tratamientos analgésicos y aumentando la vulnerabilidad del paciente a los posibles efectos adversos asociados a éstos. Muchos de estos pacientes tienen más de una comorbilidad, por lo que reciben varios medicamentos (polimedicados) y pueden aparecer interacciones medicamentosas con los analgésicos.
En la mayoría de los casos el dolor está localizado, por lo que la elección de un analgésico tópico puede proporcionar una eficacia adecuada y una mejor tolerabilidad que la terapia sistémica. Sin embargo, para el tratamiento óptimo de estos pacientes, en la mayoría de los casos, será necesario la terapia combinada de varios fármacos con diferentes mecanismos de acción. En este sentido si se requiere un opiode potente recurrir a la buprenorfina de inicio es una opción recomendable.
Una adecuada consideración de la comorbilidad y el cuidado en la selección de medicamentos en el paciente inmunodeprimido con dolor es, por lo tanto, esencial para garantizar una gestión adecuada de la enfermedad con un mínimo de riesgo.
No se ha podido demostrar que los avances dirigidos al tratamiento de la etiología de la enfermedad, como es el caso del tratamiento del virus HIV, provoque necesariamente una mejoría del dolor. El conocimiento de mecanismos centrales inmunes comunes de dolor crónico y sus comorbilidades podría conducir a enfoques de tratamiento más completos y con mejores resultados.
Bibliografía
1. Garrison CJ, Dougherty PM, Kajander KC et al. Staining of glial fibrillary acidic protein (GFAP) in lumbar espinal cord increases following a sciatic nerve constriccion injure. Brain Res 1991;565:1-7.
2. Grace PM, Rolan PE, Hutchinson MR. Peripheral immune contributions to the maintenance of central glial activation underlying neuropathic pain. Brain Behav Inmnun 2011; 25:1322-1332.
3. Parker R, Stein DJ; Jelsman J. Pain in people living with HIV/AIDS: as systematic review of the International AIDS Soc 2014;17:18719
4. Schütz SG, Robinson Papp J. HIV-related neuropathy: corrent perspectives. HIV AIDS (Auckl).2013; 5:243-251.
5. Attal N, Finnerup N. Pharmacological management of neuropathic pain. [webpage on the Internet]. Seattle, WA: International Association for the Study of Pain. Pain: Clinical Updates. Nov 2010 (Volume XVIII, Issue 9). Available from: http://www.iasppain.org/AM/Template.cfm?Section=Clinical_Updates&Template=/TaggedPage/TaggedPageDisplay.cfm&TPLID=5&ContentID=1566.
6. Simpson DM, Brown S, Tobias J. NGX-4010 C107 Study Group. Controlled trial of high-concentration capsaicin patch for treatment of painful HIV neuropathy. Neurology. 2008; 70(24):2305–2313.
7. Clifford DB, Simpson DM, Brown S et al. NGX-4010 C119 Study Group. A randomized, double-blind, controlled study of NGX-4010, a capsaicin 8% dermal patch, for the treatment of painful HIV-associated distal sensory polyneuropathy. J Acquir Immune Defic Syndr. 2012; 59(2):126–133.
8. Hahn K, Arendt G, Braun JS et al. German Neuro-AIDS Working Group. A placebo-controlled trial of gabapentin for painful HIV-associated sensory neuropathies. J Neurol. 2004; 251(10):1260–1266.
9. Simpson DM, Schifitto G, Clifford DB et al. 1066 HIV Neuropathy Study Group. Pregabalin for painful HIV neuropathy: a randomized, double-blind, placebo-controlled trial. Neurology. 2010; 74(5):413–420.
10. Kieburtz K, Simpson D, Yiannoutsos C et al. A randomized trial of amitriptyline and mexiletine for painful neuropathy in HIV infection. AIDS Clinical Trial Group 242 Protocol Team. Neurology. 1998; 51(6): 1682–1688.
11. Bruckenthal P, Barkin RL. Options for treating postherpetic neuralgia in the medically complicated patient. Ther Clin Risk Manag. 2013; 9: 329–340.
12. Finnerup NB, Attal N, Haroutounian S, et al. Pharmacotherapy for neuropathic pain In adults: a systematic review and meta-analysis. Lancet Neurol. 2015;14(2):162-173.
13. Backonja MM, Malan TP, Vanhove GF et al. C102/106 Study Group. NGX-4010, a high-concentration capsaicin patch, for the treatment of postherpetic neuralgia: a randomized, double-blind, controlled study with an open-label extension. Pain Med. 2010; 11(4):600–608
14. Rehm S, Binder A, Baron R. Post-herpetic neuralgia: 5% lidocaine medicated plaster, pregabalin, or a combination of both? A randomized, open, clinical effectiveness study. Curr Med Res Opin. 2010; 26(7): 1607–1619.
15. Demant DT, Lund K, Finnerup NB et al. Pain relief with lidocaine 5% patch in localized peripheral neuropathic pain in relation to pain phenotype. Pain 2015 Jun 18. [Epub ahead of print]
“Twelve Reasons for Considering Buprenorphine as a Frontline Analgesic in the Management of Pain”. Mellar P. Davis. J Support Oncol 2012;10(6):209-219.




