Alrededor del 10% de la población mundial padece una insuficiencia renal crónica (IRC), alcanzando el 50% en la población geriátrica (1).
La mayor parte de pacientes con IRC se pueden enmarcar en el concepto de paciente crónico complejo (PCC) por la dificultad de manejo de su proceso renal debido a las múltiples interacciones ocasionadas por la presencia de las comorbilidades asociadas.
El paciente crónico complejo con IRC. Comorbilidades asociadas
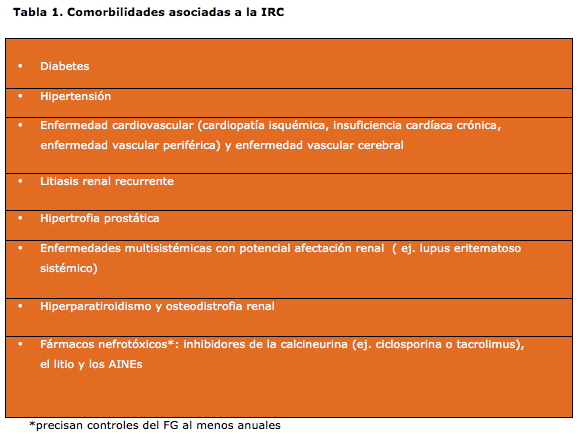
La IRC provoca un incremento importante de la mortalidad que va asociado a las comorbilidades que aparecen a lo largo del proceso (2). (Tabla 1). La monitorización del filtrado glomerular (FG) debe hacerse de forma regular cuando existen estos factores de riesgo.
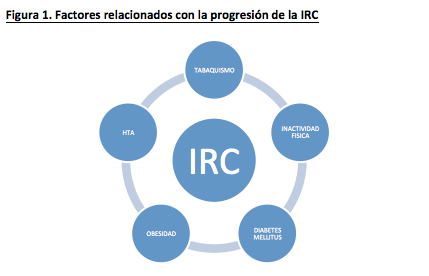
Factores como el estilo de vida, la hipertensión, la nefropatía diabética y el tabaquismo se han relacionado con un aumento de la prevalencia de la IRC. Todos ellos contribuyen a la progresión de la IRC y están correlacionados entre sí (Figura 1). La obesidad podría conducir a la IRC a través de la diabetes y la hipertensión. Del mismo modo, el tabaquismo y la inactividad física contribuyen a la progresión de la IRC. No está claro si estos factores de riesgo pueden también actuar de forma independiente produciendo un efecto directo sobre la IRC o lo hacen de forma indirecta (3).
La IRC puede ser asintomática y no ser diagnosticada hasta fases avanzadas de la enfermedad. Las comorbilidades asociadas, como la patología cardiovascular y la diabetes, incrementan la gravedad y aceleran su progresión.
Tratamiento de la IRC
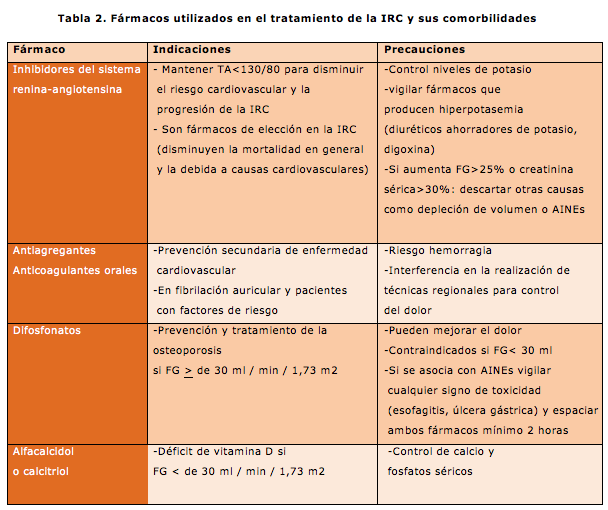
En la Tabla 2 se señalan algunas consideraciones sobre los fármacos utilizados en el tratamiento de la insuficiencia renal y sus comorbilidades.
En el contexto del PCC con insuficiencia renal existen diversas causas que pueden originar dolor. Las más frecuentes son:
- Fracturas por fragilidad ósea desde los primeros estadios de la enfermedad. La incidencia de fractura de cadera aumenta de manera inversa al FG, de forma que en la población en diálisis, al menos un 50%, ha sufrido una fractura por este motivo (4). La osteodistrofia renal se caracteriza por un conjunto de alteraciones sistémicas del metabolismo óseo y mineral que se manifiestan por anormalidades en la resistencia ósea y calcificaciones vasculares. Se acompañan de alteraciones en los niveles de calcio, fósforo, PTH y vitamina D.
- La osteoporosis se asocia a la edad avanzada y a la inmovilidad, una población en la que la insuficiencia renal es extraordinariamente frecuente. Además, los fármacos que se utilizan para su tratamiento deben ser manejados con precaución e incluso pueden estar contraindicados en los estadios avanzados de la enfermedad (Tabla 2).
- Dolor isquémico por enfermedad vascular periférica o angina de pecho
- Dolor central por accidente vascular cerebral
- Alta incidencia de polineuropatía diabética
- Dolor por neuralgia postherpética asociada a la edad y a la comorbilidad
Enfoque del tratamiento del dolor en el PCC con insuficiencia renal
La IRC se define como la pérdida progresiva de la tasa de filtración glomerular expresada por una reducción del aclaramiento de creatinina estimado <60 ml/min/1,73 m2 o por un aumento de la creatinina sérica de más del 20% (3). La función renal en individuos normales disminuye alrededor de 0,75 ml/minuto por año después de la cuarta década de vida. En esta situación deberán ajustarse las dosis de los fármacos según las cifras de filtrado glomerular y el riesgo inherente al fármaco que vamos a administrar.
El manejo del dolor en estos pacientes es complicado porque confluyen diferentes tipos de dolor, muchas veces de elevada intensidad, lo que requerirá introducir una terapia multimodal en un paciente que ya está polimedicado por sus comorbilidades asociadas y que tiene riesgo de toxicidad por su insuficiencia renal.
- AINES
La utilización de AINEs (antiinflamatorios no esteroideos) de forma continuada se puede relacionar con la progresión de la insuficiencia renal. Por tanto, hay que tener especial precaución al tratar a las personas con enfermedad renal crónica con AINEs durante periodos prolongados de tiempo debiéndose monitorizar sus efectos sobre el FG, sobre todo en personas con un FG basal bajo y en presencia de otros riesgos asociados (Tabla 1). Además, estos agentes pueden reducir el efecto de los diuréticos y antihipertensivos por su acción sobre las prostaglandinas renales. Como consecuencia, podría producirse un empeoramiento del control de la tensión arterial, de la función renal y de la sensibilidad a la insulina en pacientes diabéticos.
Los AINE más nefrotóxicos son la indometacina y el fenoprofeno, però potencialmente todos lo son, tanto los llamados COX-1 como COX-2.
- Antidepresivos Tricíclicos
En aquellos pacientes que por su tipo de dolor (dolor neuropático) se deban utilizar los antidepresivos tricíclicos (ADT) es importante considerar sus efectos adversos, especialmente frecuentes en pacientes ancianos: somnolencia, afectación de la capacidad cognitiva, desorientación, constipación, retención urinaria, aumento de peso, arritmias e insuficiencia cardíaca, los cuales pueden deteriorar enormemente la calidad de vida de estas personas. Así mismo, al ser metabolizados en hígado y tener un margen terapéutico estrecho, se recomiendan ajustes de dosis en pacientes de edad avanzada o en los que coexistan enfermedades que se acompañen de un cierto grado de insuficiencia hepática.
A destacar que desipramina y clomipramina deben usarse con precaución en pacientes con IRC (5) por su afectación añadida sobre la función renal.
- Anticonvulsivantes
La gabapentina y la pregabalina aunque no poseen efecto directo sobre la función renal (no son nefrotóxicos) se eliminan principalmente por el riñón, por lo que deben administrarse con precaución en pacientes con aclaramiento de creatinina <60 ml / minuto / m2 y ajustar la dosis según el grado de deterioro de la función renal. En esta población se debe prestar atención a la posible aparición de efectos secundarios como mareos, somnolencia, alteraciones psiquiátricas o edema periférico.
- Opioides
La combinación de los ADT con opioides puede tener efectos aditivos sobre la somnolencia y la motilidad intestinal o vesical. Especial atención con tramadol (el opioide más utilizado según las cifras del CATSALUT) ya que los antidepresivos pueden disminuir su eficacia y aumentar sus efectos secundarios. Si se asocian ISRS (inhibidores selectivos de la recaptación de la serotonina) con tramadol, las dosis elevadas de alguno de los dos fármacos pueden potenciar un síndrome serotoninérgico.
Si el paciente presenta un dolor tanto nociceptivo (el más frecuente) como neuropático de elevada intensidad, debemos plantearnos la utilización de analgésicos potentes como son los opioides y utilizar el que ofrezca mayor seguridad para este tipo de pacientes ya que la mayoría de los opioides se eliminan por la orina. Destacaremos la buprenorfina que se excreta principalmente por vía biliar, por lo que su farmacocinética no se ve afectada en pacientes con deterioro de la función renal pudiéndose administrar, incluso, en los pacientes dializados. Es un opioide agonista parcial, que no produce metabolitos activos, y que presenta un buen perfil de seguridad incluso en pacientes oncológicos con IRC (6). Aunque 1/3 de la buprenofina se metaboliza en el higado por el citocromo P450, no hay datos clínicos relevantes de interacciones con otros fármacos metabolizados por esta misma vía. Además, la buprenofina no se transporta en plasma por la albumina por lo que no compite con los fármacos que sí se transportan por esta proteína, disminuyendo, por tanto, el riesgo de sobredosificación. Esto representa una ventaja, principalmente en pacientes crónicos polimedicados. Por otra parte, posee un efecto techo en relación a la depresión respiratoria, lo que representa un ventaja en los ancianos.
La metadona no se excreta por la orina pero no se recomienda como tratamiento de primera línea, sobre todo en pacientes de edad avanzada y polimedicados porque tiene un índice terapéutico estrecho y una farmacocinética muy variable. La morfina, hidromorfona, y tramadol producen metabolitos activos que pueden acumularse en insuficiencia renal y provocar efectos neuroexcitadores (convulsiones, alodinia, mioclonus) (7). El fentanilo no posee metabolitos activos relevantes pero a diferencia de la buprenorfina se elimina vía renal.
Cuando iniciemos el tratamiento con opioides potentes en estos pacientes, siempre debe ser titulando muy bien la dosis necesaria, es decir, siempre se debe iniciar el tratamiento con dosis muy bajas e ir aumentando en función de los beneficios obtenidos (analgesia vs efectos adversos). Debemos también informar al paciente y familiares de los posibles efectos secundarios que puedan aparecer y anteponernos a ellos.
- Tratamientos tópicos
Otro tipo de tratamiento a tener en cuenta en estos pacientes, cuando presentan un dolor neuropático localizado (neuralgia postherpética, lesiones nerviosas postquirúrgicas, dolor postoracotomía… ), es la via tópica relegada a la segunda opción de tratamiento por las guías más actualizadas de dolor neuropático (8).
Los dos tratamientos de que disponemos son la capsaicina a dosis altas en parche y la lidocaina al 5% en apósito (con indicación en neuralgia postherpética).
La acción de capsaicina 8% se produce en 2 fases: una excitatoria, mediante su unión al receptor TRVP1, provocando una liberación y depleción de la sustancia P, y una fase posterior de desensibilización de estos receptores e incapacidad para responder a los estímulos que provocan dolor. La primera fase es dolorosa, por lo que la aplicación del parche debe hacerse en medio hospitalario, tras la administración de un anestésico local tópico o un analgésico endovenoso (el tramadol se ha mostrado eficaz). Su acción es transitoria y las terminaciones nerviosas se recuperan en 2-3 meses, por lo que el tratamiento puede repetirse cada 3-4 meses en función de los síntomas del paciente, aunque su seguridad a largo plazo todavía no está bien establecida. El dolor y eritema que provoca pueden limitar su indicación en pacientes cardiópatas e hipertensos inestables.
La eficacia y la tolerabilidad de la lidocaína 5 % en apósitos se han confirmado en estudios a largo plazo en el tratamiento del dolor neuropático en pacientes de edad avanzada con múltiples comorbilidades y politratados (9). El parche está indicado en adultos con neuralgia postherpética.
En pacientes con NPH y polineuropatía diabética, al comparar la lidocaína al 5% en parche y la pregabalina, se objetiva un mejor perfil de eficacia/seguridad para el paciente en el grupo de lidocaína al 5%, así como una mejoría de su satisfacción y del test de calidad de vida (10).
En la última revisión sistemática de la farmacoterapia en el dolor neuropático, publicada en febrero de 2015, Finnerup et al. consideran los tratamientos tópicos como fármacos de segunda línea en el tratamiento del dolor neuropático periférico (8).
Los niveles sistémicos de lidocaína alcanzados son bajos y por tanto no presenta efectos aditivos con otros agentes. Sólo es necesario tener precaución en pacientes que reciban concomitantemente lidocaína y antiarrítmicos, especialmente en pacientes con enfermedad hepática grave, que tienen una incapacidad para metabolizar la lidocaína (5).
La IRC puede influir en la selección de un tratamiento de primera línea (ADT o duales y gabapentina/pregabalina) o provocar un cambio de un tratamiento de primera línea a una terapia de segunda o tercera línea (tratamientos tópicos, opioides). La Tabla 3 refleja el riesgo relativo de los fármacos administrados para el tratamiento del dolor cuando existe deterioro de la función renal.

La experiencia acumulada en estos pacientes es que el dolor más frecuente es el osteomuscular y el tratamiento debe ser multimodal si el dolor es de elevada intensidad. Es por ello que la vía tópica debe ser utilizada en combinación con otros fármacos analgésicos más potentes como serían los opioides. Este enfoque multimodal permitiría disminuir las dosis de los fármacos analgésicos obteniendo resultados satisfactorios de riesgo/beneficio.
Conclusiones
El paciente crónico con insuficiencia renal requerirá tratamientos complejos y prolongados, tanto para sus comorbilidades como para el control del dolor asociado a éstas. El manejo del dolor debe hacerse de forma cuidadosa siendo necesario monitorizar su intensidad y los signos de toxicidad.
Los pacientes con insuficiencia renal tienen un riesgo de fracturas y osteoporosis aumentado. Además, la mayoría presentan dolor de diversas etiologías y características, como neuropatía diabética, dolor anginoso, dolor isquémico por arteriopatía obliterante o dolor de origen central debido a accidentes vasculares.
Se deberá prestar especial atención a las interacciones medicamentosas, así como al riesgo de toxicidad en un paciente polimedicado ligado al deterioro de la función renal y al riesgo de progresión de la insuficiencia renal asociado a determinados analgésicos, como los AINEs. Los efectos secundarios más frecuentes producidos por los analgésicos, especialmente sedación, náuseas, mareos y estreñimiento, limitan la adherencia al tratamiento y crean un desequilibrio entre la analgesia, la tolerabilidad, la funcionalidad y la recuperación. Un esquema de tratamiento combinando la vía tópica con la sistémica a fin de poder disminuir dosis y mejorar la tolerabilidad se considera particularmente útil en estos pacientes, sobre todo en los de edad avanzada.
Bibliografía
1. F. Aucella. Epidemiologic and clinical challenges of geriatric nephrology .J Nephrol. 2010; 23: S1-S4.
2. Luis Arboleya.Trastorno mineral y óseo asociado a la enfermedad renal crónicaReumatol Clin.2011; 7 Supl 2:18-21.
3. National Clinical Guideline Centre (NICE) Clinical Guideline 182. Methods, evidence and recommendations July 2014. Chronic kidney disease (partial update). Early identification and management of chronic kidney disease in adults in primary and secondary care.
4. Dooley AC, Weiss NS, Kestenbaum B. Increased risk of hip fracture among men with CKD. Am J Kidney Dis. 2008;51:38–44.
5. Bruckenthal P, Barkin RL. Options for treating postherpetic neuralgia in the medically complicated patient. Therapeutics and Clinical Risk Management 2013; 9: 329-340.
6. Melilli G, Samolsky D BG, Frenquelli C. et al. Transdermal opioids for cancer pain control in patients with renal impairment. J Opioid Mang 2014;10(2):85-93.
7. Smith H, Bruckenthal P. Implications of opioid analgesia for medically complicated patients. Drugs Aging. 2010; 27(5): 417–433.
8. Finnerup NB, Attal N, Haroutounian S, et al. Pharmacotherapy for neuropathic pain In adults: a systematic review and meta-analysis. Lancet Neurol. 2015;14(2):162-173.
9. Clère F, Delorme-Morin C, George B et al. 5% lidocaine medicated plaster in elderly patients with postherpetic neuralgia. Result of a compassionate use program in France. Drugs Aging. 2011; 28(9): 693–702.
10. Devers A, Galer BS. Topical lidocaine patch relieves a variety of neurophatic pain conditions: an open-labelstudy. Clin J Pain. 2000;16(3):205-208.




