Redacción Farmacosalud.com
La compañía Pfizer ha anunciado que la vacuna Comirnaty (Pfizer/BioNTech) es segura y parece inducir una robusta respuesta inmune en un ensayo clínico que ha incluido a niños de 5 a 11 años, y en el que se han utilizado esquemas de vacunación de dos dosis de 10 microgramos (µg) administradas con un intervalo de 3 semanas. Se prevé que esta cantidad sea de 3 µg en los estudios centrados en menores de 5 años. El preparado Comirnaty ya comercializado para adolescentes y adultos contiene 30 µg. La respuesta inmune y los efectos adversos observados en menores de 12 años han sido similares a los encontrados en adolescentes y jóvenes, informa la Asociación Española de Vacunología (AEV). Todo parece indicar que los buenos resultados obtenidos con el suero abren las puertas a la vacunación masiva frente al COVID-19 en menores de 12 años de edad.
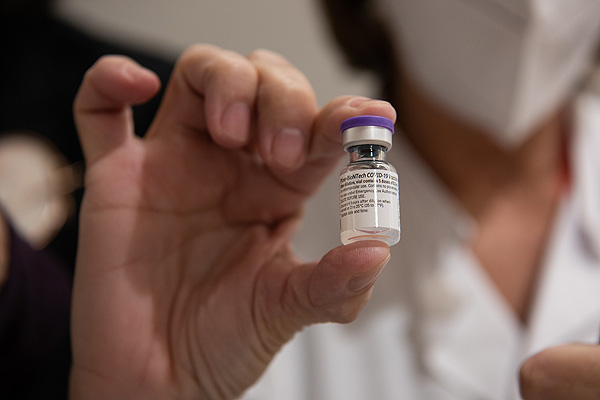
Vacunación frente al COVID-19
Autor/a de la imagen: Oriol Martí - Hospital Clínic
Fuente: Hospital Clínic de Barcelona (IMAGEN DE ARCHIVO)
“Yo creo que es una buena noticia porque hasta ahora sólo disponíamos de vacunas frente al COVID-19 a partir de los 12 años de edad. Por tanto, se incorpora una nueva franja etaria, en concreto de 5 a 11 años”, apunta el Dr. Fernando Moraga-Llop, pediatra y vicepresidente de la AEV. El nuevo estudio se ha centrado en población pediátrica de entre 6 meses y 11 años, que a su vez ha sido dividida en tres subgrupos, de tal modo que en esta primera comunicación se han difundido los resultados del grupo con edades comprendidas entre los 5 y los 11 años.
Para que la vacuna pueda ser comercializada para esta franja etaria pediátrica, debe seguirse la ruta que recorre cualquier fármaco para su autorización: que los datos del ensayo sean publicados en una revista científica y posteriormente analizados por las agencias reguladoras de medicamentos, y que, finalmente, se confirmen los buenos resultados obtenidos en el estudio. Es decir, habrá que verificar que el preparado vacunal es seguro y que aporta una buena inmunogenicidad (propensión de un medicamento a inducir una respuesta inmunitaria frente a él mismo, lo que en vacunas es lo pertinente), es decir, que hay una importante respuesta en forma de anticuerpos neutralizantes del coronavirus SARS-CoV-2.
Con todo, no hay datos de eficacia
Ahora bien, el nuevo ensayo no ha aportado datos de eficacia, tal y como puntualiza el Dr. Moraga-Llop: “La respuesta en forma de anticuerpos neutralizantes ha sido muy importante, similar a la observada en el grupo etario de 16 a 25 años. Esto ya nos está indicando una gran respuesta inmunogénica y nos permite inferir que la vacuna va a tener una eficacia similar a la ya vista en otros grupos de edad. Con todo, cabe destacar que este estudio clínico no ha permitido sacar datos de eficacia porque no ha habido suficientes casos de infección COVID… hay que tener en cuenta que, de los más de 4.000 niños participantes, sólo la mitad (algo más de 2.000) pertenecían al grupo etario de 5 a 11 años. A su vez, de esos más de 2.000, dos tercios se han vacunado y un tercio han recibido placebo”.
No obstante, el ensayo sí ha permitido ver, en comparación con el grupo de 16 a 25 años, que es un suero seguro y que tiene una buena tolerabilidad. Los eventos adversos detectados han sido los mismos que los observados en el segmento adolescente y joven (fiebre, dolor de cabeza, cansancio, dolor articular y muscular…) “En todo caso, son efectos secundarios leves que se autolimitan”, remarca el pediatra.
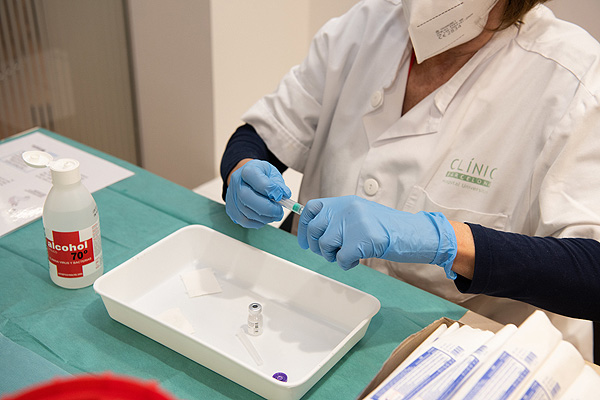
Vacunación frente al COVID-19
Autor/a de la imagen: Oriol Martí - Hospital Clínic
Fuente: Hospital Clínic de Barcelona (IMAGEN DE ARCHIVO)
Así las cosas, todo parece indicar que se han puesto las bases para que el preparado de Pfizer/BioNTech dé lugar a una vacunación masiva en menores de 12 años. “En base a esas dos premisas -que es una vacuna segura y con una gran respuesta inmunogénica-, si la valoración riesgo-beneficio es positiva, y dependiendo del momento en que se encuentre la pandemia, en efecto, sería una vacuna a poner en esos niños”, sostiene el vicepresidente de la AEV. La decisión sobre su comercialización para tales edades pediátricas podría llegar a finales de año o a principios del 2022.
¿Las vacunas no basadas en ARNm también pueden funcionar en menores de 12 años?
En el ensayo han participado niños de los Estados Unidos, Finlandia, Polonia y España. Pfizer espera remitir el correspondiente dossier a la FDA (Agencia del Medicamento de Estados Unidos) a finales de este mes de septiembre. Adicionalmente, espera disponer de resultados del suero en los menores de 6 meses a 5 años para finales de octubre, según agregan desde la AEV.
La vacuna de Pfizer/BioNTech, igual que la de Moderna, se basa en un suero de ARN mensajero (ARNm). Otros preparados, como los de Janssen de Johnson & Johnson y AstraZeneca, están basados en un vector viral. En este sentido, Moraga-Llop señala que al menos en Janssen se están llevando a cabos ensayos en menores de 12 años. Asimismo, explica que la vacuna CoronaVac, de origen chino y con un mecanismo de virus inactivado, y la vacuna Soberana 02, un preparado conjugado con toxoide tetánico desarrollado en Cuba, ya tienen indicación pediátrica para menores de corta edad.
El suero vacunal antiCOVID protege a los pacientes con cáncer
Por otro lado, una investigación revela que las personas con cáncer tienen una respuesta inmune protectora adecuada a la vacunación frente al COVID-19 sin experimentar más efectos secundarios que la población general, según se ha conocido en el Congreso anual de la Sociedad Europea de Oncología Médica (ESMO Congreso 2021).
Personal sanitario trabajando en plena pandemia
Fuente: Francisco Avia / Hospital Clínic (IMAGEN DE ARCHIVO)
La evidencia indirecta sugiere, además, que una tercera inyección de refuerzo podría aumentar aún más el nivel de protección entre esta población de pacientes.
Los hospitalizados por COVID-19 y con inmunosupresión, con más riesgo de evolución grave
Un trabajo retrospectivo del Registro SEMI-COVID-19 de la Sociedad Española de Medicina Interna (SEMI) que analiza datos de 13.206 pacientes, recogidos durante la primera ola de COVID-19, concluye que los enfermos con inmunosupresión ─trasplantados de órgano sólido, con distintos tipos de neoplasias (cáncer) o bajo tratamiento crónico con diversos fármacos inmunosupresores─ que han sido hospitalizados por COVID-19 presentan mayor riesgo de muerte y de complicaciones graves que los ingresados por infección por SARS-CoV-2 sin inmunosupresión.
El estudio, liderado por las Dras. Isabel Perales Fraile e Inés Suárez García, médicas internistas de la SEMI, ha sido publicado en PLOS ONE bajo el título ‘In-hospital mortality among immunosuppressed patients with COVID-19: analysis from a national cohort in Spain’. En el trabajo se describen y analizan, de forma comparativa, las características clínicas y el pronóstico de una amplia cohorte de pacientes españoles hospitalizados por COVID-19, con y sin inmunosupresión. Se trata de la serie más grande publicada hasta el momento de sujetos con cáncer, trasplantados e inmunosuprimidos ingresados por esta infección.
Los pacientes con inmunosupresión tenían mayor edad, mayor frecuencia de hábito tabáquico, mayor presencia de enfermedades crónicas (hipertensión arterial, insuficiencia cardiaca, enfermedad pulmonar obstructiva crónica, diabetes mellitus, enfermedad hepática o renal) y mayor comorbilidad medida por el índice de Charlson.

Asistencia prestada durante la crisis del coronavirus
Fuente: Francisco Avia / Hospital Clínic (IMAGEN DE ARCHIVO)
La tasa de mortalidad en individuos hospitalizados por COVID-19 fue muy alta, tanto entre inmunodeprimidos como no inmunodeprimidos (31.3% y 19.3%, respectivamente), lo que refleja la situación sanitaria y la edad avanzada de los pacientes ingresados por COVID-19 en la primavera de 2020 en España. La tasa de letalidad, frecuencia de complicaciones y duración de la estancia hospitalaria siguió siendo significativamente mayor entre los inmunodeprimidos tras el ajuste por los factores de riesgo asociados a COVID-19 grave.
Sin más mortalidad en operados de urgencia con coronavirus
Por último, un amplio estudio llevado a cabo en 25 hospitales de España, y que han coordinado especialistas del Hospital Universitario de Bellvitge y el IDIBELL (l’Hospitalet de Llobregat, en Barcelona), ha demostrado que las personas con COVID-19 operadas de urgencia de cirugía general y digestiva no tienen una mayor mortalidad por haberse contagiado con el coronavirus SARS-CoV-2.
Esta investigación, que ha publicado la prestigiosa revista científica ‘British Journal of Surgery’, matiza las conclusiones de trabajos anteriores puramente descriptivos en los que se había constatado que las personas operadas y con infección por COVID-19 presentan una mortalidad muy superior a la habitual. Estos datos habían llevado a algunos expertos a recomendar retrasar o evitar las cirugías en pacientes positivos de SARS-CoV-2 siempre que fuese posible.




