Redacción Farmacosalud.com
Llega a España la nueva y cuarta indicación de SKYRIZI® (risankizumab), en este caso para tratar la colitis ulcerosa (CU). De acuerdo con los resultados de los ensayos clínicos, risankizumab logra, tras un año de tratamiento, que aproximadamente el 40% de los pacientes alcancen la remisión clínica de la enfermedad, una tasa de respuesta “muy alta” si se tiene en cuenta que la mayoría de los participantes en los estudios “venían de haber fracasado a múltiples tratamientos”, por lo que eran pacientes que presentaban una CU “más grave de lo habitual”, argumenta el Dr. Federico Argüelles Arias, jefe de la Sección de Digestivo del Hospital Universitario Virgen Macarena y Prof. de la Facultad de Medicina de Sevilla. En paralelo, se ha podido comprobar que alrededor del 50% de los enfermos alcanzan la curación mucosa.
La indicación de risankizumab se centra en el tratamiento de adultos con colitis ulcerosa activa de moderada a grave que han tenido una respuesta inadecuada, han perdido respuesta o han sido intolerantes al tratamiento convencional o a un fármaco biológico, informa la compañía AbbVie. De esta forma, risankizumab constituye el primer inhibidor selectivo de la IL-23 aprobado tanto en CU como en enfermedad de Crohn, las dos formas de la Enfermedad Inflamatoria Intestinal (EII)1.

Autor/a: de la imagen mikesaran
Fuente: depositphotos.com
Eficaz frente a la urgencia intestinal, incontinencia fecal, dolor abdominal…
Risankizumab, asimismo, se ha mostrado eficaz en varios indicadores PRO (resultados informados por el paciente): frente a urgencia intestinal, incontinencia fecal, dolor abdominal, tenesmo (sensación de tener que defecar aunque el intestino esté vacío) y frente a la necesidad de realizar deposiciones nocturnas. También se ha observado su utilidad a la hora de controlar la fatiga, el cansancio y las interrupciones del sueño. El nuevo fármaco, además, se asocia a un control sintomático precoz, ya que, con la primera administración, el paciente ya nota beneficios en su calidad de vida.
Risankizumab, que está financiado por la sanidad pública española, cuenta además con indicación en España para la psoriasis en placas, artritis psoriásica y enfermedad de Crohn. Por otra parte, la aprobación de esta terapia se acompaña de una extensión de línea que incluye una nueva presentación: Skyrizi 180 mg solución inyectable en cartucho a través de un autoinyector corporal, de manera que es el propio enfermo quien se autoadministra el tratamiento. A este respecto, el Dr. Argüelles señala que la autoadministración subcutánea de risankizumab se puede realizar en casa y por tanto “ahorra al paciente desplazamientos al hospital”, lo que, “desde mi punto de vista, es un avance muy importante. Otro avance es que este medicamento se tiene que administrar una vez cada dos meses, con lo cual el paciente se olvida durante dos meses por completo del fármaco”. Además, la autoaplicación de risankizumab es “muy fácil” de llevar a cabo, agrega.
Menor uso de los recursos del sistema sanitario público
A juicio de Luis Nudelman, director médico de AbbVie España, la autoadministración de risankizumab “no solamente refuerza y mejora la adherencia al tratamiento, sino que también redunda en un beneficio para el sistema sanitario español”, por cuanto que el paciente “requiere ir menos a la consulta” y, por lo tanto, hay un menor “uso de recursos del sistema sanitario público”. La eficacia de risankizumab también comporta que haya “menos hospitalizaciones” y menos intervenciones quirúrgicas, entre otras ventajas tanto para los afectados de CU como para la Administración, añade Nudelman.

Luis Nudelman (a la izq. de la imagen) y Dr. Federico Argüelles
Fuente: AbbVie / Torres y Carrera
La colitis ulcerosa es una enfermedad inflamatoria del tracto gastrointestinal que afecta al intestino grueso2,3. Se estima que más de 5 millones de personas en el mundo tienen CU4, una afección que se caracteriza por ser heterogénea, idiopática, crónica y sistemática y que genera un alto impacto en la calidad de vida2,5,6. Los individuos con enfermedad activa pueden acudir más de 20 veces al baño al día; el 40% padecen fatiga y 6 de cada 10 sufren insomnio2,7,8.
“Al tratarse de una patología crónica, es fundamental seguir ampliando el arsenal terapéutico y garantizar que tanto los pacientes como los profesionales sanitarios dispongan de opciones innovadoras y adaptadas a sus necesidades específicas y que, además, tales opciones sean plenamente compatibles con su calidad de vida. Fruto de nuestro compromiso con los pacientes, en AbbVie llevamos más de 20 años estando cerca de las personas con Enfermedad Inflamatoria Intestinal. En esta línea, en el último año y medio, hemos realizado 4 lanzamientos para gastroenterología”, destaca Nudelman.
La autorización de risankizumab está fundamentada en datos de dos ensayos clínicos de fase III, un estudio de inducción (INSPIRE9) y uno de mantenimiento (COMMAND10). Esos estudios incluyen como objetivos primarios la remisión clínica; en el caso del estudio INSPIRE en la semana 12 y en el estudio COMMAND en la semana 52. El nuevo fármaco de AbbVie también cumplió con los criterios de valoración secundarios clave, incluida la curación mucosa y la curación mucosa histologico-endoscópica.
Curación mucosa: ausencia de úlceras en el tracto intestinal
La curación mucosa se define como la ausencia de úlceras en la mucosa del tracto intestinal tras evaluación endoscópica. Alcanzarla se asocia con una mejora del pronóstico de los enfermos y el control de la afección a largo plazo11. En caso contrario, si no se logra, se pueden producir consecuencias significativas al aumentar el riesgo de hospitalizaciones y colectomía12-15 (extirpación o resección de una parte del intestino grueso).
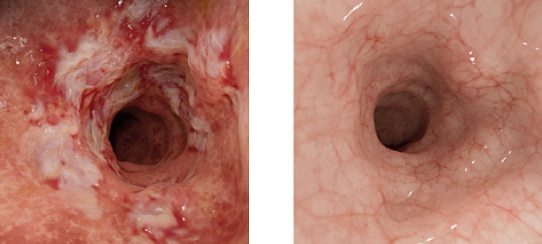
Comparación visual entre un intestino que no ha alcanzado curación mucosa (a la izq. de la imagen) con otro que sí ha logrado este objetivo terapéutico
Difusión: AbbVie / Torres y Carrera
Más allá de los buenos datos recogidos en lo concerniente a los indicadores PROs16,17, cabe decir que el perfil de seguridad de risankizumab en CU es consistente con la experiencia y perfil ya conocido en otras indicaciones ya aprobadas (psoriasis, artritis psoriásica y enfermedad de Crohn)9,10. La dosis recomendada en la indicación de CU de moderada a grave es de 1.200 mg administrados por perfusión intravenosa en la semana 0, semana 4 y semana 8 de tratamiento, y 180 mg o 360 mg administrados por vía subcutánea cada 8 semanas, a partir de la semana 12 de tratamiento1.
La colitis ulcerosa provoca una inflamación continua de la mucosa que se extiende, en diversa medida, desde el recto hasta las zonas más proximales del colon2,18. Su aparición es más frecuente en adultos jóvenes (15-30 años)2. Según un reciente estudio internacional19, más del 40% de los afectados por la CU en España no alcanzan el control de una patología que también se caracteriza por ser limitante para la persona que la sufre. “La colitis ulcerosa no afecta de la misma manera a todos los pacientes, no todos responden a los mismos fármacos, ni todos ellos la viven de la misma forma, lo que evidencia la necesidad de contar con un abanico suficientemente grande de opciones terapéuticas que permita elegir la mejor terapia para cada paciente, especialmente cuando la enfermedad avanza”, subraya Argüelles.
Además de síntomas intestinales como diarrea, dolor abdominal, sangrado rectal o tenesmo, la CU también puede afectar a otros órganos. Así, hasta un tercio de los pacientes experimentan manifestaciones extraintestinales (MEIs), como las que inciden en las articulaciones o la piel2,5,6. “La colitis ulcerosa también induce depresión y ansiedad, siendo estos los trastornos psiquiátricos más frecuentes en sujetos con esta dolencia. Las interrupciones del sueño también forman parte de la CU, estando presentes en hasta 6 de cada 10 pacientes con enfermedad activa. Incluso el 40% de las personas con CU informan de fatiga2,8”, prosigue el jefe de Sección de Digestivo del Hospital Virgen Macarena.

Autor/a: lenecnikolai
Fuente: depositphotos.com
Directrices STRIDE-II: objetivos terapéuticos más exigentes
Asimismo -remarca el Dr. Argüelles-, la cronicidad de la afección “agudiza esta carga emocional, hasta el punto de que al 71% de los pacientes les preocupa, y mucho, cuándo y cómo de grave, será su próximo brote de CU20. Estas cifras reflejan el impacto que tiene dicha patología en la calidad de vida, un aspecto que se confirma al contar con estudios que relacionan directamente un control no adecuado de la enfermedad con una menor calidad de vida”. Por este motivo, aunque el abordaje de la CU se ha centrado históricamente en controlar los síntomas y evitar la aparición de complicaciones o brotes21, actualmente, tal y como se recoge en las directrices STRIDE-II*, los objetivos terapéuticos han evolucionado hasta abarcar propósitos más exigentes. De esta forma, las guías señalan que alcanzar la curación endoscópica (también llamada curación mucosa) es un objetivo central del tratamiento a largo plazo.
* Las guías de STRIDE-II son actualizaciones de las recomendaciones de STRIDE previas iniciadas por la Organización Internacional para el Estudio de las Enfermedades Inflamatorias Intestinales (IOIBD, por sus siglas en inglés). En ellas se definen objetivos de tratamiento razonables a corto, medio y largo plazo para pacientes con EII13
“A pesar de que tradicionalmente el abordaje se centra, entre otros aspectos, en el control de los síntomas, es importante que tengamos en cuenta que la ausencia de los mismos no siempre ha de implicar que no haya actividad inflamatoria, pues también se puede producir inflamación persistente silente (sin síntomas), con los riesgos que ello conlleva”, indica el facultativo.
INSPIRE es un estudio de inducción, multicéntrico, aleatorizado, doble ciego y controlado con placebo cuyo objetivo primario era el de establecer qué proporción de pacientes alcanzaban la remisión clínica según la puntuación Mayo adaptada (aMS) en la semana 12. COMMAND es un estudio de mantenimiento, multicéntrico, aleatorizado, doble ciego y controlado con placebo que tenía como objetivo primario verificar la proporción de pacientes que alcanzaban la remisión clínica según la puntuación aMS en la semana 52.
Risankizumab es un inhibidor de la interleucina-23 (IL-23) que bloquea de manera selectiva la IL-23 uniéndose a la subunidad p19. Se piensa que la IL-23, una citocina involucrada en los procesos inflamatorios, está ligada a diversas enfermedades crónicas mediadas por el sistema inmune22-24.
Referencias
1. EPAR. Risankizumab, 2024. Disponible en: https://www.ema.europa.eu/es/documents/product-information/skyrizi-epar-product-information_es.pdf
2. Gajendran, M., Loganathan, P., Jimenez, G., Catinella, A. P., Ng, N., Umapathy, C., Ziade, N., & Hashash, J. G. (2019). A comprehensive review and update on ulcerative colitis,. Disease-a-Month, 65(12), 100851. https://doi.org/10.1016/j.disamonth.2019.02.004
3. Crohn’s & Colitis Foundation of America. The Facts about Inflammatory Bowel Diseases. Crohn’s & Colitis Foundation. Published 2014. Acceso enero 2025. Disponible en: https://www.crohnscolitisfoundation.org/sites/default/files/2019-02/Updated%20IBD%20Factbook.pdf;
4. Le Berre, C., Honap, S., & Peyrin-Biroulet, L. (2023). Ulcerative colitis. The Lancet, 402(10401), 571–584. https://doi.org/10.1016/S0140-6736(23)00966-2
5. Ordás, I., Eckmann, L., Talamini, M., Baumgart, D. C., & Sandborn, W. J. (2012). Ulcerative colitis. The Lancet, 380(9853), 1606–1619. https://doi.org/10.1016/S0140-6736(12)60150-0
6. Ungaro, R., Mehandru, S., Allen, P. B., Peyrin-Biroulet, L., & Colombel, J.-F. (2017). Ulcerative colitis. The Lancet, 389(10080), 1756–1770. https://doi.org/10.1016/S0140-6736(16)32126-2
7. ACCU España. ¿Te imaginas trabajando con alguien que arrastra una Historia Invisible? Disponible en https://accuesp.com/lahistoriainvisible/
8. Barberio, B., Zamani, M., Black, C. J., Savarino, E. V, & Ford, A. C. (2021). Prevalence of symptoms of anxiety and depression in patients with inflammatory bowel disease: a systematic review and meta-analysis. The Lancet Gastroenterology & Hepatology, 6(5), 359–370. https://doi.org/10.1016/S2468-1253(21)00014-5
9. Louis, Edouard MD1; Panaccione, Remo MD2; Parkes, Gareth MD3; Peyrin-Biroulet, Laurent MD4; Ferrante, Marc MD5; Takeuchi, Ken MD, PhD6; Siegmund, Britta MD, PhD7; Levine, Phillip MD8; Kalabic, Jasmina MD9; Neimark, Ezequiel MD8; Wallace, Kori MD8; Chen, Su PhD8; Duan, W.Rachel MD8; Armuzzi, Alessandro MD10; Biedermann, Luc MD11; Loftus, Edward V. MD12,*; Melmed, Gil MD, MS13; Schreiber, Stefan MD14. S845 Risankizumab Induction Therapy in Patients With Moderately to Severely Active Ulcerative Colitis: Efficacy and Safety in the Randomized Phase 3 INSPIRE Study. The American Journal of Gastroenterology 118(10S):p S624-S625, October 2023. | DOI: 10.14309/01. ajg.0000953020.05891.05
10. Schreiber, S., Panaccione, R., Parkes, G., Peyrin-Biroulet, L., Ferrante, M., Hisamatsu, T., Siegmund, B., Kalabic, J., Levine, P., Neimark, E., Chen, S., Cheng, L., Duan, W. R., Armuzzi, A., Biederman, L., Loftus, E., Melmed, G., & Louis, E. (2024). OP06 Risankizumab Maintenance Therapy in Patients With Moderately to Severely Active Ulcerative Colitis: Efficacy and Safety in the Randomised Phase 3 COMMAND Study. Journal of Crohn’s and Colitis, 18(Supplement_1), i10–i12. https://doi.org/10.1093/ecco-jcc/jjad212.0006
11. Ungaro, R., Mehandru, S., Allen, P. B., Peyrin-Biroulet, L., & Colombel, J.-F. (2017). Ulcerative colitis. The Lancet, 389(10080), 1756–1770. https://doi.org/10.1016/S0140-6736(16)32126-2
12. Turner D, Ricciuto A, Lewis A, et al; International Organization for the Study of IBD. STRIDE-II: an update on the selecting therapeutic targets in inflammatory bowel disease (STRIDE) initiative of the International Organization for the Study of IBD (IOIBD): determining therapeutic goals for treatto-target strategies in IBD. Gastroenterology. 2021;160(5):1570-1583. doi:10.1053/ j.gastro. 2020.12.031
13. Barreiro-de Acosta, M., Molero, A., Artime, E., Díaz-Cerezo, S., Lizán, L., de Paz, H. D., & Martín-Arranz, M. D. (2023). Epidemiological, Clinical, Patient-Reported and Economic Burden of Inflammatory Bowel Disease (Ulcerative colitis and Crohn’s disease) in Spain: A Systematic Review. Advances in Therapy, 40(5), 1975–2014. https://doi.org/10.1007/s12325-023-02473-6
14. Fumery, M., Singh, S., Dulai, P. S., Gower-Rousseau, C., Peyrin-Biroulet, L., & Sandborn, W. J. (2018). Natural History of Adult Ulcerative Colitis in Population-based Cohorts: A Systematic Review. Clinical Gastroenterology and Hepatology, 16(3), 343-356.e3. https://doi.org/10.1016/j. cgh.2017.06.016
15. Shah, S. C., Colombel, J.-F., Sands, B. E., & Narula, N. (2016). Mucosal Healing Is Associated With Improved Long-term Outcomes of Patients With Ulcerative Colitis: A Systematic Review and Meta-analysis. Clinical Gastroenterology and Hepatology, 14(9), 1245-1255.e8. https://doi.org/10.1016/j.cgh.2016.01.015
16. Siegel, CA., Rubin, DT., Panaccione, R., Rieder, F., Takeuchi,K., Hecht, PM., Levine, P., Sanchez Gonzalez, Y., Zhang, Y., Vladea, RC., Biedermann, L., Wu K. (2024). Su1770 Effect of Risankizumab on Early Symptoms in Patients With Moderately to Severely Active Ulcerative Colitis: A Post-hoc Analysis of the INSPIRE Induction Study. Presented at Digestive Disease Week (DDW) 2024,Washington, DC, USA.
17. Panés, J., Loftus Jr., E. V, Armuzzi, A., Siegmund, B., Sands, B. E., Boland, B. S., Kalabic, J., Lai, J. H., Sharma, D., Remple, V., Sanchez Gonzalez, Y., & Lindsay, J. O. (2024). P862 Effects of induction and maintenance therapy with risankizumab on health-related quality of life outcomes in patients with moderately to severely active ulcerative colitis: A post-hoc analysis of Phase 2b/3 trials. Journal of Crohn’s and Colitis, 18(Supplement_1), i1596– i1597. https://doi.org/10.1093/ecco-jcc/jjad212.0992
18. Crohn’s & Colitis Foundation of America. The Facts about Inflammatory Bowel Diseases. Crohn’s & Colitis Foundation. Published 2014. Acceso enero 2025. Disponible en: https://www.crohnscolitisfoundation.org/sites/default/files/2019-02/Updated%20IBD%20Factbook.pdf;
19. Vega P, Huguet JM, Gómez E, Rubio S, Suarez P, Vera MI, Paredes JM, Hernández-Camba A, Plaza R, Mañosa M, Pajares R, Sicilia B, Madero L, Kolterer S, Leitner C, Heatta-Speicher T, Michelena N, Santos de Lamadrid R, Dignass A, Gomollón F. IBD-PODCAST Spain: A Close Look at Current Daily Clinical Practice in IBD Management. Dig Dis Sci. 2024 Mar;69(3):749-765. doi: 10.1007/s10620-023-08220-9. Epub 2024 Jan 13. PMID: 38217680; PMCID: PMC10960747.
20. Monstad I, et al. Clinical course and prognosis in ulcerative colitis: results from population-based and observational studies. Ann Gastroenterol. 2014;27(2):95-104.
21. https://telecumple.educainflamatoria.com/programa1?_ga=2.70683411.2082581375.1626359893-1643799869.1623327291 Consultado en enero de 2025
22. Zwiers A,Kraal L, van de Pouw Kraan TCTM, Wurdinger T, Bouma G, Kraal G. Cutting edge: a variant of the IL-23R gene associated with inflammatory bowel disease induces loss of microRNA regulation and enhanced protein production. J Immunol. 2012;188(4):1573-1577. doi:10.4049/jimmunol.1101494;
23. Duvallet E, Semerano L, Assier E, Falgarone G, Boissier MC. Interleukin-23: A key cytokine in inflammatory diseases. Ann Med. 2011;43(7):503-511. doi:10.3109/07853890.2011.577093
24. Moschen AR, Tilg H, Raine T. IL-12,IL-23 and IL-17 in IBD: immunobiology and therapeutic targeting. Nat Rev Gastroenterol Hepatol. 2019;16(3):185-196. doi:10.1038/s41575-018-0084-8




