Dr. Javier Lumbreras / Dr. Luis Javier Morales García
La incidencia de la enfermedad litiásica renal está aumentando en toda la población del mundo desarrollado, también entre los niños y adolescentes. El diagnóstico de la nefrolitiasis en la edad pediátrica ha aumentado en las últimas 5 décadas a nivel mundial, llegando a quintuplicarse. Actualmente, se ha cuantificado su incidencia en algunos estudios en unos 9-50 casos/100.000 menores de 18 años/año en países desarrollados1-5. No disponemos de datos específicos españoles en cuanto a prevalencia e incidencia en la edad pediátrica, si bien estudios en adultos han revelado cifras similares a otros países europeos6. Este aumento de la incidencia podría estar en relación con el cambio producido en los hábitos alimentarios5. Se ha observado un incremento del consumo de proteínas animales, sal, chocolate y refrescos de cola, junto con una disminución del consumo de agua, frutas, verduras y legumbres5,7,8.
Los niños tienen un alto riesgo de recurrencia de la litiasis (16-44%), especialmente los menores de 10 años5,9. Debemos tener presente, pues, que se trata de una enfermedad habitualmente crónica que se presenta desde los primeros años, con lo que supone en cuanto a morbilidad y afectación de la calidad de vida.

Drs. Javier Lumbreras (a la izq. de la imagen) y Luis Javier Morales García
Fuente: Drs. Lumbreras y Morales García
La litiasis renal es resultado de un proceso complejo donde intervienen tanto causas ambientales (tipo de dieta, factores climáticos, fármacos o infecciones urinarias), como factores hereditarios (factores genéticos, metabólicos y anatómicos). En la mayoría de los pacientes concurren varios factores predisponentes10. En su orina se producen fenómenos de cristalización descontrolada, cuando se alteran sus condiciones de estabilidad. Los cambios en la composición de la orina pueden ser producidos bien por el aumento en orina de promotores de la cristalización (calcio, fosfato, oxalato, ácido úrico o cistina) o bien por el déficit de inhibidores de la cristalización (citrato, magnesio, pirofosfato, macromoléculas y glucosaminoglicanos)11.
Los niños diagnosticados de litiasis tendrán familiares afectos en más del 50% de los casos, especialmente si son escolares y no se trata de litiasis infectivas11-13. Los cálculos en edad pediátrica están compuestos principalmente por oxalato cálcico (60-70%), fosfato cálcico o hidroxiapatita (8-20%), fosfato amónico magnésico o estruvita (5-18%), ácido úrico (5-15%) y cistina (1-5%) y otros, más raros10,13,14. Son, por tanto, más frecuentes los cálculos de fosfato amónico magnésico y de fosfato cálcico que en adultos, especialmente en niños pequeños, aunque los cálculos de oxalato cálcico son los más frecuentes.
El porcentaje de pacientes pediátricos con alteraciones metabólicas varía ampliamente en la literatura, pero lo que parece claro es que la prevalencia de alteraciones metabólicas es mayor que en adultos (hasta 75% según algunos estudios). Esto concuerda con la elevada prevalencia de antecedentes familiares. La hipercalciuria (de forma más frecuente, de causa idiopática) es el trastorno más frecuentemente identificado, aunque la hipocitraturia aparece como la primera en algunos estudios recientes8. Otras alteraciones metabólicas menos frecuentes son hiperoxaluria, la hiperuricosuria y la cistinuria. Sin embargo, aunque son factores indispensables, no son suficientes por sí mismos para que se forme el cálculo, siendo necesario que se produzca la retención del cristal mediante un proceso complejo en el que el cristal debe adherirse a las células tubulares o epiteliales15. Por ello, juegan un papel importante las malformaciones o variantes anatómicas de la vía urinaria y la pobre ingesta de agua que condicionan un bajo flujo urinario; el pH urinario alto o bajo según el tipo de cálculo; y las infecciones.
Los lactantes y preescolares presentan con una frecuencia relativa mayor litiasis asociadas a alteraciones metabólicas e infecciones urinarias, y a anomalías estructurales del espectro CAKUT (Congenital Anomalies of the Kidney and Urinary Tract)13. Las litiasis en los adolescentes, sobre los que recae principalmente el aumento de incidencia en pediatría, dependen en mayor medida de los hábitos dietéticos y del estilo de vida.

Cálculos
Fuente: Archivo
Cada cálculo concreto dependerá de los factores específicos de cada paciente. Para reducir las recurrencias se deben evaluar los factores de riesgo implicados en la litogénesis y, así, poner en marcha recomendaciones profilácticas para cada paciente10,11,16-20.
La atención del enfermo con litiasis urinaria, por tanto, no debe quedar limitada al tratamiento que procure la eliminación del cálculo presente, sino también a la prevención de nuevos episodios. Los pacientes deben estar informados acerca de en qué consisten estos estudios y qué tipo de profilaxis puede ser requerida, pues una condición indispensable para el éxito de estos programas es su adherencia a las recomendaciones.
El tratamiento médico se basa en una combinación de modificaciones dietéticas y medidas farmacológicas. Las medidas preventivas, que son similares a las terapéuticas, tienen una gran importancia dada la elevada tasa de recurrencia mencionada.
Para conocer los mecanismos metabólicos subyacentes, es preciso obtener muestras biológicas (sangre y orina, además del cálculo si estuviera disponible para su estudio) que resulten representativas de la fisiopatología individual de cada paciente. Si bien los parámetros más relevantes a determinar son conocidos, las muestras idóneas están en discusión18,20-22. Por otra parte, es necesario que las muestras sean obtenidas, conservadas y procesadas adecuadamente para evitar alteraciones dependientes de estos procesos. Se ha observado que su procesamiento preanalítico presenta una alta variabilidad y no siempre es el idóneo23. En un estudio de la Asociación Española de Nefrología Pediátrica (AENP) realizado entre sus miembros y presentado en su congreso de 2017, se identificaron oportunidades de mejora como una mayor protocolización en la recogida de muestras, la disminución en la variabilidad en la elección del tipo de muestra, la mayor valoración de periodos de riesgo litogénico específico con muestras postprandiales o infradiarias, y la mayor frecuencia de determinación del pH urinario como un parámetro más del estudio (así como la exactitud del método empleado para su determinación), entre otras24.
Al constatar la disparidad de actuaciones, se propuso crear un grupo de trabajo conjunto entre la AENP y la Sociedad Española de Medicina de Laboratorio (SEQCML) para obtener un documento de consenso y estandarizar la metodología de estudio metabólico de la litiasis renal en pacientes pediátricos25.
Los datos en los que se basan las recomendaciones de dicho artículo se obtuvieron de guías de práctica clínica publicadas, documentos de consenso y revisiones, así como de los artículos más relevantes publicados durante los últimos años sobre los distintos parámetros a evaluar. Además, la información comprende conclusiones lógicas basadas en nuestra comprensión actual sobre la relación entre la composición de la orina y la formación de cálculos. Las guías de mayor aceptación y seguimiento son las propuestas por la European Association of Urology (EAU)26,27 y la American Urological Association (AUA)28, pero solo contienen algunas escasas recomendaciones específicas para los pacientes pediátricos. Posteriormente a la publicación de este documento, ha sido publicado un documento de consenso internacional titulado “Urine and stone analysis for the investigation of the renal stone former: a consensus conference”. No es específico de la edad pediátrica, pero busca también establecer unos estándares de práctica clínica y de laboratorio en el estudio de los pacientes litiásicos, y se encuentra alineado con las conclusiones de nuestro documento de consenso en muchos aspectos20.
Hay que recordar que todos los pacientes con debut de enfermedad litiásica en la infancia y adolescencia son considerados de alto riesgo de recurrencia, por lo cual todos serían candidatos a evaluación metabólica exhaustiva. Además, en muchos pacientes pediátricos concurren otros criterios de alto riesgo, como son la existencia de uropatías, los antecedentes familiares y una elevada proporción de anomalías metabólicas19,28-31.
Los métodos de evaluación metabólica que actualmente se proponen son asequibles para la mayoría de los centros hospitalarios, de sencilla ejecución y costes razonables. Estos estudios proporcionan información suficiente para una terapia racional y específica contra la enfermedad litiásica. Los planes terapéuticos profilácticos son relativamente sencillos de aplicar y seguir en el tiempo, con aceptable tolerancia y pocos efectos secundarios, y pueden reducir la tasa de recidiva litiásica por debajo del 25% a largo plazo32-34. Esto va íntimamente ligado a la adherencia continuada y completa al tratamiento, lo cual con frecuencia es difícil de conseguir.
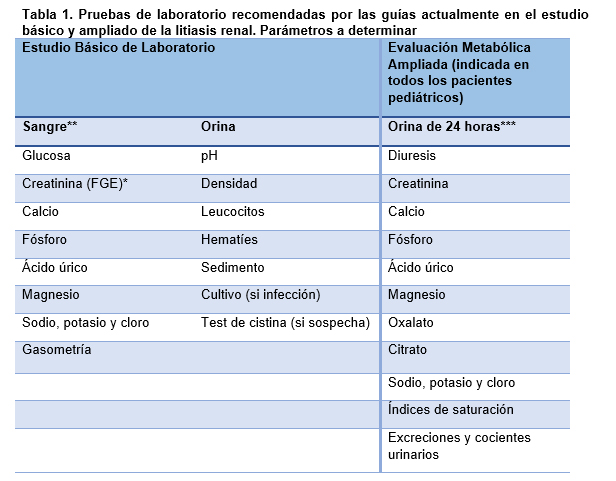
*FGE: filtrado glomerular estimado. Recomendable calcularlo con ecuaciones validadas, además de valorar la concentración de creatinina en plasma.
**El estudio de PTH y los metabolitos de la vitamina D (25-OH-vitamina D y 1,25-OH-vitamina D) debería realizarse ante el hallazgo de alteraciones metabólicas sanguíneas o urinarias en los solutos relacionados: calcio, fosfato o magnesio.
***La determinación de parámetros urinarios en fracciones de tiempo inferiores no constituye actualmente la prueba de referencia para el diagnóstico de anomalías metabólicas urinarias. Diversos autores la recomiendan para caracterizar mejor los periodos de mayor riesgo litogénico.
Adaptado de Lumbreras J et al. Estudio metabólico urinario para el diagnóstico y seguimiento de la litiasis renal en pacientes pediátricos. Documento de consenso. Revista Española de Pediatría Clínica e Investigación. 2020; 75 Suppl. 1
Todos los pacientes, independientemente de la composición del cálculo y del comportamiento clínico de la enfermedad, deberían someterse a una evaluación inicial mediante historia clínica, estudios de laboratorio, estudios por imagen y estudio morfocomposicional del cálculo20, una vez que se haya procedido al tratamiento de eliminación de dicho cálculo (Tabla 1).
A continuación, se expone un extracto del documento de consenso elaborado. En primer lugar, se hace referencia a las muestras a obtener y solutos a estudiar. Más adelante, se hace hincapié en las condiciones de recogida de las muestras de orina, ya que resultan fundamentales para que sean representativas. Finalmente se reflejan algunas consideraciones sobre el estudio de los cálculos renales y, finalmente, aparecen unas recomendaciones concretas basadas en toda la revisión previa. Las consideraciones sobre procesamiento en laboratorio de las muestras y valoración de los diferentes solutos de interés no se exponen aquí por la extensión del documento y por ser muy específicos de especialistas.
Estudios de laboratorio
Análisis de sangre
El análisis de una muestra de sangre siempre debe ser parte del estudio metabólico. La analítica sanguínea permite investigar la presencia de una enfermedad sistémica y la función renal glomerular y tubular del paciente. El análisis de sangre debe incluir, al menos, las siguientes variables: glucosa, creatinina, tasa de filtración glomerular estimada, iones (sodio, potasio y cloro), calcio total corregido con albúmina o calcio ionizado, fosfato, magnesio, urato y bicarbonato27,35. Este número mínimo de análisis siempre debe ampliarse cuando las circunstancias lo requieran.
Análisis de orina: primera orina de la mañana
En esta orina se debe realizar un sistemático, del que interesan especialmente pH, densidad, nitritos, leucocitos, hematíes; y un análisis del sedimento. Se debe realizar urocultivo si se sospecha litiasis infectiva o infección urinaria por la presencia de bacteriuria, nitritos o leucocituria en el sedimento urinario. Un cultivo positivo a gérmenes ureolíticos (Proteus spp, Staphylococcus spp, Klebsiella spp, Pseudomonas aeruginosa, Serratia marcescens) es indicativo de un cálculo de estruvita.
En caso de sospecha de litiasis cistínica, sería apropiado el test cualitativo de cistina (también conocido como test de Brand). Presenta hasta un 25% de falsos negativos. Por ello, si persiste una alta sospecha, se debería recurrir a una determinación de aminoácidos en orina.
Un pH de orina persistente por encima de 7 sugiere litiasis de fosfato amónico magnésico o de hidroxiapatita13.
Evaluación metabólica ampliada o extendida
La mayoría de documentos y guías actuales proponen que, en los pacientes con litiasis cálcica o de composición desconocida, sea determinada en orina de 24 horas la creatinina, calcio, fósforo, oxalato, ácido úrico, citrato, magnesio, sodio, potasio y diuresis total (Tabla 1). Con estos resultados se calculan las excreciones y cocientes urinarios para los distintos solutos, así como también otros parámetros de función tubular, que nos pueden informar sobre la existencia de anomalías metabólicas. También se pueden calcular los índices de saturación para oxalato cálcico, fosfato cálcico y ácido úrico. Estos índices establecen el riesgo litogénico relacionando el grado de saturación urinaria de un componente con la concentración de inhibidores de la litogénesis. El cociente calcio/citrato resulta más sencillo de calcular y tiene amplia aceptación como marcador de riesgo de cristalización de sales cálcicas. También resulta muy útil la representación en gráficas del perfil de riesgo litogénico del paciente acorde al grado de concentración en orina de los factores promotores e inhibidores de la calculogénesis36.
Es importante resaltar las diferencias conceptuales entre alteración metabólica urinaria y riesgo litogénico. La alteración metabólica indica una eliminación urinaria alterada de una sustancia relacionada con la litiasis renal (por exceso o defecto, en relación con los estándares de normalidad que suelen ser definidos de una forma estadística), mientras que el riesgo litogénico indica el riesgo de cristalización urinaria para un tipo de cristal concreto. La interrelación viene dada porque las alteraciones metabólicas hacen que la orina del paciente supere con mayor facilidad los límites de metaestabilidad, pero estos límites también se pueden superar con valores de excreción urinaria de los diversos solutos dentro de la normalidad, unidos a diuresis bajas o pH alterados.

Autor/a: Piotr Siedlecki
Fuente: www.publicdomainpictures.net
Las muestras de orina de micción aislada y de periodos inferiores a las 24 horas deben ser consideradas cuando la recogida de orina en un día completo está dificultada, como puede suceder en los niños no continentes19. Se están evaluando los beneficios de la determinación de parámetros en periodos de tiempo inferiores a 24 horas, en cuanto a una mejor caracterización de los periodos de riesgo litogénico, dado que es conocido que hay componentes urinarios implicados en la formación de cálculos con variaciones circadianas, así como el flujo urinario37.
No debe olvidarse que, en muchos casos, los cálculos presentan varios compuestos, bien por su etiología multifactorial, o bien por la influencia del tratamiento iniciado previamente a su eliminación, lo que también justifica un estudio amplio38.
Los estudios metabólicos de seguimiento son necesarios para evaluar la respuesta a las medidas preventivas recomendadas. Se recomienda realizar el primer control a los 2 o 3 meses después de comenzar la profilaxis o tratamiento médico. Se realizarán los ajustes necesarios cuando no estén corregidas adecuadamente las alteraciones metabólicas observadas, siendo necesarias nuevas evaluaciones posteriores. Una vez que se ha conseguido la normalización de los parámetros urinarios, las guías consideran suficiente una nueva evaluación metabólica en períodos anuales39. En los pacientes pediátricos, teniendo en cuenta los cambios corporales debidos al crecimiento, seguramente sea precisa una evaluación más frecuente.
Condiciones de recogida de la orina para la medición de pruebas bioquímicas
Recogida de la orina de 24 horas
La obtención de la orina, a diferencia de otros tipos de muestra, depende fundamentalmente de la colaboración del paciente. Por este motivo, resulta fundamental instruirlo respecto a las condiciones óptimas de recogida y transmitirle la responsabilidad de la obtención de una orina de calidad que repercutirá en los resultados que de ella se deriven. La instrucción del paciente, por tanto, será clave para permitir la obtención de una muestra adecuada, requiriéndose además unos procedimientos estandarizados para producir intervalos de referencia consistentes y límites de decisión para la interpretación armonizada de los resultados.
Debido a los avances tecnológicos, los errores más frecuentes no se producen en el análisis de la muestra sino en su recolección, transporte y procesamiento preanalítico en el laboratorio40.
Ante la necesidad de estandarizar los procedimientos de recogida, transporte, manejo y análisis de las muestras de orina se elaboraron guías internacionales como la European Urinalysis Guidelines (2000) bajo el auspicio de la European Confederation of Laboratory Medicine (ECLM)40, o la GP16-a3 Urinalysis; Approved Guideline - Third Edition (2009) del Clinical and Laboratory Standards Institute (CLSI)41. Estas guías tienen el reconocimiento internacional y deben ser adaptadas a cada laboratorio según sus circunstancias.
Las principales recomendaciones que habría que tener en consideración para conseguir una muestra de orina de calidad hacen referencia a los diferentes aspectos del proceso preanalítico, y fueron recogidas en un trabajo de la Comisión de Función Renal de la Sociedad Española de Medicina de Laboratorio (SEQCML)42:
- En la petición y citación de una analítica de orina deberán tenerse en cuenta los requerimientos de recogida, así como las incompatibilidades de diferentes analitos en un único recipiente.
- El laboratorio deberá entregar instrucciones escritas con información gráfica para la correcta recogida de la orina, así como proporcionar los envases de recogida adecuados.
- El laboratorio, el médico peticionario o ambos deberán asegurarse de que el paciente ha entendido esa información y de que éste es consciente de la importancia de seguir las instrucciones.
- Las muestras de orina deberán ser entregadas en su totalidad al laboratorio y que éste sea el encargado de su manipulación.
- En la recepción de las orinas el laboratorio deberá verificar que han sido recogidas correctamente, y tener descritos criterios de rechazo de las muestras.
Procedimiento de recogida de la orina de 24 horas
Hay protocolos que recomiendan que la recogida sea de 8 a 8 de la mañana del día siguiente por comodidad para el paciente, pero también son válidas las orinas que se recogen en otros horarios siempre que el periodo de recolección sea el convenido, generalmente 24 horas.

Autor/a: George Hodan
Fuente: www.publicdomainpictures.net
Proponemos dos procedimientos de recogida de orina de 24 horas según las recomendaciones de las diferentes guías clínicas42:
• Procedimiento tradicional: habitualmente se recomienda que la recogida del espécimen de orina de 24 horas se inicie al levantarse por la mañana del día anterior a la cita en el laboratorio. Esa primera orina se descartará en el váter y a partir de ese momento, durante las 24 horas siguientes, el paciente deberá ir recogiendo en el contenedor toda la orina emitida, incluyendo la de la primera micción de la mañana del día de la cita en el laboratorio. Este procedimiento hace incompatible la entrega, en el mismo día de la cita, de la orina de 24 horas junto con la primera orina de la mañana.
• Procedimiento alternativo: este sistema permite la entrega de ambos especímenes (24 horas y primera orina de la mañana) en la misma cita, y de este modo evita al paciente la molestia de tener que desplazarse dos días distintos al centro de extracción para entregar las dos orinas. Consiste en iniciar la recogida de la orina de 24 horas en cualquier momento dos días antes de la fecha de la cita, por ejemplo, al acostarse. Justo antes de irse a la cama, el paciente orinará directamente en el váter y anotará la hora exacta en el recipiente. A partir de ese momento iniciará la recogida completa de la orina durante 24 horas. Al día siguiente antes de acostarse, exactamente a la misma hora en que se inició la recogida el día anterior, el paciente orinará por última vez incluyendo esta porción en el contenedor de 24 horas. A la mañana siguiente, es decir, el día de la cita en el laboratorio, al levantarse de la cama recogería la orina de una micción, siguiendo el procedimiento habitual de porción media de la primera orina de la mañana tras lavado de genitales externos. Podría ser propuesto como único procedimiento de recogida de orina de 24 horas para simplificar y facilitar la transmisión de la información, haya que recoger o no la primera orina de la mañana.
Problemas con la recogida de la orina de 24 horas
Tradicionalmente, y en la mayoría de las recomendaciones actuales sobre la evaluación metabólica de los pacientes con urolitiasis, se destaca el importante papel del análisis de orina de 24 horas. Debido a la variabilidad de este tipo de muestras, algunas sociedades recomiendan confirmar los resultados encontrados en una muestra de orina, si bien no hay unanimidad. La guía clínica de la EAU recomienda dos muestras19 y la de la AUA una o dos muestras28. Parece evidente que, cuanto mayor sea el número de muestras necesario, menor va a ser el cumplimiento, pero mayor la representatividad de las muestras.
La mayoría de los protocolos actuales proponen la recogida de dos muestras de orina de 24 horas para la evaluación inicial, bajo una dieta libre, con el fin de aumentar las posibilidades de detección de alteraciones metabólicas.
Sin embargo, es importante enfatizar que, independientemente del número de recolecciones de orina usadas para el análisis, este método de muestreo solo proporciona información sobre la composición promedio de la orina durante todo el período de recolección. En consecuencia, no se ha establecido si todos los formadores de cálculos recurrentes se benefician de la recolección de orina de 24 horas19. A pesar de ello, se ha demostrado que casi el 90% de los pacientes evaluados presentan una o varias alteraciones metabólicas asociadas. Se piensa que, en aquellos pacientes en los que no se detecta ninguna alteración, esto puede ser debido a errores de metodología como inadecuada recolección de orina durante las 24 horas, modificaciones de la dieta y estilo de vida habituales del paciente, no supresión de medicación potencialmente litogénica, episodio clínico de litiasis muy reciente, incorrecta manipulación o contaminación bacteriana de las muestras, y retrasos en el procesamiento desde su entrega al laboratorio.
Aunque el consejo para los pacientes siempre debe ser que la recolección de orina se realice en condiciones tan normales como sea posible, la experiencia ha demostrado que la ingesta de líquidos es mayor y que la orina es recogida durante los fines de semana cuando las condiciones no necesariamente reflejan la actividad normal entre semana43.
Los pacientes pueden tener períodos de alto riesgo, ocasionales y muy específicos que, por esta misma razón, permanecen sin ser detectados si la recolección no es llevada a cabo en relación directa con dichos períodos. Por ejemplo, se supone que la baja ingesta de líquidos durante las actividades deportivas o el ejercicio intenso pueden dar a corto plazo picos de supersaturación u otras anomalías de la orina. Este último problema solo puede resolverse mediante un interrogatorio apropiado en la historia clínica y, en consecuencia, adaptarlo a los procedimientos analíticos.

Fuente: Archivo
La demostración de altos niveles de sobresaturación en la orina de 24 horas ciertamente refleja la presencia de períodos con picos de riesgo de cristalización, pero no es posible con este muestreo saber cuándo ocurren estos períodos particulares44,45.
Las condiciones bajo las cuales el paciente almacena la orina durante el período de recolección también son de gran importancia. La orina debe almacenarse refrigerada a una temperatura inferior a 8 °C durante la recolección para evitar el crecimiento bacteriano, y este sería el método de conservación recomendado46,47. De lo contrario, sería necesaria la utilización de conservantes como timol al 5% en isopropanol. La utilización de conservantes ácidos como el ácido clorhídrico (2 N) o el ácido bórico (10 g) produciría la precipitación del ácido úrico y no sería aconsejable, ya que serían necesarias varias muestras de orina de 24 horas. La utilización de la orina nocturna de 8 horas o de primera micción es una alternativa en pacientes en los que la recogida de la orina de 24 horas se hace complicada, como en los niños, relacionando la tasa de excreción con la creatinina.
Recogida de orina aislada
El error preanalítico en las muestras de orina reciente es difícil de detectar; por ello es importante que los laboratorios tengan procesos para garantizar el cumplimiento de las mejores prácticas en la recolección, manejo y transporte.
La muestra de la primera hora de la mañana es la muestra de orina más recomendada y con frecuencia solicitada y contiene una gran cantidad de información, pero el desconocimiento o poco cuidado que se hace de su recolección hace que los errores preanalíticos sean muy frecuentes. Es conocida también como orina de ocho horas u orina de primera hora de la mañana41.
Siempre es importante solicitar la primera orina de la mañana, puesto que al ser la más concentrada es más fácil encontrar los elementos propios de la muestra, de ahí que la capacidad de diagnóstico esté aumentada. También podemos destacar que, al prescribir la primera orina de la mañana, estará menos influida por las dietas y el ejercicio físico. Sin embargo, solicitar otras muestras posprandiales o en otras condiciones concretas puede evidenciar situaciones de riesgo litogénico.
El volumen de orina necesario para realizar el estudio sistemático de la orina incluido el sedimento oscila entre 8 y 12 mL, siendo aconsejable recoger al menos 30 mL. Sin embargo, en los niños pequeños o en pacientes que tengan oligoanuria es muy frecuente encontrar que las muestras recolectadas en un momento puntual son de un volumen inferior a éste48.
Procedimiento de recogida de orina aislada
Se informará debidamente al paciente sobre las condiciones de cómo debe recoger la muestra, entregándole las instrucciones por escrito. Éstas deben ser muy gráficas, con ilustraciones, que permitan una comprensión fácil por parte del paciente y sus tutores, además de ser explicadas verbalmente.
Se le entregarán al paciente los contenedores para la recogida de los especímenes de orina que se deberían proporcionar junto con las instrucciones, con el fin de evitar el uso de recipientes inadecuados. Consideramos útiles los contenedores con dispositivos de transferencia a los tubos de recogida por el sistema de vacío; éstos presentan numerosas ventajas en cuanto a la facilidad de manejo, ya que permiten el llenado de tantas alícuotas como sean necesarias de forma fácil, rápida e higiénica, evitando los riesgos de derramamiento, contaminación, olores, exposiciones accidentales a la orina con el peligro de contagios, etc.

Autor/a de la imagen: E. Arandes / www.farmacosalud.com
Fuente: www.farmacosalud.com
Instrucciones genéricas:
1. El día de la cita, al levantarse por la mañana, lávese las manos y los genitales externos con jabón. Después, aclárese con abundante agua y séquese con una toalla limpia y seca.
2. Desprecinte el contenedor y destápelo.
3. Empiece a orinar en el váter y recoja en el contenedor de la orina la porción media de la micción.
4. Tape el contenedor y acuda al laboratorio para entregarlo.
En el caso de los pacientes pediátricos que no controlen adecuadamente la micción o recién nacidos, se deben utilizar las bolsas colectoras con adhesivos hipoalergénicos, que se cambiarán cada 20 minutos para evitar las contaminaciones. Instrucciones:
1. Lave y seque cuidadosamente los genitales y el área perineal.
2. Coloque la bolsa de plástico o el colector estéril con ayuda de los adhesivos.
3. Retire la bolsa en cuanto el niño haya orinado. Meterla en un recipiente, taparla y entregarla en el laboratorio.
4. Si en 20 minutos el niño no ha orinado, retire la bolsa y repita de nuevo el proceso desde el principio.
Estudio de los cálculos urinarios
La composición bioquímica del cálculo y su ultraestructura proporcionan información sobre los factores implicados en su génesis38. Por ello, es deseable recuperar el cálculo para su análisis tanto si la expulsión es espontánea (con o sin litotricia previa) como si se obtiene por técnicas de endourología o cirugía abierta27, incluso aunque se recuperen fragmentos y no el cálculo íntegro.
El cálculo debe ser remitido en un recipiente en seco al laboratorio para evitar su disolución, aunque sea parcial, o cambios en su composición por interacción con el disolvente (esto incluye no enviarlo en orina).
Se pueden utilizar diversas técnicas analíticas. El análisis mediante reactivos químicos no se recomienda, dado que proporciona información insuficiente (solo sobre los componentes y no sobre la estructura y proporciones de los mismos en el caso de cálculos mixtos). Además, la probabilidad de errores es inaceptable, especialmente si el cálculo tiene varios componentes (lo cual es frecuente)23,49.
La microscopía estereoscópica requiere de personal entrenado, pero puede identificar los componentes, la estructura superficial e interna, y si hay punto de anclaje a la papila, a un coste aceptable.
La espectrometría de infrarrojos conlleva un coste más alto y requiere un laboratorio con personal especializado. Por tanto, es necesario un volumen de muestras (para esta u otras finalidades) que permita rentabilizar costes. Permite identificar los componentes del cálculo y trabajar con muestras pequeñas.

Cálculo al microscopio
Fuente: Archivo
La microscopía electrónica de barrido (a menudo acoplada a análisis por dispersión de rayos X) tiene un coste alto y requiere personal especializado, pero permite identificar los componentes y da imágenes detalladas de la estructura.
En general, balanceando las ventajas e inconvenientes, sería recomendable el estudio con microscopía estereoscópica, apoyado siempre que sea posible en espectrometría de infrarrojos y en la microscopía electrónica siempre que esté disponible49,50. Por ello, los cálculos renales deberían ser analizados en laboratorios especializados. Así pues, tanto por criterios de eficiencia como de coste-beneficio, se debería centralizar el análisis de las muestras por áreas geográficas.
Recomendaciones y puntos clave
• Dada la mayor prevalencia de anomalías metabólicas y elevada tasa de recurrencia, en todos los niños y adolescentes con litiasis renal se debe realizar un estudio metabólico completo. Éste debería realizarse en condiciones habituales de ingesta y hábitos generales de vida, y al menos 20 días después de episodios de infección urinaria o cólico renal.
• El estudio metabólico debería incluir una bioquímica en sangre y en orina de 24 horas. Dada la elevada variabilidad en la recogida de la orina de 24 horas y de la eliminación de muchos solutos y del volumen urinario entre distintos días, el estudio metabólico debería incluir varias muestras urinarias de días diferentes, al menos dos.
• En los pacientes no continentes podría sustituirse la orina de 24 horas por orina de micción, teniendo en cuenta la posible falta de concordancia en cuanto a la presencia o ausencia de anomalías metabólicas. También parece recomendable la determinación de los parámetros mencionados previamente en muestras de varios días diferentes.
• El riesgo litogénico de la orina varía a lo largo del día en función de las concentraciones de solutos, volúmenes urinarios y pH. No hay consenso sobre cómo evaluar esto, pero parece que la recogida de muestras de orina fraccionadas por periodos de tiempo podría ayudar a caracterizar mejor las anomalías metabólicas y los periodos de riesgo litogénico.
• Es preciso tomar medidas para la conservación de la muestra de orina de 24 horas (o de periodos inferiores que no sean una orina aislada que se procese tras su recogida). La adición de inhibidores del crecimiento bacteriano como el timol o la conservación en frío parecen opciones válidas.
• No es preciso recoger orina separada en recipientes con y sin adición de acidificante. De hecho, esto impide determinar todos los solutos en una misma muestra y, dada la variabilidad interdiaria, dificulta el cálculo del riesgo litogénico. A su llegada al laboratorio, se puede separar en varias alícuotas y acidificar las que se destinen a determinación de calcio, fosfato, magnesio y oxalato, si no se van a procesar inmediatamente. Parece recomendable agitar la muestra antes de su procesado para suspender posibles precipitados. Para un correcto estudio del úrico, en caso de no procesarse inmediatamente la orina, sería conveniente alcalinizarla y podría ser preciso calentarla previamente a su análisis.
• El análisis de los cálculos urinarios mediante reactivos da insuficiente información y posibles errores, especialmente en lo cálculos con varios componentes. El estudio de los cálculos urinarios debe realizarse por microscopía estereoscópica, espectrofotometría de infrarrojos o microscopía electrónica de barrido con microanálisis por difracción de rayos X, o mejor aún, por varias técnicas, si es posible. Deberían ser realizadas e interpretadas por profesionales con formación específica.
Agradecemos la colaboración de la Asociación Española de Nefrología Pediátrica (AENP) y de la Sociedad Española de Medicina de Laboratorio (SEQCML) en la elaboración del documento de consenso y, en especial, de los coautores que participaron con nosotros en la revisión de la bibliografía, así como en su diseño y redacción. Por parte de la AENP: B. Amil, J. Cabrera, V. Cantos, L. Espinosa, S. González Pastor, B. Huertes, E. Trillo. Y por parte de la SEQCML, P. Fernández Riejos, A.M. García Raja, C. Gómez Cobo, C. Macías.
Bibliografía
1. Grases F, Rodriguez A, Costa-Bauza A, et al. Factors Associated With the Lower Prevalence of Nephrolithiasis in Children Compared With Adults. Urology. 2015;86(3):587-592. doi:10.1016/j.urology.2015.06.028
2. Scales CDJ, Smith AC, Hanley JM, Saigal CS. Prevalence of kidney stones in the United States. Eur Urol. 2012;62(1):160-165. doi:10.1016/j.eururo.2012.03.052
3. Sharma AP, Filler G. Epidemiology of pediatric urolithiasis. Indian J Urol. 2010;26(4):516-522. doi:10.4103/0970-1591.74450
4. Edvardsson VO, Ingvarsdottir SE, Palsson R, Indridason OS. Incidence of kidney stone disease in Icelandic children and adolescents from 1985 to 2013: results of a nationwide study. Pediatr Nephrol. 2018;33(8):1375-1384. doi:10.1007/s00467-018-3947-x
5. Hernandez JD, Ellison JS, Lendvay TS. Current trends, evaluation, and management of pediatric nephrolithiasis. JAMA Pediatr. 2015;169(10):964-970. doi:10.1001/jamapediatrics.2015.1419
6. Cano-Castiñeira R, Carrasco-Valiente J, Pérula-de-Torres LA, et al. Prevalencia de la litiasis renal en Andalucía: resultados del estudio PreLiRenA. Actas Urológicas Españolas. 2015;39(1):26-31. doi:10.1016/j.acuro.2014.02.006
7. Romero V, Akpinar H, Hospital L. Kidney Stones : A Global Picture of Prevalence , Incidence , and. Rev Urol. 2016;12(May):86-96. doi:10.3909/riu0459
8. Cameron MA, Sakhaee K, Moe OW. Nephrolithiasis in children. Pediatr Nephrol. 2005;20(11):1587-1592. doi:10.1007/s00467-005-1883-z
9. Pietropaolo A, Proietti S, Jones P, et al. Trends of intervention for paediatric stone disease over the last two decades (2000-2015): A systematic review of literature. Arab J Urol Arab J Urol (Official J Arab Assoc Urol. 2017;15:306-311. doi:10.1016/j.aju.2017.10.006
10. Lancina Martín JA. Estudio metabólico. Cómo hacerlo accesible, útil y generalizado. Arch Esp Urol. 2017;70(1):71-90.
11. Moreira Guimarães Penido MG, de Sousa Tavares M. Pediatric primary urolithiasis: Symptoms, medical management and prevention strategies. World J Nephrol. 2015;4(4):444-454. doi:10.5527/wjn.v4.i4.444
12. Monico CG, Milliner DS. Genetic determinants of urolithiasis. Nat Rev Nephrol. 2012;8(3):151-162. doi:10.1038/nrneph.2011.211
13. Lumbreras Fernández J. Aportes a la investigación en Litiasis renal infantil. Published online October 2, 2020. Accessed February 28, 2021. http://dspace.uib.es/xmlui/handle/11201/154580
14. Garcia-Nieto V, Luis-Yanez MI, Fraga Bilbao F. Litiasis Renal. Nefrol al Día. Published online 2018. doi:10.1157/13068212
15. Areses Trapote R, Urbieta Garagorri MA, Ubetagoyena Arrieta M, Monge TM, Arruebarrena D. Evaluación de la enfermedad renal litiásica. Estudio metabólico. An Pediatr. 2004;61(5):418-445.
16. Gambaro G, Croppi E, Coe F, et al. Metabolic diagnosis and medical prevention of calcium nephrolithiasis and its systemic manifestations: a consensus statement. J Nephrol. 2016;29(6):715-734. doi:10.1007/s40620-016-0329-y
17. Gouru VR, Pogula VR, Vaddi SP, Manne V, Byram R, Kadiyala L. Metabolic evaluation of children with urolithiasis. Urol Ann. 2018;10(1):94-99. doi:10.4103/UA.UA_98_17
18. Hoppe B, Kemper MJ. Diagnostic examination of the child with urolithiasis or nephrocalcinosis. Pediatr Nephrol. 2010;25:403-413. doi:10.1007/s00467-008-1073-x
19. Skolarikos A, Straub M, Knoll T, et al. Metabolic evaluation and recurrence prevention for urinary stone patients: EAU guidelines. Eur Urol. 2015;67(4):750-763. doi:10.1016/j.eururo.2014.10.029
20. Williams JC, Gambaro G, Rodgers A, et al. Urine and stone analysis for the investigation of the renal stone former: a consensus conference. Urolithiasis. 2021;49(1):1-16. doi:10.1007/s00240-020-01217-3
21. Sáez-Torres C, Rodrigo D, Grases F, et al. Urinary excretion of calcium, magnesium, phosphate, citrate, oxalate, and uric acid by healthy schoolchildren using a 12-h collection protocol. Pediatr Nephrol. 2014;29(7):1201-1208. doi:10.1007/s00467-014-2755-1
22. Hoppe B. Editorial commentary: Urinary excretion of calcium, magnesium, phosphate, citrate, oxalate, and uric acid by healthy schoolchildren using a 12-h collection protocol. Pediatr Nephrol. 2014;29(11):2065-2067. doi:10.1007/s00467-014-2925-1
23. Morales LJ, Salvador G, Pedret V, Llop ES. Muestras de Orina de 24 Horas y Orina Reciente Para La Medición de Las Magnitudes Biológicas Más Comunes. Comité de Comunicación de la Sociedad Española de Medicina de Laboratorio; 2017.
24. The XLII Spanish Congress of Pediatric Nephrology : 18-20 May 2017, Madrid, Spain. In: Pediatric Nephrology (Berlin, Germany). Vol 33. Springer International; 2018:731-739. doi:10.1007/s00467-018-3890-x
25. Lumbreras J, Morales-García LJ, Amil B, et al. Estudio metabólico urinario para el diagnóstico y seguimiento de la litiasis renal en pacientes pediátricos. Documento de consenso. Rev Española Pediatría Clínica e Investig. 2020;75(Suppl I).
26. Turk C, Petrik A, Sarica K, et al. EAU Guidelines on Urolithiasis. Eur Assoc Urol. 2013;69(3):475-482. doi:10.1159/000049803
27. Türk C, Petřík A, Sarica K, et al. EAU Guidelines on Diagnosis and Conservative Management of Urolithiasis. Eur Urol. 2016;69(3):468-474. doi:10.1016/j.eururo.2015.07.040
28. Pearle MS, Goldfarb DS, Assimos DG, et al. Medical management of kidney stones: AUA guideline. J Urol. 2014;192(2):316-324. doi:10.1016/j.juro.2014.05.006
29. Trinchieri A, Ostini F, Nespoli R, Rovera F, Montanari E, Zanetti G. A prospective study of recurrence rate and risk factors for recurrence after a first renal stone. J Urol. 1999;162(1):27-30. doi:10.1097/00005392-199907000-00007
30. Straub M, Strohmaier WL, Berg W, et al. Diagnosis and metaphylaxis of stone disease. Consensus concept of the National Working Committee on Stone Disease for the upcoming German Urolithiasis Guideline. World J Urol. 2005;23(5):309-323. doi:10.1007/s00345-005-0029-z
31. Tiselius HG. Possibilities for preventing recurrent calcium stone formation: principles for the metabolic evaluation of patients with calcium stone disease. BJU Int. 2001;88(2):158-168. doi:10.1046/j.1464-410x.2001.02308.x
32. Cameron M, Maalouf NM, Poindexter J, Adams-Huet B, Sakhaee K, Moe OW. The diurnal variation in urine acidification differs between normal individuals and uric acid stone formers. Kidney Int. 2012;81(11):1123-1130. doi:10.1038/ki.2011.480
33. Fink HA, Wilt TJ, Eidman KE, et al. Medical management to prevent recurrent nephrolithiasis in adults: A systematic review for an American College of Physicians Clinical Guideline. Ann Intern Med. 2013;158(7):535-543. doi:10.7326/0003-4819-158-7-201304020-00005
34. Parks JH, Coe FL. Evidence for durable kidney stone prevention over several decades. BJU Int. 2009;103(9):1238-1246. doi:10.1111/j.1464-410X.2008.08170.x
35. Moe OW, Pearle MS, Sakhaee K. Pharmacotherapy of urolithiasis: Evidence from clinical trials. Kidney Int. 2011;79(4):385-392. doi:10.1038/ki.2010.389
36. Pak CY, Skurla C, Harvey J. Graphic display of urinary risk factors for renal stone formation. J Urol. 1985;134(5):867-870. doi:10.1016/s0022-5347(17)47496-9
37. Mir C, Rodriguez A, Rodrigo D, et al. Analysis of urine composition from split 24-h samples: use of 12-h overnight samples to evaluate risk factors for calcium stones in healthy and stone forming children. J Pediatr Urol. 2020;16(3):371e1-371e7. doi:10.1016/j.jpurol.2020.02.011
38. Cloutier J, Villa L, Traxer O, Daudon M. Kidney stone analysis: “Give me your stone, I will tell you who you are!” World J Urol. 2014;33(2):157-169. doi:10.1007/s00345-014-1444-9
39. Norman RW, Bath SS, Robertson WG, Peacock M. When should patients with symptomatic urinary stone disease be evaluated metabolically? J Urol. 1984;132(6):1137-1139. doi:10.1016/s0022-5347(17)50064-6
40. (ECLM) . European Confederation of Laboratory Medicine. European urinalysis guidelines. Scand J Clin Lab Invest Suppl. 2000;231:1-86.
41. Rabinovitch A, Arzoumanian L, Curcio KM, Dougherty B, Halim A-B. Clinical Laboratory Standards Institute (CLSI). Urinalysis and Collection, Transportation, and Preservation of Urine Specimens; Approved Guide¬line. CLSI Document GP16-a3—Third Edition. Clin Lab Stand Inst. 2009;29(4):1-53.
42. Moreno-Carbonell V, Morales-García L, Martínez-López R. Preanalítica de orina de 24 horas: qué hacemos y qué deberíamos hacer. Rev Lab Clin. 2016;9(3):115-123.
43. Rodgers A, Barbour L, Pougnet B, Lombard C, Ryall R. Urinary element concentrations in kidney stone formers and normal controls: the week-end effect. J Trace Elem Electrolytes Health Dis. 1994;8(2):87-91.
44. Murayama T, Sakai N, Yamada T, Takano T. Role of the diurnal variation of urinary pH and urinary calcium in urolithiasis: A study in outpatients. Int J Urol. 2001;8(10):525-531. doi:10.1046/j.1442-2042.2001.00366.x
45. Ahlstrand C, Larsson L, Tiselius HG. Variations in urine composition during the day in patients with calcium oxalate stone disease. J Urol. 1984;131(1):77-81. doi:10.1016/s0022-5347(17)50211-6
46. Ribeiro Nogueira Ferraz R, Calabria Baxmann A, Gorayb Ferreira L, et al. Preservation of urine samples for metabolic evaluation of stone-forming patients. Urol Res. 2006;34(5):329-337. doi:10.1007/s00240-006-0064-2
47. Yilmaz G, Yilmaz FM, Hakligör A, Yücel D. Are preservatives necessary in 24-hour urine measurements? Clin Biochem. 2008;41(10-11):899-901. doi:10.1016/j.clinbiochem.2008.03.002
48. Ventura Pedret S. Principios de Preanalítica En Atención Primaria. Vision Libros; 2010.
49. Hesse A, Kruse R, Geilenkeuser W-J, Schmidt M. Quality control in urinary stone analysis: results of 44 ring trials (1980-2001). Clin Chem Lab Med. 2005;43(3):298-303. doi:10.1515/CCLM.2005.051
50. Garcia-Garcia S, Millán-Rodríguez F, Rousaud-Barón F, et al. Por qué y cómo hemos de analizar los cálculos urinarios. Actas Urol Esp. 2011;35(6):354-362. doi:10.1016/j.acuro.2011.01.017.




