Redacción Farmacosalud.com
‘Muerto el perro, se acabó la rabia’, dice el refranero popular. Pues bien, en el caso que nos ocupa, podríamos decir perfectamente que ‘curado el pollo, eliminada la Salmonella’... o, al menos, gran parte de la población de Salmonella, en tanto que “los pollos y otros animales de producción aviar son el principal reservorio de estas bacterias” tan nocivas para la salud, recuerda la profesora Montserrat Llagostera Casas, catedrática de Microbiología del Departamento de Genética y Microbiología de la Universitat Autònoma de Barcelona (UAB), en Cerdanyola del Vallès (Barcelona). Siguiendo la estela del lenguaje aviar, no está de más resaltar que la Salmonella -agente causante de la salmonelosis- no es, ni mucho menos, moco de pavo: la salmonelisis es potencialmente mortal [1]. De hecho, la variante no tifoidea de este patógeno causa anualmente “155.000 muertes de humanos” en el mundo, comenta la profesora. Por ello, cobra aún más importancia el hecho de haber descubierto las virtudes de la nanoencapsulación lipídica, un método innovador que sirve para luchar eficazmente contra la Salmonella en animales, e indirectamente en humanos. Y, lo que es mejor, las perspectivas son más que prometedoras a la hora de combatir mediante este sistema otros agentes infecciosos, dado que “la tecnología de encapsulación que hemos desarrollado” puede aplicarse “contra patógenos bacterianos muy diversos”, opina Llagostera.

Un ejemplar de ganado aviar
Autor/a de la imagen: Lydia Jacobs
Fuente: www.publicdomainpictures.net
Investigadores de la UAB y del Instituto Catalán de Nanociencia y Nanotecnología (ICN2) han desarrollado un sistema de nanoencapsulación que aumenta la eficacia de los bacteriófagos -virus inocuos utilizados para eliminar infecciones bacterianas- incrementando su resistencia al ácido del estómago y alargando su actividad una vez están en el intestino. El método, publicado en ‘Applied and Environmental Microbiology’[2], ha sido probado con éxito en animales con Salmonella y podría aplicarse en seres humanos. Los científicos, en concreto, han puesto en práctica un sistema de nanoencapsulación basado en envoltorios de lípidos para aumentar la eficacia de los bacteriófagos en la terapia fágica (uso de virus para combatir bacterias nocivas) oral. La investigación ha demostrado que la nanoencapsulación lipídica confiere a los bacteriófagos una mayor resistencia a la acidez del estómago y aumenta su tiempo de residencia en el tracto intestinal en un modelo de pollos de engorde que simula las condiciones de las granjas de producción aviar. La tecnología desarrollada podría aplicarse a bacteriófagos con diferentes morfologías para su uso en terapia fágica, tanto en animales como en seres humanos.
“Los lípidos soportan mejor el efecto deletéreo de la acidez que las proteínas”
Los bacteriófagos son, fundamentalmente, entes biológicos que constan de DNA dentro de una envuelta proteica que protege a este material genético, y también están formados por unas estructuras proteicas, denominadas colas, que les sirven para reconocer a las células bacterianas que infectan. En definitiva, están compuestos básicamente por proteínas y DNA. “Ello hace que sean susceptibles a desestructurarse en condiciones ambientales diversas, como puede ser la acidez del medio, con lo cual pierden su capacidad de infectar y matar a las bacterias. Por ello, la aplicación de bacteriófagos como agentes terapéuticos por vía oral es más eficaz si estos entes biológicos están protegidos de alguna manera. La obtención de cápsulas lipídicas que contienen bacteriófagos les confiere a estos entes una mayor resistencia al efecto deletéreo de la elevada acidez estomacal, a la vez que les permite permanecer más tiempo en el intestino, dado que los lípidos pueden adherirse con mayor facilidad que los propios bacteriófagos a las paredes intestinales. La razón de ello se debe a que los lípidos soportan mejor el efecto deletéreo de la acidez que las proteínas”, explica la experta.
“La mayoría de serovariedades de Salmonella -señala Llagostera- que provocan salmonelosis en el hombre no producen ningún efecto sobre los pollos de engorde y otros animales de producción aviar. Entre estas bacterias debe distinguirse entre las tifoideas y las no tifoideas. Para que se hagan una idea sobre la importancia de Salmonella no tifoidea como patógeno, indicarles que se estima que estas bacterias, en un solo año, son las responsables de 94 millones de gastroenteritis en humanos en todo el mundo, con el resultado de 155.000 muertes; además, aproximadamente unos 80 millones de casos han adquirido dicha enfermedad por la ingestión de alimentos contaminados”. Los cuadros de gastroenteritis en el hombre cursan con fiebre que se resuelve en 24-48 h y diarrea, que puede persistir durante varios días. Esta sintomatología puede ser mucho más grave en recién nacidos, niños, personas de edad avanzada o inmunocomprometidas.

Profesora Montserrat Llagostera Casas
Fuente: Prof. Llagostera
La Unión Europea, decididamente comprometida contra la Salmonella
“Dado que los pollos y otros animales de producción aviar son el principal reservorio de estas bacterias, nuestro objetivo ha sido estudiar si la terapia fágica oral es efectiva para reducir o erradicar Salmonella en este tipo de animales, ya que ello tendrá un efecto en la salmonelosis no tifoidea en humanos. Además, debe también tenerse en cuenta que la Unión Europea está decididamente comprometida con la erradicación de Salmonella en las explotaciones animales y para ello se han implementado diversos reglamentos de obligado cumplimiento por parte de los estados miembros. Por ello, hemos trabajado con un modelo de pollo de engorde, contaminado experimentalmente con la serovariedad no tifoidea Salmonella enterica Typhimurium, en condiciones que simulan las de las granjas de producción de este tipo de animales. Nuestros resultados han demostrado que la administración por vía oral de bacteriófagos encapsulados a estos animales reduce muy significativamente la concentración de esta bacteria en su intestino (ciego) y este efecto se prolonga mucho más en el tiempo que si se les trata con bacteriófagos no encapsulados”, subraya la catedrática.
La terapia oral con bacteriófagos ha demostrado ser una herramienta factible y eficaz para el control de infecciones causadas por diferentes patógenos bacterianos. En estudios anteriores, el Grupo de Microbiología Molecular de la UAB publicó el aislamiento y la caracterización de tres bacteriófagos virulentos (UAB_Phi20, UAB_Phi78, y UAB_Phi87) específicos para Salmonella, y mostró su eficacia en la reducción de la concentración de esta bacteria zoonótica en un modelo de pollitos White Leghorn libres de patógenos específicos (SPF), y en diversas matrices alimentarias contaminadas experimentalmente. No obstante, en esa investigación se observaron dos limitaciones en el uso de los bacteriófagos en la terapia oral: la reducida estabilidad de los bacteriófagos en ambientes extremadamente ácidos, como el del estómago, y su bajo tiempo de residencia en el tracto intestinal.
Con el fin de superar estas limitaciones, los investigadores han desarrollado ahora un sistema de nanoencapsulación basado en cápsulas de lípidos (liposomas) que han aplicado a los tres bacteriófagos virulentos mencionados para poder comparar el efecto de los bacteriófagos encapsulados y los no encapsulados en la disminución de la concentración de Salmonella en un modelo de pollos de engorde infectados experimentalmente. La experimentación se ha llevado a cabo en el Servicio de Granjas y Campos Experimentales de la UAB simulando las condiciones de una granja real.
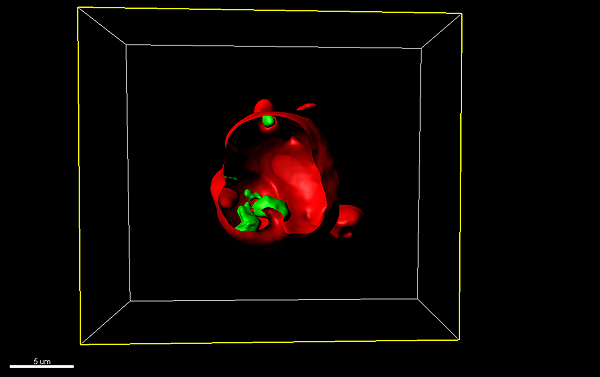
Imagen de microscopía confocal de nanocápsulas de liposomas que contienen bacteriófagos
Fuente: UAB
Cápsulas a escala nanométrica con un diámetro medio de 320 nm
A raíz de este estudio se han elaborado cápsulas a escala nanométrica con un diámetro medio de 320 nm y una carga positiva de 33 mV. Las nanocápsulas que contienen los bacteriófagos han sido observadas por criomicroscopía electrónica (Cryo-TEM) y por microscopía confocal. Los investigadores han observado como el recubrimiento con lípidos permite que los bacteriófagos encapsulados sean significativamente más estables en los fluidos gástricos. El recubrimiento también mejora significativamente la retención de los bacteriófagos en el tracto intestinal de los pollos de engorde. Después de 72 horas se detectaron bacteriófagos encapsulados en el 38,1% de los animales, mientras que los no encapsulados fueron detectados sólo en el 9,5% de los ejemplares. En experimentos de terapia oral, una vez que el tratamiento se detuvo, la protección conferida por los bacteriófagos no encapsulados desapareció, mientras que la proporcionada por los bacteriófagos encapsulados persistió durante al menos una semana.
La nueva metodología permite la encapsulación de bacteriófagos de diferente tamaño y morfología, demuestra las ventajas de utilizar bacteriófagos encapsulados en la terapia fágica oral y, gracias a su tamaño nanométrico, posibilita su adición al agua potable y al pienso para los animales.
A pesar del éxito del experimento, la profesora de la UAB no quiere lanzar las campanas al vuelo y dar por solucionada la amenaza de la Salmonella: “La lucha contra la salmonelosis es muy compleja y requiere una aproximación multifactorial. La propia Unión Europea, y por ende todos sus estados miembros, están comprometidos al máximo en esta lucha. El lema que se acuñó en su momento fue que la lucha contra la salmonelosis debe realizarse de forma integrada bajo el lema ‘de la granja a la mesa’. Fíjense que este lema ya indica que debe actuarse tanto a nivel de producción animal (y específicamente en producción aviar, ya que es el principal reservorio), como a lo largo de toda la cadena alimentaria, lo que incluye transporte de animales, mataderos y empresas que producen alimentos, e incluso actuar también en restauración y en los propios hogares”.
Según la profesora Llagostera, “la administración de antibióticos para el tratamiento de la salmonelosis no tifoidea en el hombre sólo es recomendable en casos graves. En los demás, se debe controlar esta enfermedad a base de una dieta e hidratación adecuadas. Y, por supuesto, no deben utilizarse antibióticos para prevenir la contaminación de animales con Salmonella. El mal uso de antibióticos conlleva la selección y emergencia de cepas bacterianas resistentes a los mismos, lo cual compromete su futura utilización”.
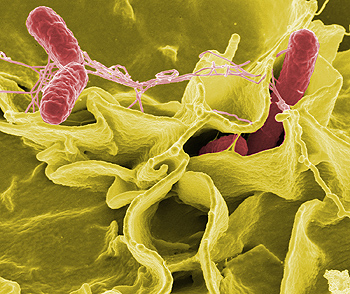
Microscopía electrónica de Salmonella typhimurium
Autor/a de la imagen: Rocky Mountain Laboratories, NIAID, NIH (User: Taragui)
Fuente:Wikpiedia
“Los bacteriófagos no son la solución definitiva, en mayúsculas, frente a la Salmonella”
“Combatir la salmonelosis requiere de muchas medidas. Entre ellas, cabe destacar las mejoras en la higienización de los sistemas de producción de animales y de productos derivados de ellos, la vacunación de los animales contra Salmonella, y los controles microbiológicos frecuentes para detectar a este patógeno antes de que llegue al hombre. La aplicación de estas y otras medidas ha conseguido una disminución de Salmonella en los animales, su reservorio, si bien no se ha conseguido su erradicación. Por ello, se requieren nuevas herramientas con las que conseguir disminuir más la prevalencia de este patógeno en granjas y en toda la cadena alimentaria. Los bacteriófagos, específicos contra estas bacterias, son una de estas herramientas que, además, puede aplicarse tanto en animales como en la cadena de producción de alimentos derivados de ellos, e incluso en restauración y en nuestro hogares. No obstante, teniendo en cuenta la complejidad de la lucha contra Salmonella, no puede pensarse que los bacteriófagos sean la solución definitiva, en mayúsculas, a este problema”, admite la investigadora.
Sea como fuere, el hallazgo de los científicos de la UAB y del ICN2 permite exclamar en voz alta que, a partir de ahora, los patógenos bacterianos -y no sólo la Salmonella- lo van a tener mucho más crudo a la hora de realizar progresos. “La tecnología de encapsulación que hemos desarrollado es válida para bacteriófagos con distintas morfologías y puede aplicarse a bacteriófagos específicos contra patógenos bacterianos muy diversos. Mi opinión es que la nanoencapsulación de bacteriófagos en envueltas lipídicas puede ser de gran ayuda para aplicar con éxito una terapia fágica administrada por vía oral contra enteropatógenos bacterianos, tanto en el hombre como en animales. Además, también puede ser útil para mejorar la eficacia de esta terapia si debe aplicarse en ambientes que puedan tener algún efecto deletéreo sobre los bacteriófagos”, asegura Llagostera.
La investigación sobre nanoencapsulación lipídica se ha llevado a cabo conjuntamente por el grupo de Microbiología Molecular del Departamento de Genética y Microbiología de la UAB, dirigido por Montserrat Llagostera, y el grupo Supramolecular Nanochemistry & Materiales del ICN2, dirigido por el profesor ICREA Daniel Maspoch. El trabajo ha sido publicado recientemente en la revista ‘Applied and Environmental Microbiology’ y es parte del trabajo de la tesis doctoral con mención internacional de Joan Colom Comas titulada "Studies of the molecular features of three Salmonella Phags for use in phage therapy and of encapsulation methodologies tono improve oral phage administration", han informado desde la UAB.
Referencias
1. Organización Mundial de la Salud (OMS). ‘Salmonella (no tifoidea)’. Nota descriptiva Nº139 Agosto de 2013 [http://www.who.int/mediacentre/factsheets/fs139/es/]
2. Colón J, Cano-Sarabia M, Otero J, Cortés P, Maspoch D, Llagostera M. liposome-Encapsulated bacteriophages for enhanced oral phage therapy against Salmonella. Applied and Environmental Microbiology (2015) doi: 10.1128 / AEM.00812-15.




