Introducción

Jordi Giner Donaire
Fuente: Archivo
La vía inhalatoria es la de elección para la administración de fármacos inhalados ya que administra los medicamentos directamente en los pulmones. Las ventajas que aporta la administración por vía inhalada son: permite administrar una dosis más baja de fármaco en comparación con la vía oral, y los efectos secundarios por tanto se reducen al mínimo; además el inicio de la acción es más rápido que cuando se administran por vía oral.
Para su administración existe una amplia gama de dispositivos disponibles: los inhaladores presurizado de dosis medida (pMDI), solos o con cámara de inhalación, los dispositivos de polvo seco (DPI) y los nebulizadores.
El éxito de la terapia inhalada depende de diferentes parámetros relativos al paciente como la edad, el estado de las vías aéreas, y relativos al propio dispositivo como son las características de la nube que genera, dosis del fármaco y su distribución y depósito en el pulmón. Para cada uno de los diferentes dispositivos es necesaria una técnica específica y en muchos casos distinta (1-3), para lograr una dosis efectiva (4). La mayoría de los dispositivos existentes son eficaces si se usan de forma correcta (1), sin embargo el uso incorrecto de estos dispositivos de inhalación reduce su eficacia clínica (3, 4, 5, 6) y por tanto el control de la enfermedad.
Tipos de dispositivos y sus principales características
Los dispositivos pMDI fueron los primeros comercializados y aún continúan siendo los más utilizados. Para generar el aerosol utiliza propelentes del tipo Clorofluorocarbonos o Hidrofluoroalkenos. Por ello sus características técnicas como la velocidad de salida de las partículas del aerosol, de alrededor de 25 km / hora que, combinado el tamaño de las partículas, hace que un gran porcentaje de la dosis de aerosol generado, entre el 50 y el 80% se deposite en la orofarínge y llegue poca cantidad a los pulmones, no más de un 10%. Por ello es necesario que el paciente tenga que utilizar una técnica de inhalación correcta para que sea eficaz.
El aspecto más comprometido de la técnica de utilización de los pMDI es la coordinación entre la actuación del dispositivo y la inhalación, siendo el error más habitual (7) en su utilización y un problema común en los niños y gente mayor. La falta de coordinación provoca una inhalación demasiado temprano o demasiado tardía (8, 9), con escasa o nula llegada del aerosol al pulmón.
Una alternativa a este problema es la utilización de cámaras de inhalación, lo que elimina la necesidad de coordinación (1), aumentando considerablemente el aporte de fármaco al pulmón. Pero el tamaño de las cámaras las reduce al uso domiciliario. Otra alternativa a estos dispositivos son los inhaladores de polvo seco. Estos utilizan la fuerza y el volumen generado por la inspiración del paciente para generar el aerosol, que contiene las partículas de fármaco, evitando así la coordinación entre la liberación de dosis y la inhalación. En estos dispositivos el fármaco está en partículas micronizadas (rango de tamaño de 1-5 µm) agregadas a un vehículizante de tamaño de partícula mucho más mayor, la lactosa (partículas de tamaño de alrededor de 25 µm).
Estos dispositivos están diseñados para que el fármaco y el vehículizante se desaglomeren (se separen) durante la maniobra de inhalación. Este fenómeno depende en gran medida del flujo del aire inspirado y de la capacidad pulmonar, parámetros que difieren de paciente a paciente. Esta variabilidad en el flujo y en el volumen inspiratorio hace que la dosis inhalada pueda variar entre pacientes y en algunos casos ser relativamente baja o nula (10).
Finalmente disponemos de los nebulizadores, en sus diferentes versiones (Jet, ultrasónicos, de malla vibrante). La ventaja es que no requieren de maniobras especiales para su utilización, basta con una respiración normal para poder inhalar el fármaco generado. Pero el gran inconveniente de estos dispositivos es que precisan de una fuente de energía externa (aire comprimido, electricidad) para su funcionamiento y la poca disponibilidad farmacológica existente.
Un "nebulizador" de bolsillo
Una alternativa a todos estos dispositivos sería un dispositivo de bolsillo capaz de aerosolizar una solución de fármaco que pueda ser inhalada sin la dependencia de la coordinación y del flujo inspiratorio y que genere un aerosol respirable parecido al que producen los nebulizadores, pero sin la necesidad de fuentes de energía externas. Este es el caso del Respimat® Soft Mist ™ Inhalador (SMI), que se basa en la aerosolización de la solución de fármaco en forma de niebla fina. El aerosol se forma por una fuerza mecánica generada por un muelle que hace que se comprima una cantidad de 15µL de solución procedente del depósito del dispositivo.
Al pulsar un botón del disparador, suelta el resorte del muelle forzando la solución a atravesar el “uniblock”. Esta pieza consiste en un cristal de silicio, de unas dimensiones de 2,5 x 2 x 1,1 mm³, que mediante el uso de técnicas de grabado fotolitográficas forma unos microcanales de unos 5 x 8 µm² a través de los cuales pasa la solución. Estos canales convergen en dos salidas de líquido, situados uno enfrente del otro, en un ángulo que hace que impacten y se desintegre la solución para producir el aerosol. Por este motivo no es necesaria la presencia de propelentes para generar el aerosol (11).
En el diseño del dispositivo Respimat® hay tres parámetros físicos que son particularmente relevantes en cuanto al aerosol generado: el tamaño de partícula, la velocidad de aerosol a la salida del dispositivo y la duración de la nube del aerosol.
• El diseño del dispositivo permite generar un aerosol con aproximadamente el 75% de partículas con un diámetro superior a 1 µm y menores de 5.8 µm, para facilitar un depósito pulmonar eficiente, casi el doble del generado por los pMDI y los DPI (21, 13).
• La velocidad de salida del aerosol es de aproximadamente 0,8 m / seg, en el rango bajo del flujo inspiratorio generado por un paciente durante una maniobra inspiratoria (14) y entre 3 y 10 veces más lento que la velocidad de liberación del aerosol de un pMDI (15). Esta velocidad facilita un aumento del depósito pulmonar y reduce el orofaríngeo.
• La duración de la nube de aerosol es de aproximadamente 1,5 segundos, considerablemente de mayor duración que el del pMDI (de entre 0,15 y 0,36 segundos). Esta mayor duración de la pulverización permite al paciente una mejor coordinación entre la maniobra de inhalación y la liberación del fármaco (Figura 1). (15)

Captura de pantalla 2016-01-07 a las 12.00.43
FIGURA 1
Imagen de la pluma generada por el dispositivo Respimat (abajo)
y por un pMDI (arriba)
Gracias a estas características físicas del dispositivo Respimat® el depósito orofaríngeo es inferior y el aporte pulmonar de fármaco superior a otros dispositivos de inhalación, tal como se indica en la Figura 2 (16).
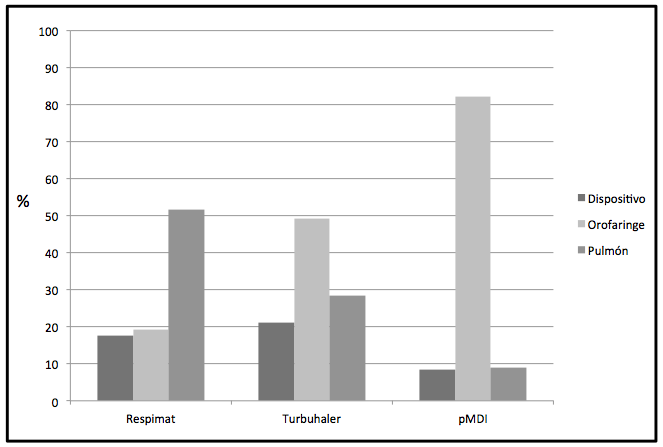
FIGURA 2
Porcentaje de depósito de fármaco en el dispositivo, la orofarínge y el pulmón de los dispositivos Respimat, Turbuhaler y pMDI.
Modificada de Pitcairn et al. (16)
Estas características convierte al Respimat® Soft Mist ™ en un dispositivo presurizado con las características del aerosol generado parecido al que se genera con un "nebulizador", pero portable y sin necesidad de energías externas para su utilización, lo que facilita su utilización en un amplio abanico de pacientes, independientemente de su grado de alteración respiratoria, ya que como indican (17) el dispositivo Respimat puede ser utilizado con cámara de inhalación (Figura 3), en niños incluso de entre 2 y 5 años, y a partir de esta edad directamente, dispensado por los padres o un cuidador. Además su utilización se abre a las nuevas indicaciones del Bromuro de Ipatropio, dispensado con el dispositivo Respimat, en pacientes con asma mal controlada, con una reducción significativa del riesgo de exacerbaciones, proporcionado además una broncodilatación sostenida (18).

FIGURA 3
Imagen del dispositivo Respimat utilizable directamente o conectado a una cámara de inhalación.
Entre las características destacables del dispositivo se puede indicar como ventajas (19):
• No contiene propelentes tipo CloroFluoroCarbonos o HidroFfluoroAlkenos.
• Menor velocidad de salida del aerosol.
• Mayor depósito pulmonar.
• Facilita la coordinación.
• Requiere flujos inspiratorios bajos.
• Contiene un contador de dosis.
• El tapón está integrado al equipo.
Técnica de utilización
La técnica de utilización del dispositivo se divide en dos fases: la carga del dispositivo y la técnica de inhalación propiamente dicha (19). Carga del dispositivo:
• Retirar la base transparente.
• Empujar suavemente el extremo estrecho del cartucho hacia el interior del dispositivo hasta oír un “clic”, asegurar que se ha introducido totalmente.
• Colocar la base transparente.
• En posición vertical (boquilla en la parte superior), girar la base (media vuelta) hasta oír un “clic”.
• Abrir la tapa verde de la boquilla.
• Presionar el botón de liberación de dosis. Repetir esta operación unas 4 a 6 veces, hasta observar que se genera la nube de aerosol. El dispositivo está listo para ser utilizado. Utilización del dispositivo:
• En posición vertical (boquilla en la parte superior), girar la base (media vuelta) hasta oír un “clic”.
• Abrir la tapa de la boquilla.
• Vaciar los pulmones.
• Colocar la boquilla entre los labios y los dientes, evitando que la lengua obstruya la salida de la boquilla.
• Inspirar lentamente hasta que los pulmones estén llenos mientras se presiona el botón de liberación de dosis.
• Aguantar la respiración 10 segundos o tanto como sea posible.
• Si no debe realizar una nueva inhalación tapar el dispositivo.
Conclusiones
El dispositivo Respimat® Soft Mist ™ Inhaler (SMI) es un dispositivo de inhalación de bolsillo que genera un aerosol de solución de fármaco fácilmente inhalable e independiente de las características individuales del pacientes, reproducible y respetuosa con el medio ambiente al no utilizar propelentes.
Las características del aerosol se pueden resumir en:
• Gran cantidad de partículas respirables
• Baja velocidad de salida del aerosol
• Mantenimiento de la nube de aerosol por un tiempo superior al de los pMDI.
Por ello facilita la inhalación por parte del paciente sin requerir maniobras especiales y aportando un alto porcentaje de depósito pulmonar. El dispositivo es utilizable tanto en niños como en personas mayores con una cámara espaciadora.
Bibliografía
1. Dolovich MB, Ahrens RC, Hess DR, Anderson P, Dhand R, Rau JL, Smaldone GC, and Guyatt G: Device selection and outcomes of aerosol therapy: evidence-based guidelines: American College of Chest Physicians/American College of Asthma, Allergy, and Immunology. Chest. 2005;127:335–371.
2. Boe J, Dennis JH, O’Driscoll BR, Bauer TT, Carone M, Dautzenberg B, Diot P, Heslop K, and Lannefors L: European Respiratory Society Guidelines on the use of nebulizers.Eur Respir J. 2001;18:228–242.
3. Ari A, and Fink JB: Guidelines for aerosol devices in infants, children and adults: Which to choose, why and how to achieve effective aerosol therapy. Expert Rev Respir Med. 2011;5:561–572.
4. Melani AS, Bracci LS, and Rossi M: Reduced peak inspiratory effort through the Diskus((R)) and the Turbuhaler((R)) due to mishandling is common in clinical practice. Clin Drug Investig. 2005;25:543–549.).
5. Fink JB, and Rubin BK: Problems with inhaler use: A call for improved clinician and patient education. Respir Care. 2005;50:1360–1374.
6. Kamps AW, van EB, Roorda RJ, and Brand PL: Poor inhalation technique, even after inhalation instructions, in children with asthma. Pediatr Pulmonol. 2000;29:39–42. 7. Sanchis J Corrigan C, Levy M, Viejo JL. Inhaler devices e From theory to practice. Respir Med. 2012;107(4):495-502
8. Newman SP, Pavia D, Clarke SW. How should a pressurized beta- adrenergic bronchodilator be inhaled? Eur J Respir Dis. 1981;62:3–21.
9. Crompton EK. Problems patients have using pressurized aerosol inhalers. Eur J Respir Dis Suppl. 1982;119:101–104.
10. Meakin BJ, Ganderton D, Panza I, Ventura P. The effect of flow rate on drug delivery from the Pulvinal, a high-resistance dry powder inhaler. J Aerosol Med. 1988;11:143–152.).
11. Dalby RN, Eicher J, Zierenberg B, Development of Respimat® Soft MistTM Inhaler and its clinical utility in respiratory disorders. Medical Devices: Evidence Research. 2011;4:145-155
12. Van Noord JA, Smeets JJ, Creemers JP, Greefhorst LP, Dewberry H, Cornelissen PJ. Delivery of fenoterol via Respimat®, a novel soft mist inhaler. Respiration. 2000;67:672–678.
13. Steed KP, Freund B, Towse L, Newman SP. High lung deposition of fenoterol from BINEB, a novel multiple dose nebuliser device [Abstract]. Eur Respir J. 1995;8 Suppl 19:204.
14. Zhang Z, Kleinstreuer C, Kim CS. Micro-particle transport and deposition in a human oral airway model. J Aerosol Sci. 2002;33: 1635–1652.
15. Hochrainer D, Hölz H, Kreher C, Scaffidi L, Spallek M, Wachtel H. Comparison of the aerosol velocity and spray duration of Respimat® Soft Mist™ Inhaler and pressurized metered dose inhalers. J Aerosol Med. 2005;18(3):273–282.
16. Pitcairn G, Reader S, Pavia D, Newman S. Deposition of corticosteroid aerosol in the human lung by Respimat® Soft MistTM Inhaler compared to deposition by Metered Dose Inhaler or by Turbuhaler ® dry powder inhaler. J Aerosol Med. 2005; 18(3): 264-272
17. Kamin W, Frank M, Kattenbeck S, Moroni-Zentgraf, Wachtel H, Zielen S. A handling study to assess use of the Respimat® Soft MistTM inhaler in Children under 5 years old. J Aerosol Med. 2015; 28(5):372-381.
18. Tiotropium in Asthma Poorly Controlled with Standard Combination Therapy. Huib A.M. Kerstjens, M.D., Michael Engel, M.D., Ronald Dahl, M.D., Pierluigi Paggiaro, M.D., Ekkehard Beck, M.D., Mark Vandewalker, M.D., Ralf Sigmund, Dipl.Math., Wolfgang Seibold, M.D., Petra Moroni-Zentgraf, M.D., and Eric D. Bateman, M.D. N Engl J Med 2012; 367:1198-1207September 27, 2012.
19. Consenso SEPAR-ALAT sobre terapia inhalada. Arch Bronconeumol. 2013; 49(Suppl 1):1-14




