Redacción Farmacosalud.com
El Instituto de Investigación Biomédica (IRB Barcelona), en colaboración el Instituto de Oncología Molecular FIRC de Milán (Italia), han identificado a GEMC1 como un gen maestro para generar células multiciliadas, células que son específicas de cerebro, tracto respiratorio y sistema reproductivo. Un defecto en GEMC1 causa un subtipo de ciliopatías conocidas como Enfermedades de Depuración Mucociliar, unas enfermedades raras poco investigadas. Según el doctor Travis Stracker, jefe del Laboratorio de Inestabilidad Genómica y Cáncer de IRB Barcelona, dado que las Enfermedades de Depuración Mucociliar son de origen genético, el descubrimiento acerca de GEMC1 abre las puertas a estudios genéticos que, enmarcados en la medicina predictiva, puedan ayudar a discernir si una pareja corre el peligro de tener un/a descendiente con esa clase de patologías: “Actualmente no hay revisiones generalizadas para ciliopatías en mujeres embarazadas. Sin embargo, en las familias en riesgo, GEMC1 y muchos otros genes que hemos identificado podrían ser examinados para determinar el riesgo de que los niños tengan una ciliopatía”.
Doctor Travis Stracker
Fuente: IRB Barcelona
Travis Stracker y su equipo han presentado en ‘EMBO Journal’, en colaboración con el laboratorio de Vincenzo Costanzo del Instituto de Oncología Molecular FIRC de Milán, un trabajo con ratones[1] donde descubren a GEMC1 como un gen candidato para diagnosticar un subtipo de ciliopatía humana. GEMC1 es indispensable para generar células multiciliadas, específicas de tejidos como cerebro, tráquea, pulmones y oviductos. La superficie de las células multiciliadas está cubierta por centenares de cilios, han indicado desde IRB Barcelona. Estas delgadas estructuras, parecidas a los cabellos, sirven para hacer circular el líquido cerebroespinal, limpiar de mucosa las vías respiratorias y trasportar óvulos por los oviductos, entre otras funciones. Los defectos en la generación o función de estas células producen un subtipo de ciliopatías, las mencionadas Enfermedades de Depuración Mucociliar (Mucociliary Clearance Disorders en inglés).
“Con el tiempo vamos a encontrar pacientes con mutaciones GEMC1”
En concreto, los investigadores de IRB y el Instituto FIRC han reproducido en ratones los síntomas de una enfermedad (una ciliopatía) denominada RGMC*, una patología que causa hidrocefalia, infecciones respiratorias graves e infertilidad. El trabajo encabezado por la estudiante de doctorado del IRB Barcelona, Berta Terré y el investigador postdoctoral Gabriele Piergiovanni, reporta que GEMC1 está regulando los dos únicos genes conocidos hasta ahora para diagnosticar esta enfermedad, Multicilin y Cyclin O, lo que lo convierte en otro buen candidato de diagnosis para RGMC.
“Hasta el momento, no se han identificado pacientes con mutaciones en GEMC1. En base a los hallazgos, predecimos que con el tiempo vamos a encontrar pacientes con mutaciones GEMC1, ya que este gen controla la expresión de MCIDAS y CCNO, los 2 genes identificados hasta el momento en el subtipo RGMC. Nuestros ratones imitan muchas de las patologías asociadas a las mutaciones de MCIDAS y CCNO en los seres humanos, por lo que representan un posible modelo para la comprensión de las bases de la enfermedad y probar estrategias de tratamiento”, aduce Stracker en declaraciones a www.farmacosalud.com.
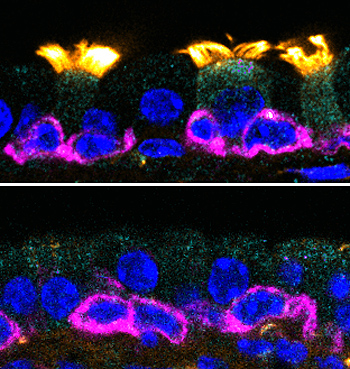
GEMC1 es necesario para generar células multiciliadas. Imágenes de las tráqueas de ratones. Los cilios (en amarillo) son notorios en los modelos con el gen (sup.), mientras que los modelos que no lo tienen, carecen de ellos
(Berta Terré, IRB Barcelona)
Fuente: IRB Barcelona
Así pues, la reproducción de los síntomas de RGMC se ha llevado a cabo en modelos animales. ¿Cuándo se abordará la investigación en humanos? Según el científico, “vamos a seguir adelante con el intento de utilizar nuestro modelo de enfermedad para tratar de explorar algunos enfoques terapéuticos, pero probablemente pasarán muchos años antes de que tengamos un enfoque eficaz para el tratamiento de este tipo de enfermedades”.
Identificar al gen causante para comprender cómo se puede tratar al paciente
De acuerdo con el investigador, “la aplicación más directa de nuestro trabajo para los pacientes humanos es a nivel de diagnóstico. Hemos encontrado GEMC1 y muchos otros genes que creemos que están implicados en la formación y función de cilios móviles que no han sido previamente identificados por otros estudios. Estos genes actualmente no se están estudiando como posibles genes de la enfermedad y podrían añadirse a screenings de detección de ciliopatía. La identificación del gen causante es fundamental para la comprensión de cómo se puede tratar al paciente en particular. Además, ayudará al tratamiento con potenciales tecnologías de edición génica utilizando CRISPR/CAS9, que está recibiendo mucha atención en el momento”.
El hallazgo de los investigadores de IRB Barcelona y FIRC es doblemente importante, porque aparte de abrir las puertas a una posible medicina predictiva en ciliopatías, incide en un tipo de enfermedades raras muy poco estudiadas hasta el momento. “Como las ciliopatías -señala Stracker- son enfermedades raras, que además también son muy diversas en cuanto a las mutaciones que las causan y en cuanto a los espectros patológicos, no representan un objetivo atractivo para la investigación clínica comercial. Hay, simplemente, un mercado más pequeño que para la fibrosis quística u otros síndromes respiratorios. Por lo tanto, hay mucha menos investigación clínica que para otras enfermedades”.
Sin embargo, “la buena noticia es que hay una cantidad cada vez mayor de investigación básica en curso centrada en los cilios. Nuestro trabajo no hubiera sido posible si no hubiera sido por muchas observaciones anteriores de muchos otros grupos de investigación. Aunque el nuestro es un avance significativo, no diría en absoluto que es el más importante que se ha hecho. También es importante reconocer que otros grupos han informado recientemente de hallazgos similares en GEMC1 en ratones, peces y ranas. En cada resultado científico (o en cada artículo) hay una cierta superposición de información, pero también hay en cada uno algunos datos únicos que ayudan a ampliar nuestro conocimiento. Espero que nuestros resultados colectivos ayudarán a futuros estudios y contribuirán al diagnóstico en la clínica”, establece Stracker, quien tiene la esperanza de que todo ello permita "encontrar tratamientos para estas enfermedades graves”.
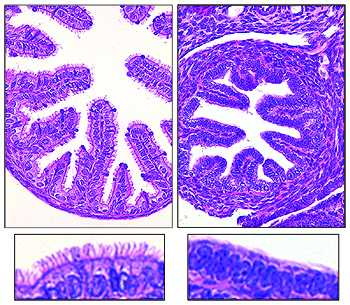
Los oviductos de los ratones con el gen GEMC1 (izquierda) están recubiertos con células multiciliadas, totalmente ausentes en los ratones que carecen del gen
(Berta Terré, IRB Barcelona)
Fuente: IRB Barcelona
Por cierto, el equipo de este científico examinaba GEMC1 por la función del gen en la replicación del ADN y su potencial contribución en cáncer, por lo que el hallazgo relativo a las ciliopatías ha sido cuando menos inesperado. En lo concerniente a la investigación sobre GEMC1 y el cáncer, el jefe del Laboratorio de Inestabilidad Genómica y Cáncer de IRB Barcelona comenta que actualmente se encuentran “en una fase muy temprana” del estudio. “Sin embargo, creemos que nuestro trabajo y estudios anteriores podrían indicar que GEMC1 puede ser importante para controlar la replicación en algunos tipos de cáncer. Esperamos usar el conocimiento que hemos adquirido sobre sus funciones y su regulación para explorarlo más a fondo en un futuro próximo”, afirma.
CRISPR-Cas9, en varios proyectos sobre enfermedades raras
La tecnología que Stracker citaba anteriormente, la CRISPR-Cas9, ha centrado la atención de la IX Reunión Anual del Centro de Investigación Biomédica en Red de Enfermedades (CIBERER), dependiente del Instituto de Salud Carlos III [Madrid]. En el encuentro se han presentado diversos proyectos que utilizan esta revolucionaria herramienta de edición genética, en este caso para la investigación de enfermedades raras. De hecho, existe un colaborativo de 7 grupos de investigación del CIBERER que utiliza CRISPR-Cas9 para generar modelos celulares y animales de 12 enfermedades raras neurosensoriales que producen alteraciones en la visión o la audición. El objetivo es comprender los mecanismos moleculares de estas patologías y poder así comenzar a trabajar en el desarrollo de terapias.
"La edición genómica con las herramientas CRISPR-Cas9 ha impactado de forma extraordinaria en la investigación en enfermedades raras. La versatilidad, facilidad y rapidez con la que es posible ahora desarrollar nuevos modelos celulares y animales, más específicos de las enfermedades raras investigadas, y más ajustados a las alteraciones genéticas observadas en la población humana, deberá permitir avanzar de forma muy significativa en nuestro conocimiento de dichas patologías", explica el doctor Montoliu, investigador del CIBERER en el Centro Nacional de Biotecnología-CSIC.

Imagen de la Reunión Anual del CIBERER
Fuente: Jordi Play/ CIBERER / CIBER
Como ejemplos de utilización de la tecnología CRISPR-Cas9 para la investigación de patologías minoritarias figura el análisis funcional de las variantes genéticas en la anemia de Fanconi, la identificación del papel de dos genes en la retinitis pigmentosa, el restablecimiento del defecto genético en la aciduria glutárica mediante la inserción dirigida de un gen responsable de esta enfermedad, y la generación de células mutantes que puedan ayudar a comprender el síndrome de Ellis-van Creveld y una variante suya, la disostosis acrofacial de Weyer, han informado desde el Centro de Investigación Biomédica en Red (CIBER).
‘Playa y montaña’, un cortometraje que sensibiliza sobre las enfermedades raras
La Fundación Mehuer, dedicada a fomentar la investigación y la divulgación en torno a las enfermedades raras y los medicamentos huérfanos, ha presentado el cortometraje ‘Playa y montaña’, una pieza dirigida por el actor, director y productor Emilio Aragón a partir de una idea original de la agencia ‘Crepes&Texas’ y creada para promover una mayor sensibilización en torno a las patologías de baja prevalencia, que tan sólo en España afectan a unos tres millones de personas.
El vídeo, en cuya creación han trabajado más de 100 personas, cuenta la historia de unos padres que esperan la llegada de un hijo. El embarazo lo viven como si de la preparación de un viaje a un lugar idílico (en este caso, una playa) se tratara, aunque en el proceso sus planes se ven contrariados. En vez de a la playa se ven obligados a conducir sus pasos hacia la montaña, con los obstáculos que ello conlleva. Esa reorientación de destino se utiliza como símil para narrar el desenlace del embarazo, ya que finalmente tienen una hija afectada por una patología minoritaria.
“La historia narra perfectamente cómo muchos padres viven un inesperado revés en la vida al tener un hijo afectado por una enfermedad rara. Lo que en principio parece siempre un viaje idílico hacia la playa se convierte posteriormente en toda una historia de superación, en la proeza de superar esta montaña dura y desconocida hacia la que les ha conducido la vida”, explica Manuel Pérez, presidente de la Fundación Mehuer. “Pese a todo”, prosigue Pérez, “en ese viaje duro e inesperado también hay lugar para la belleza, para la alegría y las satisfacciones”, asevera el también presidente del Colegio de Farmacéuticos de Sevilla, colaborador en la fundación de FEDER y miembro del Consejo Asesor de Sanidad en el grupo de trabajo de las enfermedades raras.
* RGMC (en inglés, Reduced Generation of Multiple Motile Cilia)
Referencias
1. GEMC1 is a critical regulator of multiciliated cell differentiation. Berta Terré, Gabriele Piergiovanni, Sandra Segura-Bayona, Gabriel Gil-Gómez, Sameh A. Youssef, Camille Stephan-Otto Attolini, Michaela Wilsch-Bräuninger, Carole Jung, Ana M. Rojas, Marko Marjanović, Philip A. Knobel, Lluís Palenzuela, Teresa López-Rovira, Stephen Forrow, Wieland B. Huttner, Miguel A. Valverde, Alain de Bruin, Vincenzo Costanzo and Travis H. Stracker. EMBO Journal (2016) 10.15252/embj.201592821




