Redacción Farmacosalud.com
La Clínica Universidad de Navarra ha puesto en marcha el primer chequeo genómico que se realiza en España. El proceso de secuenciación genómica se lleva a cabo a partir del análisis de una muestra de sangre y sus resultados ofrecen información acerca de cuestiones de salud relevantes, como los riesgos de desarrollar diferentes tipos de enfermedades y de compartir este riesgo con los familiares, o bien sirve para aproximar el modo en que el paciente responderá previsiblemente a determinados fármacos. Contrariamente a lo que pueda pensarse, el nuevo test no está indicado para la población infantil, por más que pueda deducirse que, con la información obtenida mediante esas pruebas, la medicina podría anticiparse a la posible aparición de determinadas enfermedades en el presente del niño, y en el futuro cuando dicho menor alcance la edad adulta. Así pues, el novedoso procedimiento está indicado cuando el posible paciente ya ha alcanzado la mayoría de edad, y obviamente en edades posteriores.
“Existe una gran controversia sobre qué test genéticos hacer y cuándo realizarlos a los niños, pero está universalmente aceptado que los test a los niños han de hacerse cuando hay síntomas, es decir, cuando se sospecha de una determinada enfermedad y, desde luego, cumpliendo dos condiciones: 1) que la patología que se va a estudiar genéticamente pueda ser diagnosticada durante la pediatría, epidemiológicamente hablando, es decir, que sea una enfermedad del menor y 2) que la realización del test vaya a aportar alguna ventaja al niño- que es el paciente-, no al progenitor. Si se desea respetar y proteger la autonomía del paciente pediátrico actual, que será un paciente adulto futuro, no hay que realizar test genéticos presintomáticos a los niños. Otra cosa muy diferente es si se sospecha enfermedad, pero en este caso el test genético estará orientado y no será un genoma completo a un niño sano”, argumenta a través de www.farmacosalud.com la Dra. Ana Patiño, catedrática en genómica y directora de la Unidad de Genómica de la Clínica Universidad de Navarra.

(de izq. a dcha) Drs. Óscar Beloqui, Ana Patiño y Luis Izquierdo
Fuente: Clínica Universidad de Navarra
El estudio incluye información sobre 225 enfermedades de origen genético
“El chequeo genómico no es útil para el niño sano, tal y como lo hemos orientado en la Clínica Universidad de Navarra. Pero, por supuesto, será útil para tomar decisiones reproductivas cuando esos niños sean adultos. Por eso, si lo desean, a partir de la mayoría de edad o cuando deseen tener familia podrían realizarse el test, ya que el estudio del genoma incluye información sobre 225 enfermedades de origen genético de las que se puede ser portador sin manifestar la enfermedad, y, si dos portadores de alteración en el mismo gen (que no saben que lo son porque no tienen síntomas) tienen hijos, éstos manifestarán la enfermedad condicionada por ese gen con una probabilidad del 25%”, detalla Patiño. En definitiva, el novedoso chequeo es totalmente recomendable en caso de que se quieran identificar posibles problemas de salud que pudieran ser transmitidos a la futura descendencia de la persona que se somete a las pruebas.
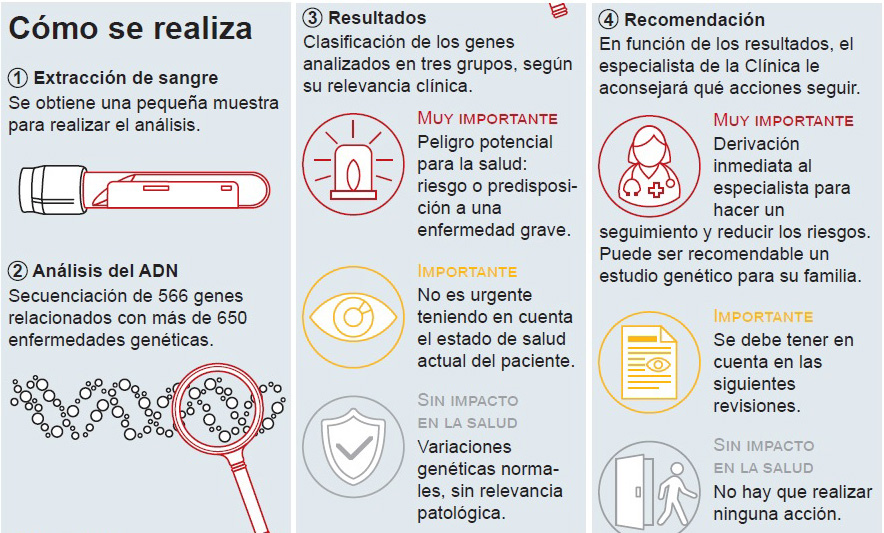
El chequeo genómico que han puesto en marcha varios especialistas de las unidades de Genómica y de Chequeos de la Clínica Universidad de Navarra consiste en la realización de un examen médico completo que incluye un test de secuenciación genómica con el que se obtiene información sobre más de 650 enfermedades y rasgos de origen genético. Esta prueba de secuenciación del genoma completo –ofrecida de la mano de Veritas Intercontinental- es la base del chequeo genómico, que analiza el ADN individual y aporta información genética sobre cerca de 566 genes relacionados con esas más de 650 enfermedades con relevancia clínica, además de información sobre diferentes cualidades genéticas, un planteamiento impensable hace apenas unos años, tanto desde el punto de vista técnico, como desde el económico.
El principal aspecto diferencial del novedoso test reside en la combinación de este extenso análisis genético con un examen general de salud, lo que se entiende por un chequeo convencional. Unas pruebas diagnósticas que, en el caso de la Clínica, incluyen una exploración completa mediante un avanzado TAC de cuerpo entero, es decir, mediante un equipo de tomografía espectral de dosis ultra baja, recién adquirido por el centro hospitalario.
Minimizar o anticiparse… hacer, por tanto, medicina predictiva
En detalle, el chequeo genómico consiste en una evaluación médica específica, que incluye la secuenciación del genoma y su interpretación, además de una consulta con un especialista en Medicina Interna, una analítica completa, un TAC de cuerpo entero con el nuevo equipamiento de ultra baja radiación y un informe con la valoración final; estas últimas, pruebas propias de un chequeo médico convencional. A modo de aval del procedimiento, figuran la trayectoria profesional de la propia Dra. Patiño, y la experiencia de más de 20 años de la Unidad de Chequeos del mismo centro hospitalario, que cuenta con más de 60.000 exámenes completos.
©2019 Clínica Universidad de Navarra
Infografía: Fundamentium
Difusión: Clínica Universidad de Navarra
El conjunto de procedimientos médicos que se agrupan bajo el paraguas del chequeo genómico sirve, en definitiva, para analizar el estado de salud actual del individuo estudiado, a la vez que ofrece información sobre la predisposición genética del paciente. La obtención de estos datos ayuda a predecir estados de salud y a tomar decisiones médicas a la vista de los resultados recogidos, con el objetivo de minimizar o anticiparse a las condiciones que la genética anuncia. En definitiva, ayuda a hacer, por tanto, una medicina predictiva.
Para el director de la Unidad de Chequeos de la Clínica, el Dr. Óscar Beloqui, la importancia del chequeo genómico radica en “la posibilidad de reducir en algunas ocasiones el riesgo asociado a las mutaciones genéticas al aplicarse medidas de seguimiento, tratamiento y/o cambios de estilo de vida asociados con el riesgo” detectado.
La importancia de la interpretación de los datos obtenidos
La información que aportan los resultados del test genético es permanente, ya que no experimenta cambios sustanciales con el paso del tiempo y, aunque actualmente se desconoce el significado de muchas de las variantes identificadas, permite al experto en genómica evaluar la mayoría de los genes importantes para la salud. Además, a medida que se identifiquen nuevas asociaciones entre la genética y la patología o bien cambie su interpretación, “podremos actualizar la relevancia clínica de los datos genéticos y actuar de nuevo sobre genes secuenciados hace meses o años”, señala a través de un comunicado la Dra. Patiño.
No obstante, “la clave de la secuenciación del genoma no está tanto en la obtención de la información como en la interpretación de esos datos genéticos. Eso es lo clínicamente relevante y lo que va a repercutir en la salud del paciente”, subraya. Por eso, el especialista asignado deberá informar al paciente de las variantes que suponen riesgo de enfermedad y asesorarle para que tome las medidas oportunas. En este sentido, el Dr. Luis Izquierdo, director médico de Veritas Intercontinental, remarca que “cada genoma es único; es nuestro manual personal e irrepetible y contiene una ingente cantidad de información sobre nosotros. Esta combinación de individualidad y riqueza de datos hace que la genómica sea extremadamente poderosa y se constituya como la base de una nueva medicina: la medicina individualizada o personalizada, también denominada medicina de precisión, complementando a la perfección el actual chequeo médico de la Clínica y ofreciendo a sus pacientes el acceso a esa nueva concepción de la medicina.”
El análisis del ADN aporta información sobre esas más de 650 enfermedades de origen genético, de las cuales más de 225 son potencialmente hereditarias, es decir, se pueden haber heredado de los padres y se pueden transmitir a los hijos. Entre ellas, se pueden encontrar algunos tipos de cáncer (como determinados tumores de cáncer de colon o de mama), enfermedades cardiovasculares y alteraciones del sistema inmune. Además, el mencionado análisis también aporta información sobre la eficacia y toxicidad de más de 150 fármacos usados para tratar diferentes patologías.
A la hora de gestionar la información genómica, la Clínica cuenta con la plataforma Arvados. Desarrollada inicialmente en la Facultad de Medicina de la Universidad de Harvard, la plataforma permite almacenar, gestionar y procesar los datos genómicos, de imagen y biomédicos, de manera eficiente. Arvados incluye la información genómica de los pacientes de forma anónima, con el objetivo de proporcionar información muy útil para los diferentes grupos de investigación, así como para aportar valor en la clasificación de las variantes genéticas.
Información relevante acerca de varias afecciones
Aunque los resultados de la secuenciación genómica los deberá interpretar siempre el especialista, se exponen a continuación algunos ejemplos de enfermedades de las que se puede detectar un riesgo potencial.
• Alzheimer
• Cáncer de páncreas
• Cáncer colorrectal
• Cáncer de mama y ovario
• Cáncer de próstata
• Melanoma
• Niveles de vitaminas
• Riesgo de muerte súbita (miocardiopatía hipertrófica)
• Riesgo de tromboembolismo venoso
• Riesgo de lesión de ligamentos
• Riesgo de lesión en tendón de Aquiles, entre otras lesiones




