Dr. Jose Luis López Estebaranz
Introducción
La psoriasis es una enfermedad inflamatoria crónica y recurrente de la piel que afecta en torno al 2.3% de la población española y que impacta de forma negativa en la calidad de vida de los pacientes que la padecen[1]. En sus formas moderadas y severas asocia con más frecuencia ciertas comorbilidades como la artropatía, hipertensión, obesidad, hiperlipemia, síndrome metabólico y enfermedad cardiovascular.
Los fármacos utilizados en el manejo de la psoriasis moderada severa incluyen los denominados fármacos sistémicos clásicos (metotrexato, ciclosporina y acitretino) y los nuevos fármacos biológicos (etanercept, adalimumab, infliximab, ustekinumab, secukinumab, ixekizumab). Además, disponemos de la fototerapia como otra forma de terapia física para formas moderadas y algunas severas de psoriasis y las nuevas pequeñas moléculas como apremilast y tofacitinib[2].
Probablemente metotrexato (mtx) sea el fármaco que más se ha utilizado y desde hace más años en el tratamiento de la psoriasis moderada severa. Las primeras referencias a su uso en psoriasis se remontan al año 1958[3].

Doctor Jose Luis López Estebaranz
Fuente: Dr. López Estebaranz
El metotrexato (mtx) (C20H22N8O5) es un antimetabolito análogo del ácido fólico derivado por metilación de la ametopterina. Es un inhibidor competitivo de la enzima dihidrofólico-reductasa que cataliza la reducción del ácido dihidrofólico en tetrahidrofólico. Tiene efectos antiproliferativos, antiinflamatorios e inmunosupresores. La Food and Drug Administration aprobó en 1972 la indicación de metotrexato para el tratamiento de la psoriasis en placas. Está indicado también para el tratamiento de la artritis psoriásica y para otras formas de psoriasis, como la psoriasis pustulosa y psoriasis palmo-plantares y eritrodérmicas. En 2010 el grupo de psoriasis de la AEDV publicó una guía de manejo de metotrexato en psoriasis[4].
Dosificación y vía de administración
Metotrexato está disponible para administración oral en comprimidos de 2.5 mg y para administración subcutánea o intramuscular en jeringuillas precargadas y en pluma precargada (autoinyector) en diferentes presentaciones que cubren un rango de dosis entre los 7.5 mg y los 30 mg. Las dosis administradas en psoriasis moderada severa son dosis bajas semanales que van desde 7.5 mg a 25-30 mg. Se administra en una sola toma o tres tomas en dos días la forma oral para disminuir los efectos adversos gastrointestinales. La forma subcutánea se ha observado que presenta menos efectos adversos gastrointestinales y evita errores en la pauta de administración[5]. Se suelen administrar concomitantemente a las 24-48 horas con ácido fólico para disminuir los efectos adversos gastrointestinales y la hepatotoxicidad[6].
Eficacia en psoriasis
Los datos de eficacia de metotrexato en psoriasis provienen en su mayoría de su amplio uso clínico y de estudios retrospectivos. Son escasos los estudios prospectivos que lo comparan con otros fármacos como ciclosporina, adalimumab y briakinumab.
Los datos que tenemos sobre eficacia en cuanto a PASI 75 son menores que con los fármacos biológicos y con ciclosporina.
En un reciente metaanálisis publicado se observan reducciones del PASI 75 en la semana 12-16 de en torno al 45% (rango de 9-92%) con las formas orales y con dosis de inicio de 7.5 mg semanal llegando a dosis de 15-20 mg[7]. No obstante, existe gran heterogenicidad en los estudios analizados en este metaanálisis en cuanto a diseño de los mismos, etnicidad de las cohortes, esquema de incremento de dosis de mtx y factores metabólicos asociados. Pautas de incremento de dosis más rápidos en la práctica clínica darían tasas superiores de respuesta. En un estudio comparativo con briakizumab en psoriasis moderada severa, mtx mostró una reducción del PASI 75 a la semana 8 del 20%, a la semana 24 del 39.9% y a la semana 52 del 23.9%. La dosis empleada de mtx fue de 5-20 mg/semanal[8].
Recientemente se ha observado que los niveles basales de calcio previos al inicio del tratamiento con mtx constituyen un factor predictivo de la respuesta terapéutica[9].
En cuanto a la vía de administración del mtx, en pacientes con artritis reumatoides se ha visto que la vía subcutánea podría ser superior en eficacia a la vía oral[10].
No existen estudios comparativos en psoriasis. Sin embargo, un reciente estudio europeo con mtx vía subcutánea versus placebo en psoriasis moderada severa (PASI >10) consigue tasas de eficacia similares a las publicadas con mtx oral en la semana 16. En este estudio, durante las primeras 16 semanas los pacientes recibieron placebo (n = 29) o mtx subcutáneo (n = 91) a dosis de 17,5 mg/semana, aumentando a 22,5 mg/semana según respuesta clínica a la semana 8. Posteriormente, todos los pacientes recibieron mtx subcutáneo hasta la semana 52. A la semana 16, el 41% del grupo con mtx subcutáneo y el 10% del grupo placebo consiguieron un PASI 75. A la semana 52, el 45% (n=41) de los pacientes alcanzó un PASI 75, y el 28% un PASI 90[11].
Estos datos a la semana 52 sí son superiores a los conseguidos en otros estudios con dosis orales (23%). Además, se consiguen respuestas más rápidas que con el fármaco oral; a la semana 8 consigue PASI 75 del 27% frente al 20% conseguido en otro estudio con mtx oral.
Las dosis de escalado rápido, como muestra este estudio y como ha sido previamente sugerido por otros autores, consigue tasas de eficacia mayores[12].
Aunque metotrexato no alcanza las tasas de eficacia de los biológicos en psoriasis, su menor coste y su amplia experiencia en la vida real hacen que siga siendo un fármaco de primera línea y con una relación coste/eficacia muy favorable.
Autor/a: John Campbell
Fuente: Flickr / Public Domain
La vía de administración subcutánea tiene las ventajas de disminuir los errores accidentales de dosificación, además de mostrar menos efectos secundarios y mayores tasas de eficacia a medio plazo. No obstante, carecemos de estudios comparativos de ambas formas de presentación que confirmen estos datos en psoriasis.
Seguridad
Los efectos adversos de mtx son diversos y de frecuencia variable.
De nuevo los datos que disponemos de la evidencia científica publicada son escasos y muchos provienen de series retrospectivas y práctica clínica habitual.
En un reciente metaanálisis se describen los efectos adversos de mtx en los diferentes ensayos clínicos en psoriasis y también en otras patologías en las que se utiliza la misma dosis que en psoriasis (espondilitis, artritis reumatoide, Crohn, artropatía psoriásica)[7].
Esto permite tener una visión más global de los mismos. No obstante, estos estudios tienen la limitación de la duración de los mismos, no superior al año y ser estudios con escasa “n” de pacientes.
En la tabla 1 se describen los efectos adversos más frecuentes de mtx. Los efectos adversos limitantes más frecuentes en los ensayos clínicos son las náuseas, alteraciones en la función hepática, cefalea, leucopenia y diarrea. Estos efectos adversos son los mismos que se suelen ver en la práctica clínica diaria. En general, en los ensayos clínicos publicados más del 90% de los pacientes no sufre efectos adversos limitantes que obliguen a la suspensión del tratamiento durante 6 meses de tratamiento. En el estudio clínico de Warren con mtx subcutáneo el tratamiento fue bien tolerado, sin ninguna muerte, infección grave o evento cardiovascular graves. Sólo en el 3% tuvieron intolerancia digestiva que obligó a suspender el tratamiento a lo largo de las 52 semanas del estudio.
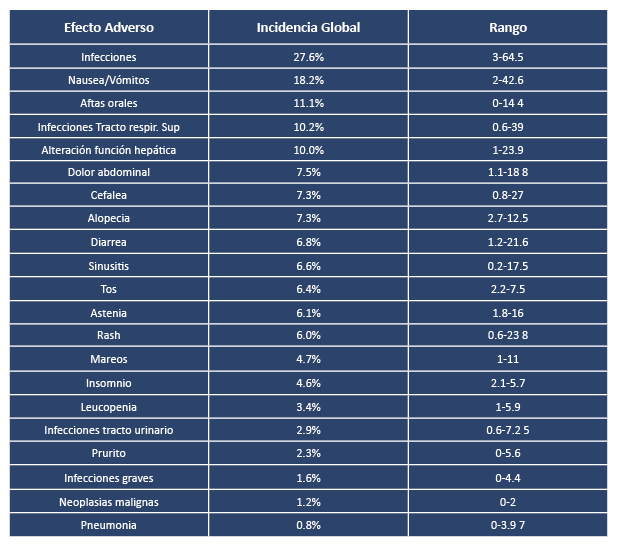
Tabla 1: Efectos adversos descritos por mtx en ensayos clínicos en psoriasis
y otras enfermedades utilizando dosis de psoriasis (modificado de West J, et al[7])
En un estudio publicado por Kim en práctica clínica habitual en 42 pacientes con psoriasis y tratamiento con mtx, encontró anomalías de laboratorio en el 26.2% de los pacientes con un seguimiento medio de 9.5 meses. El efecto adverso más frecuente fue la elevación de enzimas hepáticas leve moderada en el 23.8%[13]. Elegir a los candidatos ideales minimiza los posibles efectos adversos del mtx.
En cuanto a la supervivencia de mtx en psoriasis, Otero y col en un registro prospectivo con 85 pacientes obtienen una supervivencia media con metotrexato de 1.8 años. Existe un 65% de discontinuaciones del fármaco de las que el 35% son debidas a efectos adversos, 26% a ineficacia y 13% a ambas causas. Los efectos adversos más frecuente fueron las molestias gastrointestinales, a pesar de utilizar ac fólico como coadyuvante. Metotrexato se administró en la mayoría de los pacientes por vía oral (84%). En este estudio la supervivencia media a 5 años de mtx fue del 15%. En un subanálisis se observó mayor supervivencia en los pacientes que recibieron mtx vía subcutánea frente a la vía oral, si bien este grupo fue muy reducido[14].
Perspectivas futuras
La aparición de nuevas formas de administración como los sistemas de liberación del fármaco con coloides, las formas en liposomas, nanosomas, ionosomas y nanopartículas van a permitir en el futuro una administración del fármaco más selectiva y dirigida aumentando su eficacia y disminuyendo sus efectos adversos al poder aplicarse tópica o localmente. Existen ya estudios experimentales que avalan su viabilidad[15].
Conclusiones
• Metotrexato es un fármaco que ha mostrado a lo largo de los años ser seguro y eficaz en el tratamiento de la psoriasis moderada-severa.
• Deben descartarse contraindicaciones en su prescripción y elegir al candidato ideal para minimizar los efectos adversos.
• Las formas de administración subcutánea presentan menos efectos adversos y son algo más eficaces en el medio plazo.
• La eficiencia de metotrexato (gracias a un coste bajo) en el manejo de la psoriasis hacen de él un fármaco de primera línea que manejado de forma adecuada presenta un perfil terapéutico muy atractivo.
• En el futuro nuevas formas de presentación tópicas probablemente expandan su uso terapéutico.
Bibliografía
1. Ferrandiz C, Carrascosa JM, Toro M. Prevalencia de la psoriasis en la era de los agentes biológicos. Actas Dermosifiliograf. 2014; 105: 504-9
2. Nast A, Gisondi P, Ormerod AD et al. European S3-Guidelines on the systemic treatment of psoriasis vulgaris – update 2015 – short version – EDF in cooperation with EADV and IPC. J Eur Acad Derma- tol Venereol 2015; 29:2277–94.
3. Edmunson WF, Guy WB. Treatment of psoriasis with folic acid antagonists. AMA Arch Derm. 1958;78:200–3.
4. Carretero G, Puig L, Dehesa L, et al.Guidelines on the use of methotrexate in psoriasis. Actas Dermosifiliogr. 2010 Sep;101(7):600-13
5. Bianchi G, Caporali R, Todoerti M et al. Methotrexate and rheuma- toid arthritis: current evidence regarding subcutaneous versus oral routes of administration. Adv Ther 2016; 33:369–78.
6. Menting SP, Dekker PM, Limpens J et al. Methotrexate dosing regimen for plaque-type psoriasis: a systematic review of the use of test- dose, start-dose, dosing scheme, dose adjustments, maximum dose and folic acid supplementation. Acta Derm Venereol 2016; 96:23–8.
7. West J, Ogston S, Foerster J. Safety and efficacy of methotrexate in psoriasis: A meta-analysis of published trials. PLoS One. 2016;11:e0153740.
8. Reich K, Langley RG, Papp KA, Ortonne JP, Unnebrink K, Kaul M, et al. A 52-week trial comparing briakinumab with methotrexate in patients with psoriasis. N Engl J Med. 2011;365: 1586-96.
9. Zhai Z, Chen L, Yang H, Yan J, Wang C, Yang J, et al. Can pretreatment serum calcium level predict the efficacy of methotrexate in the treatment of severe plaque psoriasis? Journal of the American Academy of Dermatology. 2015;73(6):991–7.e3. pmid:26416303
10. Braun J, Kästner P, Flaxenberg P, Währisch J, Hanke P, Demary W, et al., MC-MTX.6/RH Study Group. Comparison of the clinical efficacy and safety of subcutaneous versus oral admi- nistration of methotrexate in patients with active rheumatoid arthritis results of a six-month, multicenter, randomized, double- blind, controlled, phase IV trial. Arthritis Rheum. 2008;58: 73-81.
11. Warren RB, Mrowietz U, von Kiedrowski R, Niesmann J, Wilsmann- Theis D, Ghoreschi K, et al. An intensified dosing schedule of subcutaneous methotrexate in patients with moderate to severe plaque-type psoriasis (METOP) a 52 week, multicentre, rando- mised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2017;389:528-37.
12. Carrascosa JM, de la Cueva P, Ara M, Puig L, Bordas X, Carretero G, et al. Metotrexato en psoriasis moderada-grave revisión de la literatura y recomendaciones de experto. Actas Dermosifiliogr. 2016;107:194-206.
13. Kim BR, Ohm J, Choi CW, Youn SW. Methotrexate in a Real-World Psoriasis Treatment: Is It Really a Dangerous Medication for All? Ann Dermatol 2017;29:346-8.
14. Otero ME, Van der Reek JM, Seeger MM, et al. Determinants for drug survival of methotrexate in patients with psoriasis, split according to different reasons for
discontinuation: results of the prospective MTX-CAPTURE . Br J Dermatol 2017;
15. Ferreiras M , Barreiros L, Segundo MA, et al. Topical co-delivery of methotrexate and etanercept using lipid nanoparticles: A targeted approach for psoriasis management. Colloids Surf B Biointerfaces. 2017 Jul 29;159:23-29
Para acceder a la ficha técnica, clicar aquí






