Dr. Fernando Civeira
PCSK9 son las iniciales de Proprotein Convertase Subtilisin/Kexin tipo 9.
PCSK9 es una enzima de 692 aminoácidos miembro de una familia de serin-proteasas que activan una gran variedad de proteínas involucradas en la regulación de varias vías metabólicas. PCSK9 tiene actividad autocatalítica, y una vez en su forma activa se une al receptor de las lipoproteínas de baja densidad (rLDL) acompañándolo hasta su degradación en los lisosomas, y por tanto, impidiendo el reciclado del rLDL a la superficie del hepatocito y reduciendo la captación hepática de colesterol LDL plasmático (1,2).
El descubrimiento de PCSK9 se realizó en el curso de la investigación de la causa de hipercolesterolemia en un grupo de familias en quienes se había excluido mutaciones en los genes responsables conocidos hasta entonces: el gen del rLDL (LDLR), y el gen de la apolipoproteina B (APOB) (3). Pronto se identificó que existían mutaciones en PCSK9 con ganancia de función que causaban hipercolesterolemia familiar, y también mutaciones en PCSK9 con pérdida de función que se acompañaban de reducciones variables de colesterol LDL pero de una protección muy considerable en la enfermedad cardiovascular (2,4). Estos estudios pusieron de relieve el papel fundamental de PCSK9 en la regulación de la concentración de colesterol LDL en sangre, y del enorme potencial terapéutico de una reducción de la actividad ligada a PCSK9 en la prevención de las enfermedades cardiovasculares.

Doctor Fernando Civeira
Fuente: Archivo
La hipótesis inicial se confirmó en modelos animales, y los ratones “knockout” para PCSK9 mostraron una disminución importante en el desarrollo de la arteriosclerosis. Simultáneamente se describieron en la literatura varios sujetos adultos homocigotos para mutaciones con pérdida de función en PCSK9 con concentraciones de colesterol muy bajas (<25 mg/dL), ausencia de enfermedad cardiovascular, y con un desarrollo físico y psíquico normales. Estos sujetos reafirmaron el papel de PCSK9 en el metabolismo lipídico, y la viabilidad sin riesgos aparentes para la salud de una reducción muy importante de PCSK9 a lo largo de la vida (2,5).
Esto llevó a la exploración de varios métodos para reducir PCSK9 o inhibir su función incluyendo oligonucleótidos antisentido, RNAs de interferencia, péptidos miméticos y moléculas pequeñas para inhibir la unión rLDL y PCSK9. Pero han sido los anticuerpos monoclonales anti PCSK9 el procedimiento con más éxito en su desarrollo demostrando una gran potencia reduciendo el colesterol LDL, seguridad clínica con ausencia de efectos secundarios relevantes, y gran comodidad en su administración.
Los primeros estudios en humanos en voluntarios sanos se realizaron con el anticuerpo totalmente humano MoAb REGN727 (actualmente llamado alirocumab) y, poco después con MoAb AMG145 (evolocumab), y RN316 (bococizumab), éste último un anticuerpo humanizado. Estos estudios demostraron reducciones rápidas dosis dependiente de colesterol LDL de hasta el 80%, que aparecían a los pocos días de la administración del anticuerpo, y que perduraban entre 2-6 semanas tras una única administración subcutánea (5,6). Estos estudios iniciales también demostraron la eficacia y seguridad de estos fármacos en sujetos con diferentes formas de hipercolesterolemia, incluidos los sujetos heterocigotos para mutaciones funcionales en el LDLR, es decir afectos de hipercolesterolemia familiar. Así mismo, el efecto hipolipemiante era aditivo al conseguido con la estatinas, incluso a las dosis más potentes de éstas últimas (6).
Alirocumab y evolocumab han sido ampliamente estudiados en múltiples estudios de fase 2, especialmente con dosis de 75 y 150 mg cada 14 días para alirocumab; y de 140 mg cada 14 días y 420 mg cada 28 días para evolocumab. Las poblaciones de estudio han incluido pacientes de alto riesgo cardiovascular fuera de objetivos de colesterol LDL en terapia máxima con estatinas (7); sujetos con diferentes grados de hipercolesterolemia en tratamiento con dieta, estatinas, y/o ezetimiba; sujetos intolerantes a estatinas con concentraciones de colesterol LDL elevadas (8); y sujetos con hipercolesterolemia familiar, tanto homocigotos como heterocigotos (9). Los resultados de todos ellos han sido muy consistentes: reducciones entre el 45-60% en la concentración de colesterol LDL; reducciones del 10-20%, 20-35% y 30-50% en las concentraciones de triglicéridos, lipoproteína(a) y apolipoproteína B respectivamente; y efectos adversos semejantes al comparador que habitualmente fue placebo y en menor medida ezetimiba. Los resultados son muy consistentes sin diferencias entre sexos, edad, peso, uso concomitante de estatinas, concentración basal de colesterol LDL, triglicéridos, lipoproteína (a), o PSCK9 (5); o tipo de mutación responsable de hipercolesterolemia en los casos de hipercolesterolemia familiar heterocigota (10). La eficacia y seguridad se mantuvo en el seguimiento a más de un año (11).

Autor/a: Horia Varlan
Fuente: Flickr / Creative Commons
Las fases 3 de alirocumab y evolocumab han confirmado los datos de eficacia y seguridad de fases previas pero al incluir mayor número de pacientes y mayores periodos de seguimiento, han comenzado a dar resultados sobre enfermedad cardiovascular. En el estudio ODYSSEY LONG TERM, donde se estudió la eficacia y seguridad de alirocumab 150 mg cada 14 días en 2.341 pacientes en dosis máximas toleradas de estatinas fuera de objetivos de colesterol LDL, alirocumab redujo el colesterol LDL un 62% a las 24 semanas en comparación con el placebo, y el 79% alcanzó objetivos de colesterol LDL frente al 8% del grupo placebo. En un análisis post-hoc de eventos cardiovasculares que incluyó los casos de muerte cardiovascular, infarto de miocardio e ictus isquémicos no fatales y angina inestable que requirió hospitalización fue menos frecuente con alirocumab que con placebo con una reducción de 48% tras un seguimiento medio de aproximadamente un año (12). Resultados semejantes se obtuvieron en el seguimiento de los estudios OSLER de fases 1 y 2 que incluyeron a 4.465 pacientes que fueron randomizados a evolocumab más tratamiento habitual, o a tratamiento habitual, y donde hubo una reducción del 53% de eventos (13). En el estudio OSLER el seguimiento no fue doble ciego como en el caso del estudio ODYSSEY LONG TERM, pero la similitud de los resultados de ambos estudios hace ser optimista sobre los tres grandes estudios en marcha: ODYSSEY OUTCOMES con alirocumab, FOURIER con evolocumab, y SPIRE 1 y 2 con bococizumab y que tienen como objetivo principal demostrar el beneficio sobre morbi-mortalidad cardiovascular de estos anticuerpos en sujetos de alto riesgo cardiovascular, y fuera de objetivos lipídicos a pesar de dosis máximas toleradas de tratamiento con estatinas de alta potencia con o sin ezetimiba.
Dada la reducción de colesterol LDL-C observado en los ensayos de fase 2 y 3 hasta la fecha, los resultados preliminares de eficacia sobre eventos cardiovasculares, y la excelente tolerancia, se calcula que los anticuerpos monoclonales anti PCSK9 reducirán la enfermedad cardiovascular por encima del 50% en cortos periodos de tiempo 3-5 años. Dos de estos anticuerpos, alirocumab y evolocumab, ya se encuentran disponibles para su prescripción en Estados Unidos y varios países europeos, y es previsible que en España estén disponibles a lo largo de 2016. Serán candidatos ideales para este grupo farmacológico todos aquellos pacientes de alto o muy alto riesgo cardiovascular a corto plazo y con concentraciones de colesterol LDL bien por encima de los 70 mg/dL a pesar de tratamiento máximo tolerado con los fármacos actualmente en el mercado (estatinas de alta potencia y ezetimiba fundamentalmente). Pacientes en prevención secundaria, diabéticos con afectación vascular, sujetos con hipercolesterolemia familiar serán los probables candidatos a recibir estos fármacos que sin duda ayudarán a reducir drásticamente la enfermedad cardiovascular en nuestro medio.
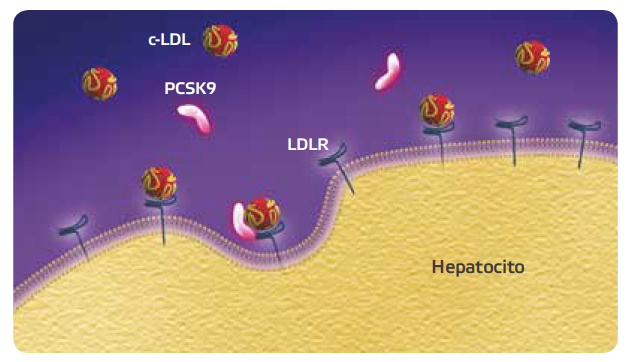
Las mutaciones con “pérdida de función” se asocian a niveles más bajos de c-LDL (14)
Bibliografía
1. Seidah NG, Benjannet S, Wickham L, et al. The secretory proprotein convertase neural apoptosisregulated convertase 1 (NARC-1): liver regeneration and neuronal differentiation. Proc Natl Acad Sci U S A 2003;100:928–33.
2. Abifadel M, Elbitar S, El Khoury P, et al. Living the PCSK9 adventure: from the identification of a new gene in familial hypercholesterolemia towards a potential new class of anticholesterol drugs. Curr Atheroscler Rep 2014;16:439.
3. Varret M, Rabes JP, Saint-Jore B, et al. A third major locus for autosomal dominant hypercholesterolemia maps to 1p34.1-p32. Am J Hum Genet 1999;64:1378–87.
4. Cohen JC, Boerwinkle E, Mosley TH Jr., et al. Sequence variations in PCSK9, low LDL, and protection against coronary heart disease. N Engl J Med 2006;354:1264–72.
5. Giugliano RP, Sabatine MS. Are PCSK9 Inhibitors the Next Breakthrough in the Cardiovascular Field? J Am Coll Cardiol 2015;65:2638-51.
6. Stein EA, Mellis S, Yancopoulos GD, Stahl N, Logan D, Smith WB, et al. Effect of a monoclonal antibody to PCSK9 on LDL cholesterol. N Engl J Med 2012;366:1108–18.
7. Koren MJ, Scott R, KimJB, Knusel B, Liu T, Lei L, et al. Efficacy, safety, and tolerability of a monoclonal antibody to proprotein convertase subtilisin/kexin type 9 as monotherapy in patients with hypercholesterolaemia (MENDEL): a randomised, double-blind, placebo-controlled, phase 2 study. Lancet. 2012;380:1995–2006.
8. Stroes E, Colquhoun D, Sullivan D, Civeira F, Rosenson RS, Watts GF, et al. Anti-PCSK9 antibody effectively lowers cholesterol in patients with statin intolerance: the GAUSS-2 randomized, placebo-controlled phase 3 clinical trial of evolocumab. J Am Coll Cardiol 2014;63:2541–8.
9. Kastelein JJ, Ginsberg HN, Langslet G, Hovingh GK, Ceska R, Dufour R, Blom D, Civeira F, et al. ODYSSEY FH I and FH II: 78 week results with alirocumab treatment in 735 patients with heterozygous familial hypercholesterolaemia. Eur Heart J. 2015;36:2996-3003.
10. Raal FJ, Stein EA, Dufour R, Turner T, Civeira F, Burgess L, et al., RUTHERFORD-2 Investigators. PCSK9 inhibition with evolocumab (AMG 145) in heterozygous familial hypercholesterolaemia (RUTHERFORD-2): a randomised, double-blind, placebo-controlled trial. Lancet 2015;385:331–40.
11. Koren MJ, Giugliano RP, Raal FJ, Sullivan D, Bolognese M, Langslet G, Civeira F, et al. Efficacy and safety of longer-term administration of evolocumab (AMG 145) in patients with hypercholesterolemia: 52-week results from the Open-Label Study of Long-Term Evaluation Against LDL-C (OSLER) randomized trial. Circulation. 2014 Jan 14;129(2):234-43.
12. Robinson JG, Farnier M, Krempf M, et al., for the ODYSSEY LONG TERM Investigators. Efficacy and safety of alirocumab in reducing lipids and cardiovascular events. N Engl J Med 2015;372:1489–99.
13. Sabatine MS, Giugliano RP, Wiviott SD, et al., for the Open-Label Study of Long-Term Evaluation against LDL Cholesterol (OSLER) Investigators. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med 2015;372:1500–9.
14. Benn M, Nordestgaard BG, Grande P, Schnohr P, Tybjaerg-Hansen A. PCSK9 R46L, low-density lipoprotein cholesterol levels, and risk of ischemic heart disease: 3 independent studies and meta-analyses. J Am Coll Cardiol. 2010;55:2833-2842.




