Redacción Farmacosalud.com
Cualquier novedad terapéutica siempre es bienvenida, en especial cuando puede solucionar un fracaso previo. En este sentido, la doctora Mónica Marazuela Azpíroz, jefa del Servicio de Endocrinología y Nutrición del Hospital Universitario de La Princesa (Madrid) y profesora titular de Endocrinología de la Universidad Autónoma de Madrid, destaca la reciente aprobación de un nuevo análogo de somatostatina, el pasireotide, que “puede ser de utilidad para algunos pacientes” de acromegalia “que no responden a los análogos de somatostatina previos”.

Doctora Mónica Marazuela
Fuente: Hospital Universitario de La Princesa
Se estima que, a nivel mundial, la acromegalia afecta a unas 60 personas por millón, presentando una incidencia anual de 3 a 4 nuevos casos por millón[1]. La acromegalia es, pues, una enfermedad rara. Y además es crónica, causada por una secreción excesiva de la hormona del crecimiento (GH). A veces, esta dolencia puede afectar a varios miembros de una misma familia debido a cambios genéticos, o mutaciones, en su ADN[2]. Algunas de estas mutaciones han sido identificadas: por ejemplo, el gen AIP en pacientes con familiares acromegálicos, o el gen menin en pacientes con neoplasia endocrina múltiple tipo 1 (MEN1)[2]. “Se pueden identificar algunas de estas mutaciones asociadas a acromegalia mediante análisis genético. Se sabe que si una persona es portadora de una determinada mutación tiene un riesgo aumentado de desarrollar esta enfermedad, pero esto no significa que vaya a desarrollar la enfermedad siempre en todos los casos. En el caso del gen de la menina, los portadores tienen un riesgo de aproximadamente un 30-40% de desarrollar tumores hipofisarios y de un 5% de desarrollar acromegalia. En el caso de mutación del gen AIP, los portadores tienen un riesgo de un 20% de desarrollar adenomas hipofisarios”, explica la facultativa.
Atención a la necesidad de aumentar el tamaño del anillo colocado en el dedo
La secreción excesiva de hormona de crecimiento (GH) se produce mayoritariamente por el desarrollo de un tumor de la hipófisis o glándula pituitaria, que casi siempre es de estirpe benigna. De acuerdo con Marazuela, “el origen de estos tumores no se conoce bien, aunque se cree que se origina por una mutación de una única célula hipofisaria que deja de responder a estímulos normales que le impiden seguir creciendo. Además de GH, estos tumores pueden sintetizar también otras hormonas hipofisarias, y conllevar distintos síndromes”.
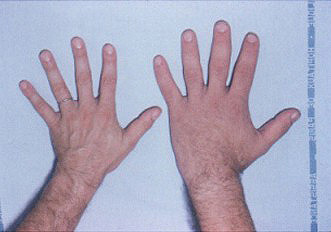
Mano de una persona no afectada (izquierda), y mano de un paciente con acromegalia (a la derecha)
Autor/a de la imagen: Philippe Chanson and Sylvie Salenave
-Acromegaly. Orphanet Journal of Rare Diseases 2008, 3:17. doi:10.1186/1750-1172-3-17
Fuente: Wikimedia Commons
La acromegalia provoca desfiguración progresiva, con tendencia al desarrollo excesivo de la mandíbula, frente ensanchada, y crecimiento desproporcionado de manos o pies. Habitualmente, algunos síntomas se confunden con el proceso de envejecimiento natural, de manera que la patología está infradiagnosticada. Entre los signos que deben alarmar al posible paciente y por ello acudir a un endocrinólogo, figuran: El característico crecimiento de las manos (necesidad de aumentar el tamaño del anillo) y de los pies (aumento de talla del zapato), así como el crecimiento de algunas partes de la cara, como nariz, orejas, labios, frente o mandíbula. Otros cambios que también se pueden asociar son, entre otros, el aumento de la sudoración, cambios de la voz (más ronca), incremento de los ronquidos nocturnos o síndrome de apnea del sueño, artrosis, bocio, diabetes…
Así pues, la acromegalia no solamente tiene repercusiones estéticas, sino que también puede puede provocar afección de los tejidos blandos y tener consecuencias cardiovasculares y metabólicas. ¿Entonces, cómo se puede detectar que una hipertensión arterial, colesterol alto o diabetes -patologías que pueden surgir en esos pacientes- están asociadas a la acromegalia y no son entidades aisladas? La experta contesta lo siguiente: “La hipertensión arterial y la diabetes son patologías muy prevalentes que pueden deberse a múltiples causas, mientras que la acromegalia es una enfermedad rara. En general, sospecharemos que pueden estar asociadas si ocurren en el contexto de un cambio evidente en el morfotipo, u otros datos que nos hagan sospechar la posible existencia de una acromegalia. En estos casos, será conveniente realizar las pruebas de cribado correspondientes para el despistaje de esta enfermedad”.
Acromegálicos no controlados: riesgo de muerte aumentado en un 70%
Identificar la acromegalia es muy importante, dado que esta patología puede llegar a ser mortal. “Los pacientes acromegálicos no controlados tienen un riesgo de muerte aumentado en un 70% aproximadamente, que se reduce a un 30% en pacientes bien controlados. Las causas de muerte se relacionan sobre todo con enfermedad cardiovascular, cerebrovascular, respiratoria y en relación al cáncer de colon”, concreta la doctora Marazuela. La mortalidad en los pacientes con acromegalia supera en tres veces la observada en la población normal, lo que conlleva una reducción del promedio de la esperanza de vida de estas personas en aproximadamente 10 años[3,4]. Sin embargo, los datos epidemiológicos disponibles indican que el buen control de la enfermedad aproxima la tasa de mortalidad de los pacientes acromegálicos a la de la población general[5,6]. En esta línea, la Dra. Rosa Cámara Gómez, jefa de Sección de Endocrinología y Nutrición del Hospital Universitario y Politécnico La Fe de Valencia, hace hincapié en que “uno de los principales objetivos del tratamiento de la acromegalia es disminuir la elevada tasa de mortalidad que arroja, manteniendo al paciente asintomático”.
![Rostro típicamente acromegálico, según el repositorio ‘Acromegalia’ de Wikimedia Commons<br />[Identifier: physicaldiagnosi1905cabo (find matches) Title: Physical diagnosis Year: 1905 (1900s) Authors: Cabot, Richard C. (Richard Clarke), 1868-1939 Subjects: Diagnosis Chest Diagnosis Publisher: New York : William Wood and Company Contributing Library: Francis A. Countway Library of Medicine Digitizing Sponsor: Open Knowledge Commons and Harvard Medical School] Rostro típicamente acromegálico, según el respositorio ‘Acromegalia’ de Wikimedia Commons Identifier: physicaldiagnosi1905cabo (find matches) Title: Physical diagnosis Year: 1905 (1900s) Authors: Cabot, Richard C. (Richard Clarke), 1868-1939 Subjects: Diagnosis Chest Diagnosis Publisher: New York : William Wood and Company Contributing Library: Francis A. Countway Library of Medicine Digitizing Sponsor: Open Knowledge Commons and Harvard Medical School Fuente: Internet Archive Book Images https://www.flickr.com/photos/internetarchivebookimages/14576529919/ Source book page: https://archive.org/stream/physicaldiagnosi1905cabo/physicaldiagnosi1905cabo#page/n42/mode/1up Wikimedia Commons](http://farmacosalud.com/wp-content/uploads/2016/11/2222-acromegalia.jpg)
Rostro típicamente acromegálico, según el repositorio ‘Acromegalia’ de Wikimedia Commons
[Identifier: physicaldiagnosi1905cabo (find matches) Title: Physical diagnosis Year: 1905 (1900s) Authors: Cabot, Richard C. (Richard Clarke), 1868-1939 Subjects: Diagnosis Chest Diagnosis Publisher: New York : William Wood and Company Contributing Library: Francis A. Countway Library of Medicine Digitizing Sponsor: Open Knowledge Commons and Harvard Medical School]
Fuente: Internet Archive Book Images
https://www.flickr.com/photos/internetarchivebookimages/14576529919/ Source book page:
https://archive.org/stream/physicaldiagnosi1905cabo/physicaldiagnosi1905cabo#page/n42/mode/1up
Wikimedia Commons
Como se ha apuntado anteriormente, por norma general el exceso de la hormona del crecimiento se relaciona con el desarrollo de un tumor benigno de la pituitaria. Los enfermos que son candidatos a someterse a una cirugía para extirpar el tumor son, en general, cualquier paciente que no presente una contraindicación quirúrgica clara. Eso es relevante porque la cirugía “permite la posibilidad de curación completa de la enfermedad, o al menos quitar parte del tumor, y facilitar la respuesta a otros tratamientos posteriores”, afirma Marazuela.
Opciones farmacológicas
A modo de tratamiento farmacológico, están a) los análogos de la somatostatina b) agonistas dopaminérgicos y c) el antagonista del receptor de GH, pegvisomant.
Según la jefa del Servicio de Endocrinología y Nutrición del Hospital Universitario de La Princesa (Madrid), “cuando el tumor no se ha curado con la cirugía es necesario normalizar los niveles de GH o IGF-I mediante otros tratamientos. En general, se utilizan como de primera elección los análogos de somatostatina, que son capaces de controlar la secreción aumentada de GH en aproximadamente un 50% de pacientes. Si la elevación de la GH es muy leve se puede intentar tratamiento con cabergolina que, aunque no es tan eficaz como los análogos de somatostatina, es un fármaco que se administra vía oral y se tolera aceptablemente. En algunos casos se puede utilizar un tratamiento combinado de cabergolina con análogos de somatostatina. Si hay ausencia de respuesta a estos tratamientos se puede utilizar como segunda elección el tratamiento con pegvisomant. Éste es un tratamiento muy eficaz que consigue controlar prácticamente al 90% de los pacientes, aunque, debido a su administración subcutánea diaria y su coste, se reserva para pacientes no controlados con otros tratamientos”.
Marazuela comenta que recientemente se ha aprobado “un nuevo análogo de somatostatina, el pasireotide, que tiene una afinidad por los distintos receptores de somatostatina diferente de la de los análogos de somatostatina clásicos previos. Se ha reportado que el pasireotide puede ser de utilidad para algunos pacientes que no responden a los análogos de somatostatina previos”.
Sin ir más lejos, en el marco del 58º Congreso de la Sociedad Española de Endocrinología y Nutrición (SEEN), Novartis Oncology ha presentado Signifor® (pasireotida [o pasireotide]), indicado para el tratamiento de adultos acromegálicos en los que la cirugía no es una opción o no ha sido curativa y que no están adecuadamente controlados con otro análogo de la somatostatina (ASS)[7]. La aprobación de la nueva terapia se ha basado en los datos de dos estudios multicéntricos de Fase III, C2402 y C2305 respectivamente, en los que se ha demostrado que Signifor® presenta una eficacia superior en el control bioquímico medido por los niveles de la hormona de crecimiento (GH) y del factor de crecimiento insulínico tipo 1 (IGF-1), en comparación con un ASS de primera generación[7]. En el marco del encuentro de la SEEN se ha celebrado el Simposio Satélite ‘Avance para conseguir el control de la acromegalia’, reunión en la que, precisamente, han participado las doctoras Marazuela y Cámara.

Vista del Palacio de Congresos de Málaga, sede del Congreso SEEN 2016
Autor/a de la imagen: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
La radioterapia, aunque sigue siendo útil, ha sido relegada a un 2º o 3er plano
Por su parte, la SEEN trabaja activamente por el control y correcto abordaje de la acromegalia mediante diversos proyectos de investigación que desarrolla en el campo de la endocrinología, la nutrición y el metabolismo. En relación a todo ello, el Dr. Manuel Puig Domingo, presidente de esta sociedad médica, indica que “desde la SEEN se trata de mejorar la comunicación con los pacientes para que dispongan de información adecuada sobre la enfermedad. Además, la SEEN busca concienciar a la sociedad civil y a los profesionales médicos no endocrinos de la existencia de la patología y de la necesidad de alcanzar un diagnóstico precoz”. Puig, asimismo, señala la importancia de “la promoción de la medicina personalizada en el tratamiento de la acromegalia a través de proyectos como REMAH (Registro Español Molecular de Adenomas Hipofisarios) u otros pertenecientes al grupo de trabajo de Neuroendocrinología”.
Otra de las opciones de tratamiento para la acromegalia es la radioterapia, un procedimiento que ha ido perdiendo fuelle en este ámbito porque, a pesar de que había llegado a posicionarse como “un pilar fundamental en el tratamiento” de dicha patología, “las mejoras actuales en las técnicas quirúrgicas y en la farmacología disponible la han relegado a un segundo o tercer plano”, asevera Marazuela. No obstante, la radioterapia “sigue siendo una técnica útil, fundamentalmente en los casos con importante tumor residual tras la cirugía”, puntualiza.
Cabe destacar que, una vez que la acromegalia ha sido controlada, el proceso de desfiguración del paciente se detiene. Las partes blandas que hubieran aumentado de tamaño, como la piel o la grasa subcutánea, pueden volver a la normalidad, y los pacientes notan que se ‘deshinchan’. “No obstante, las alteraciones óseas no suelen regresar y por ello es posible que ciertas deformidades persistan a pesar de la curación bioquímica”, advierte Marazuela.
Referencias
1. Acromegaly. National Institutes of Health. National Institute of Diabetes and Digestive and Kidney Diseases. 2008 May; 8(3924): 1-10.
2. Shlomo Melmed, Stephan Petersenn. ACROMEGALIA. RESPUESTAS A SUS PREGUNTAS. The Pituitary Society. Difusión online https://pituitarysociety.org/sites/all/pdfs/Pituitary_Society_Acromegaly_brochure_Spanish.pdf
3. Jallad RS, Bronstein MD. The place of medical treatment of acromegaly: current status and perspectives. Expert Opin Pharmacother. junio de 2013;14(8):1001-15.
4. Melmed S, Kleinberg DL, Bonert V, Fleseriu M. Acromegaly: assessing the disorder and navigating therapeutic options for treatment. Endocr Pract. octubre de 2014;20 Suppl 1:7-17; quiz 18-20.
5. Ben-Shlomo A, Sheppard MC, Stephens JM, Pulgar S, Melmed S. Clinical, quality of life, and economic value of acromegaly disease control. Pituitary. septiembre de 2011;14(3):284-94.
6. Colao A, Baldelli R, Marzullo P, Ferretti E, Ferone D, Gargiulo P, et al. Systemic hypertension and impaired glucose tolerance are independently correlated to the severity of the acromegalic cardiomyopathy. J Clin Endocrinol Metab. enero de 2000;85(1):193-9.
7. Signifor® (pasireotida) Ficha Técnica del Producto. Basilea, Suiza: Novartis Pharma AG; Septiembre de 2014.




