Redacción Farmacosalud.com
La prestigiosa revista ‘Cell Stem Cell’ ha publicado los resultados de una investigación preclínica que ha conseguido corregir el defecto genético en las células madre sanguíneas de pacientes con anemia de Fanconi mediante una novedosa manera de editar el genoma. Este trabajo demuestra por primera vez que la generación controlada de mutaciones con la tecnología CRISPR/Cas9 puede corregir de manera eficaz las mutaciones originales responsables de esta enfermedad. Además, las células editadas muestran un mayor crecimiento que las células enfermas, lo que permite la progresiva sustitución de estas últimas.
La investigación, que se propone como una estrategia de tratamiento tanto para la anemia de Fanconi como para otras enfermedades que afectan a las células madre de la sangre por su simplicidad y gran eficacia, ha sido realizada por investigadores del Centro de Investigaciones Energéticas, Medioambientales y Tecnológicas (CIEMAT), el Centro de Investigación Biomédica en Red de Enfermedades Raras (CIBERER) y el Instituto de Investigación Sanitaria de la Fundación Jiménez Díaz (IIS-FJD) dirigidos por Paula Río, de la División de Terapias Innovadoras que coordina Juan Bueren. El primer firmante del trabajo es Francisco José Román-Rodríguez.
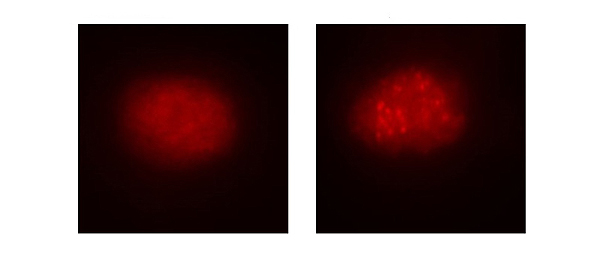
(A la izq.), célula de la sangre de un paciente con anemia de Fanconi antes de la corrección mediante el uso del sistema CRISPR/Cas9. (Dcha.), la célula ya corregida. Se observa cómo se repara la función de la ruta de la anemia de Fanconi
Fuente: CIBERER / Centro de Investigación Biomédica en Red (CIBER) / CIEMAT / IIS-FJD
Una enfermedad rara de origen genético
La anemia de Fanconi es una enfermedad rara de origen genético caracterizada por fallo de la médula ósea y predisposición al cáncer que se manifiesta en la mayor parte de los pacientes por la deficiente producción de células sanguíneas a edades muy tempranas. El trasplante de células madre sanguíneas de un donante sano constituye actualmente la terapia de elección en estos pacientes. Aunque este tipo de trasplante ha mejorado sustancialmente en los últimos años, no todos los afectados tienen un donante adecuado. Además, estos tratamientos no están exentos de reacciones de rechazo y de otro tipo de riesgos a más largo plazo.
Un estudio clínico reciente coordinado por este mismo grupo del CIEMAT/CIBERER/IIS-FJD en colaboración con el Hospital del Niño Jesús de Madrid y la Red Nacional de Anemia de Fanconi. ha demostrado que las células madre sanguíneas de estos pacientes pueden ser corregidas mediante la introducción de una copia de la versión sana del gen afectado. El trabajo va un paso más allá en la corrección de las células madre sanguíneas de pacientes con anemia de Fanconi, ya que ha conseguido en modelos preclínicos corregir directamente el propio gen mutado mediante la modificación dirigida del genoma de estas células (edición génica) utilizando el sistema conocido como CRISPR/Cas9. La tecnología CRISPR/Cas9 permite generar de forma altamente precisa cortes en regiones específicas del ADN. En el caso de las células madre de la sangre, los cortes son reparados principalmente mediante un mecanismo no preciso (reparación NHEJ) que con frecuencia introduce cambios en la secuencia, lo cual generalmente produce efectos indeseables en las células.
Paradójicamente, en este trabajo se demuestra que la generación de nuevas mutaciones dirigidas en células madre de pacientes con anemia de Fanconi constituye un procedimiento extraordinariamente sencillo que puede compensar de manera eficaz las mutaciones iniciales responsables de la enfermedad de estas células. Con ello se restauran las propiedades que caracterizan a una célula madre sana, tal como son su elevada capacidad de división y su capacidad para reparar lesiones producidas por compuestos que dañan el ADN. “La simplicidad y elevada eficacia de esta aproximación de edición génica sugiere que podría utilizarse como estrategia para corregir no solo la anemia de Fanconi, sino también otras enfermedades monogénicas que afectan a las células madre de la sangre”, subrayan Francisco José Román y Paula Río.
Artículo de referencia:
Roman-Rodriguez FJ, et al. NHEJ-mediated repair of CRISPR-Cas9-induced DNA breaks efficiently corrects mutations in HSPCs from patients with Fanconi Anemia. Cell Stem Cell. Sep. 2019. https://doi.org/10.1016/j.stem.2019.08.016 https://www.cell.com/cell-stem-cell/pdfExtended/S1934-5909(19)30351-0




