Redacción Farmacosalud.com
Las células tumorales tienen capacidad de resistencia a los medicamentos y también pericia a la hora de intentar esquivar a los tratamientos. Por ello, sólo el tiempo dirá qué recursos mostrará el cáncer frente a un revolucionario nanofármaco que, por ahora y en modelos animales, frena la aparición de metástasis e incluso induce a su regresión una vez que la diseminación tumoral ya está instaurada. El nuevo nanofármaco, conocido por el momento con el nombre de T22-GFP-FdU, es eficaz en el ámbito del cáncer de colon y ya se han obtenido buenos resultados en otros cuatro tipos de tumores. Sin necesidad de lanzar las campanas al vuelo, está claro que se está ante un hallazgo más que prometedor en el mundo de la oncología médica.

Doctor Ramón Mangues
Fuente: El Centro de Investigación Biomédica en Red (CIBER) / CIBER-BBN / Dr. Mangues
T22-GFP-FdU ha sido creado por investigadores del CIBER-BBN (Centro de Investigación Biomédica en Red en su área de Bioingeniería, Biomateriales y Nanomedicina) en el Instituto de Investigación Biomédica de Sant Pau (IIB Sant Pau, en Barcelona), la Universidad Autónoma de Barcelona (UAB) y el CSIC. El nanofármaco ya ha demostrado que elimina selectivamente las células madre metastásicas en modelos animales de cáncer de colon y los resultados obtenidos ya han sido publicados en una de las revistas científicas internacionales más prestigiosas en el ámbito de la Medicina Molecular, ‘EMBO Molecular Medicine’. Los principales artífices del hallazgo son los doctores Ramón Mangues (IIB Sant Pau), Antonio Villaverde y Esther Vázquez (UAB), todos ellos miembros del CIBER-BBN, y Ramon Eritja (Consejo Superior de Investigaciones Científicas, en Barcelona).
El receptor CXCR4, sobreexpresado en 20 tipos diferentes de cáncer
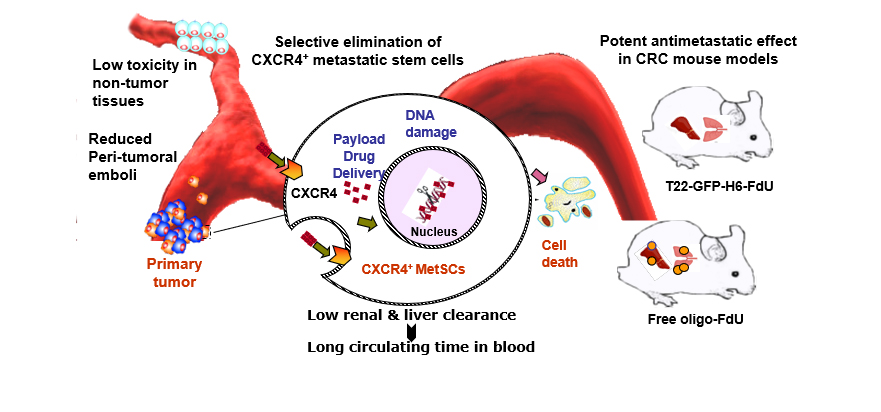
El nanofármaco actúa sobre las células iniciadoras de metástasis a través de su interacción específica entre un péptido presente en la nanopartícula proteica que lo transporta y el receptor celular CXCR4, que se encuentra sobreexpresado en las células tumorales. Esto permite atacar solamente a las células tumorales, bloqueando su diseminación en estadios tempranos, de manera que previene la aparición de metástasis a la vez que evita los efectos adversos derivados de los tratamientos habituales.
En paralelo, T22-GFP-FdU también tiene potencial cuando la metástasis ya está instaurada, es decir, es útil a la hora de frenar el crecimiento o diseminación tumoral ya avanzada e incluso puede llegar a eliminarla, tal y como refiere Mangues, líder del equipo de investigadores: “En la publicación en ‘EMBO Molecular Medicine’ se demuestra que, además de prevenir metástasis, el nanofármaco es capaz de inducir la regresión de metástasis previamente establecidas en modelos animales de cáncer colorrectal”.
El receptor CXCR4 está sobreexpresado en 20 tipos diferentes de cáncer como mínimo, entre ellos los de próstata, mama, ovario y otros no tan comunes como el de páncreas. Así pues, la nanopartícula se puede dirigir para tratar diferentes tipos de neoplasias, convirtiéndola en un vehículo muy versátil que puede transportar diferentes moléculas terapéuticas de elevada potencia. De hecho, la acción antimetástasis de T22-GFP-FdU ya se está evaluando en modelos animales de 4 tipos tumorales adicionales, más allá del cáncer de colon. “Tenemos ya buenos resultados de bloqueo de la diseminación con una estrategia similar que usa esta misma nanopartícula, pero se conjuga a fármacos diferentes al usado en cáncer de colon, para los que se sabe que son activos en cada tipo tumoral evaluado. Esperamos publicar pronto esos resultados”, afirma el doctor Mangues, a su vez investigador titular del Instituto de Investigación del Hospital de Sant Pau y coordinador de Traslación del CIBER-BBN.
“Es imposible anticipar la repercusión del descubrimiento. Tenemos que ser modestos”
T22-GFP-FdU se ha convertido en el primer fármaco del mundo que bloquea la diseminación metastásica (la principal causa de muerte en pacientes oncológicos) dado que actualmente no existen medicamentos en el mercado que eliminen selectivamente las células madre metastásicas. Por lo tanto, el nuevo descubrimiento podría tener un alto impacto clínico después de que se hayan realizado los ensayos necesarios para aplicarse en humanos. El Hospital de Sant Pau de Barcelona sería el primer centro en el mundo en evaluar este fármaco en personas, previamente a su posible introducción en la terapéutica clínica.
Con todo, para Mangues “es imposible anticipar la repercusión del descubrimiento. Tenemos que ser modestos por dos razones. Una es que las células tumorales son inestables genéticamente, por lo que casi siempre son capaces a corto o más largo plazo de desarrollar resistencia a los tratamientos. Por otra parte, las células madre metastáticas tienen plasticidad, lo que quiere decir que cuando son atacadas por fármacos pueden cambiar su fenotipo para intentar esquivar sus efectos. Por tanto, la cuestión no es si vamos a curar todo el cáncer y su diseminación, sino que es: en qué porcentaje de pacientes podremos llegar a inhibir sus metástasis y también cuánto tiempo de supervivencia añadiremos a los pacientes tratados. Sólo el resultado de los ensayos clínicos que se realicen en pacientes, que esperamos que sean en el Hospital de Sant Pau en Barcelona, determinarán a posteriori el impacto de esta nueva aproximación terapéutica”.
Si todo va bien, T22-GFP-FdU podría llegar a la práctica clínica en 5-10 años
En su aplicación en humanos, y en caso de que funcionara en personas afectadas de cáncer de colon, el nuevo nanofármaco podría estar disponible en un plazo de 5-10 años. “Iniciamos ahora los estudios preclínicos regulatorios en la compañía Nanoligent antes de entrar en ensayos clínicos en pacientes. Si los resultados clínicos fueran los que esperamos, entraría en el mercado”, señala.
Fuente: El Centro de Investigación Biomédica en Red (CIBER) / CIBER-BBN / Dr. Mangues
En junio de 2017 los investigadores del CIBER-BBN, el IIB Sant Pau y el Instituto de Biotecnología y Biomedicina de la UAB que firman ahora el artículo de ‘EMBO Molecular Medicine’ pusieron en marcha Nanoligent, una spin-off creada para desarrollar el primer fármaco diseñado para eliminar las células metastásicas. Esta empresa -con más de 10 años de estudios a sus espaldas y dirigida por Manuel Rodríguez Mariscal, profesional con una larga experiencia en el campo de la inversión y la creación de compañías biotecnológicas- tiene como objetivo conseguir la financiación para la realización del proyecto.
T22-GFP-FdU no es una terapia génica porque no interacciona con genes para regular su expresión o inactivarlos. Sin embargo, sí es un fármaco biotecnológico porque se utiliza ingeniería genética para producir en bacterias la nanopartícula proteica que direcciona al fármaco conjugado a células tumorales CXCR4+, formando ambos la nanomedicina.
Artículo de referencia:
Céspedes MV., Unzueta U., Aviñó A., et al. “Selective depletion of metastatic stem cells as therapy for human colorectal cancer”. EMBO Molecular Medicine. DOI 10.15252/emmm.201708772




