Redacción Farmacosalud.com
Los datos preliminares del primer programa nacional de inmunización frente a la meningitis B a nivel mundial con Bexsero®[1], puesto en marcha hace un año en el Reino Unido, muestran que la efectividad estimada de la vacuna es de un 83% frente a cualquier cepa de meningococo B y de un 94% frente a las cepas prevenibles mediante la vacuna, en los lactantes que reciben las primeras dos dosis de las tres dosis recomendadas[2]. Los casos notificados de la enfermedad se redujeron en un 50% en la población objetivo del programa de vacunación en los primeros diez meses del programa si los comparamos con el número medio de casos de los últimos cuatro años. Estos datos fueron presentados por Salud Pública de Reino Unido (PHE por sus siglas en inglés) durante la “International Pathogenic Neisseria Conference (IPNC por sus siglas en inglés)” celebrada en Manchester, Reino Unido.
La aceptabilidad de la vacuna en el programa nacional de inmunización del Reino Unido ha sido elevada. De los más de 600.000 lactantes de 0-1 años de edad que pueden beneficiarse de la vacuna, más del 90% recibió dos dosis, apuntan desde la compañía GSK.
Fuente: Archivo
La meningitis B no es común, pero sí muy peligrosa
La enfermedad meningocócica invasiva por serogrupo B es la principal causa de meningitis que puede poner en peligro la vida de los pacientes en el mundo industrializado. Aunque la enfermedad meningocócica invasiva por serogrupo B no es común, la progresión de la enfermedad es muy rápida entre los niños y adolescentes previamente sanos, con una alta morbilidad y mortalidad. Los síntomas iniciales a menudo pueden parecerse a los de la gripe, haciendo difícil su diagnóstico. Aproximadamente una de cada 10 de las personas que contraen la enfermedad morirá, incluso con el tratamiento adecuado. Además, hasta un 20% de los pacientes que sobreviven a una meningitis bacteriana presentan secuelas físicas o neurológicas importantes (amputaciones, de miembros, pérdida de la audición o convulsiones)[3,4].
Bexsero® es actualmente la única vacuna frente al meningococo B autorizada en Europa. El programa nacional de inmunización del Reino Unido es el primer programa puesto en marcha en el mundo para la prevención de la meningitis B. Los lactantes son vacunados a los dos y a los cuatro meses de edad, más una dosis de refuerzo a los 12 meses, fuera del esquema de vacunación aprobado* pero en línea con las recomendaciones emitidas por el Comité asesor del Reino Unido sobre inmunización[2]. Los datos presentados demuestran el impacto inmediato sobre las tasas de la enfermedad meningocócica tipo B en la población objetivo del programa después de dos dosis de la vacuna. Se esperan más datos a finales de este año cuando los primeros lactantes del programa reciban su dosis de refuerzo.
Linda Glennie, jefa de investigación de la Fundación de Investigación de la Meningitis, dice que "es estupendo tener esta evidencia temprana de que el programa nacional de inmunización frente a la meningitis B para los lactantes menores de un año es efectivo. Esperamos que otros países afectados por la meningitis B comiencen a considerar la protección de su población frente a esta enfermedad mortal. La meningitis y la septicemia pueden matar en horas y dejar un número considerable de supervivientes con secuelas que cambiarán su vida. Vamos a seguir reuniendo evidencia científica que permitan aumentar los conocimientos acerca de la vacunación frente a la meningitis B". La incidencia más alta de meningitis B se da en lactantes menores de un año de edad y el objetivo último de la vacunación meningocócica es reducir la carga total de la enfermedad. Los datos presentados ayer en la IPNC muestran que esto está pasando ahora en el Reino Unido.
Autor/a: Irum Shahid
Fuente: www.freeimages.com
Cervarix, autorizada para la prevención del cáncer anal asociado al VPH
Por otro lado, GlaxoSmithKline plc (LSE: GSK) también informa que la Comisión Europea ha aprobado la indicación de Cervarix® (vacuna frente al virus del papiloma humano [tipos 16 y 18] (recombinante, adyuvada, adsorbida)) frente al cáncer anal asociado al VPH, lo que permite el acceso a la vacunación frente al VPH a hombres y mujeres, a fin de prevenir en ambos sexos el cáncer anal asociado al VPH en los 28 países de la Unión Europea. Los ensayos clínicos han demostrado que Cervarix® induce una respuesta inmune comparable en hombres y mujeres. Se ha demostrado una eficacia del 83,6% frente a infección anal por los tipos de VPH 16/18 en mujeres sin antecedentes de infección por VPH en el momento de la vacunación.[5] Se ha estudiado la inmunogenicidad y la seguridad de Cervarix® en hombres en dos ensayos clínicos[6,7], que han demostrado que Cervarix® es bien tolerada, con un perfil de seguridad aceptable e induce una respuesta inmune similar a la obtenida en mujeres.[6,8]
Pese a que el cáncer anal es poco frecuente, su incidencia está aumentando aproximadamente un 2% por año entre hombres (1,5 por cada 100.000) y mujeres (2,0 por cada 100.000) en la población general.[9,10] El cáncer anal es más frecuente entre determinados grupos de alto riesgo (es decir, hombres que mantienen relaciones sexuales con otros hombres [HSH], hombres y mujeres infectados por el VIH y personas inmunodeprimidas).[11,12]
HZ/su, eficaz frente al herpes zóster
La citada compañía, GSK, anuncia asimismo la publicación de los resultados de un estudio aleatorizado de fase III (ZOE-70) realizado con su vacuna en desarrollo frente al herpes zóster, HZ/su. Los resultados demuestran una eficacia vacunal del 90% en adultos a partir de 70 años que se mantiene durante al menos cuatro años[13]. Los resultados han sido publicados en la revista ‘New England Journal of Medicine’ (NEJM). El estudio, cuyos resultados preliminares fueron comunicados en octubre de 2015, demostró que la vacuna en desarrollo frente al herpes zóster administrada con una pauta de dos dosis tuvo una eficacia del 90% (intervalo de confianza del 95%: 84%-94%) en comparación con placebo en personas a partir de 70 años. La eficacia de la vacuna fue similar en todos los grupos de edad incluidos en el estudio, siendo del 90% en los sujetos entre 70-79 años de edad (intervalo de confianza del 95%: 83%-94%) y del 89% en los sujetos a partir de 80 años[13] (intervalo de confianza del 95%: 74%-96%)[13].
Esta elevada eficacia está en línea con los resultados del ensayo ZOE-50, un estudio realizado en adultos a partir de 50 años que fue presentado y publicado el año pasado y en el que se observó una eficacia vacunal del 97% (intervalo de confianza del 95%: 93%- 99%)[14]. En un análisis combinado de los datos de ambos ensayos se observó una eficacia del 91% frente al herpes zóster (intervalo de confianza del 95%: 86%-95%) en adultos a partir de 70 años en comparación con placebo[13]. Esta eficacia se mantuvo, con una reducción del 88% del riesgo de herpes zóster (intervalo de confianza del 95%: 73%-95%) en el cuarto año después de la vacunación.
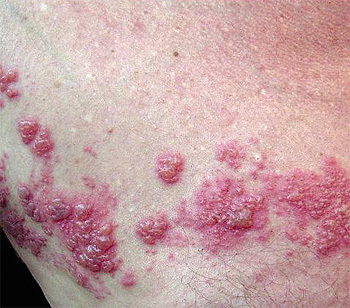
Manifestación de herpes zóster
Fuente: www.farmacosalud.com / Fisle / Wikimedia Commons
El riesgo de acontecimientos adversos graves, enfermedades potencialmente mediadas por el sistema inmune o muerte, observado en el estudio ZOE-70, fue similar en las personas que recibieron la vacuna y en las que recibieron placebo. La reacción adversa local más frecuente fue dolor en el lugar de la inyección y la reacción adversa sistémica más frecuente fue cansancio. La mayoría de las reacciones en el lugar de la inyección y de las reacciones sistémicas ocurrieron en los siete días siguientes a la vacunación. La mayor parte de estas duraron de 1 a 3 días y su intensidad fue generalmente de leve a moderada[13]. Además, en un análisis combinado de los datos de los ensayos ZOE-70 y ZOE-50 se observó que la vacuna en desarrollo redujo el riesgo de dolor neuropático crónico, también conocido como neuralgia postherpética (NPH)1, que es la complicación más frecuente y a menudo grave del herpes zóster[15,16]. La vacuna en desarrollo demostró una eficacia del 89% (intervalo de confianza del 95%: 68%-97%) para prevenir la NPH en adultos a partir de 70 años y del 91% (intervalo de confianza del 95%: 75%-98%) en adultos a partir de 50 años[13].
Avances en vacunación del adulto en territorio español
Fruto del rápido envejecimiento de la población y el aumento de la cronicidad y la dependencia, la prevención del adulto frente a enfermedades infecciosas cada vez cobra mayor importancia. Aun así, las estrategias de vacunación del adulto no gozan de la misma aceptación, ni de las mismas coberturas que las políticas de prevención infantil, a pesar de que contribuyen a garantizar su envejecimiento saludable. Para hacer frente a esta situación, tanto sociedades científicas, como profesionales sanitarios y fundaciones recomiendan a las autoridades sanitarias el desarrollo de un calendario sistemático de vacunación para el adulto, que sirva como referencia a profesionales sanitarios y recoja todas aquellas vacunas que han demostrado su eficacia, es decir, tanto las recomendadas como las financiadas.
En este sentido, 2016 está siendo un buen año: cinco Comunidades Autónomas han publicado su calendario de vacunas para el adulto (Baleares, Castilla y León, La Rioja, Navarra y País Vasco) y una más, Murcia, lo ha actualizado. Así, ya son trece las comunidades españolas que de alguna manera contemplan la prevención del adulto mediante vacunación, aunque bien es cierto que en algunos casos es mejorable al limitarse la protección a preparados de recuerdo, informa la Fundación Edad&Vida. Desde la Fundación reclaman la creación de una estrategia común de vacunación del adulto en todas las Comunidades Autónomas que "incluya todas las vacunas que se hayan demostrado coste-efectivas, ya que ahora cada Comunidad cuenta con unas vacunas financiadas y otras no".
Referencias
1. Ficha Técnica de Bexsero. 06/2016 GSK
2. In line with the recommendations made by the Joint Committee on Vaccination and Immunisation, (JCVI). JCVI position statement on use of Bexsero® meningococcal B vaccine in the UK. Marzo 2014. https://www.gov.uk/government/uploads/system/uploads/attachment_data/file/294245/JCVI_Statement_on_MenB.pdf
3. WHO factsheet: http://www.who.int/mediacentre/factsheets/fs141/en/
4. Viner RM, et al. Lancet Neurol. 2012;11:774-783
5. Kreimer A et al. Lancet Oncology, 2011, 12(9): 862–870.
6. Petäjä T et al. Immunogenicity and safety of human papillomavirus (HPV)-16/18 AS04-adjuvanted vaccine in healthy boys aged 10-18 years. J Adolesc Health. 2009 Jan;44(1):33-40.
7. Study HPV-040 results available on https://clinicaltrials.gov/ct2/show/results/NCT00534638?term=Cervarix+AND+Finland&rank=3(último acceso 5 de agosto, 2016).
8. Angelo MG et al. Pharmacoepidemiology and drug safety 2014; 23: 466–479.
9. Moscicki et al. J Low Genit Tract Dis. 2015;19 (3 Suppl 1):S27-42.
10. Johnson et al. Cancer 2004;101:281-8.
11. Palefsky J. Curr Opin HIV AIDS 2009;4:52-6.
12. Patel et al. Int J Colorectal Dis 2007;22:1-5.
13. Cunningham et al., N Engl J Med 2016; 375: 1019-32. Efficacy of the herpes zoster subunit vaccine in adults 70 years of age or older.
14. Lal et al., N Engl J Med 2015; 372:2087-2096 Efficacy of an Adjuvanted Herpes Zoster Subunit Vaccine in Older Adults
15. Shingles (Herpes Zoster) Clinical Overview. US Centers for Disease Control and Prevention. Accessed at: http://www.cdc.gov/shingles/hcp/clinical-overview.html on 6 Sept 2016.
16. Cohen et al., N Engl J Med 2013;369:255-63 Clinical practice: Herpes zoster.




