Redacción Farmacosalud.com
Las compañías Merck y Pfizer han anunciado la llegada a España de BAVENCIO® (avelumab), la primera y única inmunoterapia para el tratamiento de pacientes adultos con carcinoma de células de Merkel (CCM) metastásico. El CCM es un tipo de cáncer de piel que resulta más agresivo que el melanoma y es considerado como una enfermedad ultra-rara (afecta a menos de 1 persona por cada 50.000 habitantes), para la que hasta ahora no existía ningún tratamiento indicado. Las buenas prestaciones de avelumab en primera línea han llevado al doctor Jaume Capdevila, responsable de la Unidad de Tumores Gastrointestinales y Endocrinos del Servicio de Oncología del Hospital Universitario Vall d'Hebron y del Instituto Oncológico Vall d’Hebron (VHIO) [Barcelona], a sugerir que, por norma, los pacientes de CCM deberían recibir el nuevo fármaco como primera opción terapéutica.
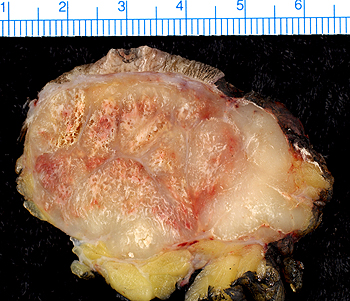
Carcinoma de células de Merkel. Muestra macroscópica
Autor/a de la imagen: Ed Uthman from Houston, TX, USA - Merkel Cell Carcinoma
Fuente: Wikipedia
El carcinoma de células de Merkel se manifiesta a través de nódulos enrojecidos de rápido crecimiento en zonas expuestas (cabeza, cara, piernas y brazos) que pueden expandirse a los ganglios linfáticos sin provocar dolor ni picor al paciente. “La aparición de pequeñas lesiones en la piel se puede asociar fácilmente a la edad (avanzada) y no a tumores, retrasando el diagnóstico y reduciendo las posibilidades de curación”, explica Capdevila a través de un comunicado difundido por Merck y Pfizer. A pesar del alto impacto para la salud que supone sufrir esta patología, el CCM continúa siendo un gran desconocido socialmente debido a su baja incidencia. En Europa se diagnostican alrededor de 2.500 casos cada año.
“Hasta este momento teníamos una quimioterapia compleja de administrar”
Hasta ahora, los afectados no disponían de ninguna opción de tratamiento indicada y su pronóstico resultaba dramático, especialmente en estadio metastásico (entre el 5 y el 12% de los pacientes): menos del 20% de los pacientes de este subgrupo presentan una supervivencia superior a 5 años. Frente a esta realidad, acaba de llegar a España avelumab, la primera y única inmunoterapia indicada para enfermos adultos con carcinoma de células de Merkel metastásico.
“La llegada de la inmunoterapia ha dado una oportunidad completamente distinta a los pacientes con esta enfermedad. Hasta este momento teníamos una quimioterapia compleja de administrar -por la falta de evidencia de actividad en estudios clínicos bien establecidos-, y porque el perfil de paciente con CCM es algo más peculiar, dado que ese tumor aparece básicamente en pacientes añosos (habitualmente mayores de 75 años), quienes, evidentemente, tienen comorbilidades y eso hace que las quimioterapias no se puedan administrar con la tranquilidad con la que sí se administran a pacientes más jóvenes o con menos comorbilidades”, comenta Capdevila. Otros de los grupos poblacionales en los que el carcinoma de Merkel tiene más incidencia son aquellos en que los afectados presentan problemas de salud relacionados con la inmunosupresión, trasplantes, enfermedades autoinmunitarias o por deficiencia inmunitaria (VIH, virus causante del Sida).
Los datos con avelumab son mejores en primera que en segunda línea
En CCM metastásico, la respuesta a la quimioterapia es de escasa duración en la mayoría de los casos y está acompañada de una supervivencia muy corta. Sin embargo, si avelumab se utiliza en primera línea se puede controlar el tumor en la mayoría de los pacientes, consiguiendo respuestas en más del 50% de los casos. A todo esto, ninguno de los afectados sobrevive al año de tratamiento en segunda línea con quimioterapia, mientras que con avelumab más del 30% responde y, de ellos, más del 50% se mantiene vivo tras un año de tratamiento. “Los datos con avelumab son mejores en primera que en segunda línea: tenemos más tasa de respuestas, más reducciones tumorales, y estas tasas de respuesta y reducciones duran mucho tiempo, o sea, los pacientes son largo-respondedores”, asegura el doctor Capdevila.

Un momento de la presentación de avelumab
Fuente: Merck / Pfizer / Weber Shandwick
El caso es que, por ahora, se han recogido más datos de seguimiento en segunda línea que en primera porque el estudio en primera línea se cerró hace escasamente un año, y como los pacientes tratados en primera línea son largo-respondedores, habrá que esperar un poco más para tener datos más maduros y una visión más completa de conjunto. Con todo, el oncólogo apela a la lógica a la hora de apostar por avelumab como primera opción de tratamiento: “Si bien el fármaco acaba de llegar al mercado y por lo tanto llevará un tiempo analizar su uso, difusión y conocimiento, para mí el mensaje es que todos los pacientes de carcinoma de Merkel metastásico deberían recibir avelumab en primera línea porque es más eficaz en primera línea que en segunda, y porque es más seguro y tiene menos toxicidad”. Eso no quita que, según comenta Capdevila en declaraciones a www.farmacosalud.com, ese tipo de administración deba estudiarse caso por caso con el fin de evitar su aplicación masiva en todos los supuestos, entre otras razones porque el 100% en medicina (también en el ámbito del CCM) es casi imposible.
Avelumab es un anticuerpo monoclonal anti PD-L1 que actúa sobre el sistema inmune por una doble vía: restaurando la inmunidad adquirida y también activando la inmunidad innata. Avelumab es un anticuerpo humano específico para una proteína denominada PD-L1 o ligando de muerte programada[1]. Se ha diseñado para ejercer un efecto potencial en los sistemas innato y adaptativo. Mediante su unión a PD-L1, se considera que el fármaco impide que las células tumorales utilicen la unión de PD1 y PD-L1 para evadir la respuesta antitumoral inducida por los linfocitos. Se ha demostrado que avelumab induce citotoxicidad mediada por células dependientes de anticuerpos (ADCC) in vitro.
No existen datos que avalen el uso de avelumab en estadíos tempranos de CCM
Según la doctora Ana Arance, especialista sénior del Servicio de Oncología Médica del Hospital Clínic (Barcelona), “la inmuno-oncología es una estrategia terapéutica muy atractiva porque permite al sistema inmune reconocer, actuar y eliminar a las células tumorales, dondequiera que estén en el cuerpo, lo que la convierte en un arma universal contra más tipos tumorales y para salvar más vidas. Además, los ensayos clínicos han demostrado que la inmunoterapia en cáncer ofrece la posibilidad de un control a largo plazo de esta enfermedad que se mantiene incluso después de que el tratamiento ha sido completado”.
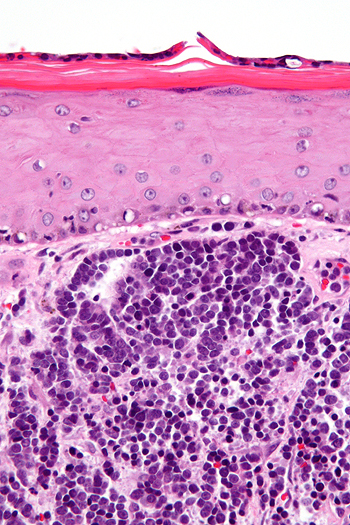
Microfotografía de un carcinoma de células de Merkel. Tinción hematoxilina-eosina
Autor/a de la imagen: Nephron (trabajo propio)
Fuente: References (Feb 2008). "Clonal integration of a polyomavirus in human Merkel cell carcinoma.". Science 319 (5866): 1096-100. DOI:10.1126/science.1152586. / Wikipedia
Para el doctor Capdevila, hoy en día no existen datos de adyuvancia que avalen el uso de avelumab en estadíos tempranos de carcinoma de células de Merkel, es decir, no se ha estudiado el uso de avelumab tras la resección del tumor y cuando hay un riesgo elevado de que ese tumor reaparezca. “Otra cosa distinta son los tumores localmente avanzados pero que no tienen metástasis -puntualiza el experto-. Esta enfermedad aparece muchas veces en las zonas fotoexpuestas (cara) y las cirugías extensas en el rostro (y más en gente mayor) son mucho más complejas. Con la tasa de respuestas tan grande que tiene este fármaco, parece lógico intentar reducir el tumor para que luego la cirugía sea más fácil o más consoladora”.
No obstante, el responsable de la Unidad de Tumores Gastrointestinales y Endocrinos del Servicio de Oncología del Hospital Universitario Vall d'Hebron advierte que los pacientes con CCM localmente avanzado pero no metastásico no se incluyeron en el estudio JAVELIN de aprobación de avelumab, de manera que faltan datos que avalen su uso en esos casos. “Por lo tanto, no estaríamos hablando de la propia ficha técnica del producto; hay que dejar bien claro que estos pacientes no entraron en el estudio y, por tanto, no estamos induciendo a una medicación fuera de indicación. Si bien faltan datos, la lógica sería: en enfermedad localmente avanzada o irresecable y en la que la cirugía sería demasiado ‘mutilante’, avelumab reduciría el tumor y luego podríamos tener cirugía de rescate, incluso con enfermedad metastásica… pero insisto, faltan datos para llegar hasta aquí”.
Dos tipos de carcinoma de células de Merkel
Por otro lado, un estudio conocido recientemente demuestra la capacidad de un biomarcador genómico para predecir la respuesta al tratamiento con inmunoterapia, independientemente del tipo de cáncer. Se trata de PD1, un receptor presente en los linfocitos, que son unas células inmunológicas clave en la respuesta contra el cáncer[2]. Dado que avelumab impide que las células tumorales utilicen la unión de PD1 y PDL-1 para evadir la respuesta antitumoral inducida por los linfocitos, cabe pensar que el nuevo hallazgo genómico podría ser de gran ayuda a la hora de predecir la capacidad de respuesta a avelumab en carcinoma de células de Merkel.
Sin embargo, parece que el descubrimiento del biomarcador PD1 vinculado a PD-L1 no sería de tanta utilidad en el CCM porque la inmunoterapia, por las propias condiciones de esta enfermedad, ya es muy eficaz de per se. “En el estudio JAVELIN se miró la expresión de PDL-1 y no se vio diferencia entre aquellos pacientes que presentaban altos o bajos niveles de expresión de PDL-1”, indica el especialista. Esto se explica por la característica que diferencia al carcinoma de Merkel del resto de tumores: las dos clases en que se divide el CCM son muy identificables a ojos del sistema inmune.
Uno de los dos tipos del CCM se define por ser inducido por la exposición solar, y por presentar un elevado número de mutaciones en el genoma tumoral. Está visto que elevar la carga mutacional de los tumores se correlaciona con un incremento de neoantígenos (proteínas aberrantes que genera la mutación), lo que a su vez facilita que los neoantígenos sean detectados como extraños y en consecuencia atacados por el sistema inmunitario del enfermo. Así, los tumores que tienen una alta carga mutacional en su DNA son buenos respondedores (por suerte para el paciente) a la inmunoterapia, tengan altos o bajos los niveles de PDL-1.
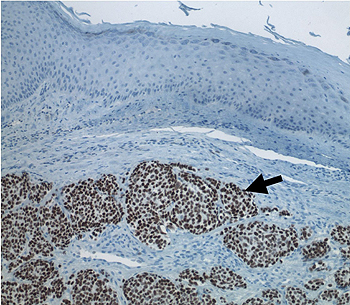
Carcinoma de células de Merkel (flecha) infiltrando el tejido cutáneo; se muestra en tono café la cadena de proteína T del Poliomavirus de las células de Merkel
Autor/a de la imagen: Patrick S. Moore (original creation)
Fuente: Wikipedia
El otro tipo de carcinoma de Merkel es aquel que está asociado a la infección crónica por el virus del polioma. Este virus genera un tumor ligeramente distinto al hipermutado e inducido por la exposición al sol, ya que los tumores vinculados al polioma incorporan en su DNA el genoma viral, y esto hace que se generen neoantígenos por la infección de dicho virus. Por lo tanto, el sistema inmunitario también es capaz de detectar a los neoantígenos generados por la infección del virus del polioma. En resumen, ya sea por un lado o por otro, son tumores que generan muchos antígenos nuevos y extraños que el sistema inmunitario es capaz de detectar.
Un medicamento con buen perfil de tolerancia
Por otra parte, avelumab presenta “el mismo perfil de efectos adversos que todos los inhibidores de PD1 / PD-L1. La verdad es que son fármacos excelentes en cuanto a tolerancia; el fármaco en sí no es anticancerígeno, por lo que no mata células tumorales por sí, ni mata células no tumorales… lo que hace es activar el sistema inmunitario y es el linfocito el que acabará destruyendo al tumor. Por tanto, a no ser que seas alérgico cuando te lo administran, a priori con avelumab no deberían aparecer efectos secundarios”, precisa Capdevila.
“Lo que pasa es que, como en toda inmunoterapia, la similitud entre antígenos tumorales y antígenos de tejidos normales a veces comporta que el linfocito pueda equivocarse de diana y empiece a atacar al tumor y a un tejido sano. Entonces, aparecen las toxicidades inmunomediadas, que son típicas de todos los anti PD1 y PD-L1. Aun así, el porcentaje de toxicidades es muy bajo. Habitualmente, las toxicidades grado 3-4 (que son las que limitan la administración del fármaco) son inferiores al 5% comparadas con quimioterapia y terapias dirigidas. En el estudio de avelumab, incluso las toxicidades de grado 1-2 (que son las que se manejan con tratamiento médico y no requieren que el fármaco se suspenda) no superaban el 20%. Son fármacos que se toleran de forma excelente”, afirma.
Especial vigilancia en el caso de los pacientes trasplantados
En cuanto a las contraindicaciones, está claro que si un paciente es alérgico a un medicamento eso sólo puede saberse cuando el paciente empieza a recibir dicho fármaco. “Aunque es extremadamente raro que uno sea alérgico a un medicamento, en ocasiones se pueden generar reacciones infusionales, que se controlan con fármacos coadyuvantes; por lo tanto, eso no acostumbra a limitar el tratamiento de los pacientes”, sostiene el facultativo. Hasta hace poco, además, se pensaba que podía estar contraindicado el uso de la inmunoterapia en pacientes que son portadores de infecciones crónicas como el virus de la hepatitis o el virus del Sida, si bien “lo que estamos viendo hoy en día es que no sólo la pueden recibir sin ningún problema, sino que incluso hay algún dato de que las respuestas al tratamiento pueden ser incluso mejores”, señala Capdevila.

Doctor Jaume Capdevila
Fuente: Merck / Pfizer / Weber Shandwick
En el ámbito de las enfermedades autoinmunitarias (el sistema inmune ataca al propio cuerpo), “si tú das un fármaco que activa el sistema inmunitario evidentemente hay que vigilar mucho más que esas enfermedades autoinmunitarias no se reactiven con fármacos tipo avelumab. Lo que estamos viendo también es que, a medida que vamos entendiendo el mecanismo de acción y por dónde pueden avanzar los efectos adversos, controlamos más y mejor todo esto", por lo que el uso de avelumab en este tipo de patologías "ya no representa una contraindicación absoluta”, apunta el oncólogo.
Otro punto a tener muy en cuenta es el perfil de pacientes con carcinoma de Merkel que han recibido un trasplante, puesto que además de ser personas que toman fármacos inmunosupresores de por vida, pueden tener el problema de que la terapia inmunológica que reciben (como avelumab) genere una reacción autoinmunitaria contra el órgano trasplantado. No obstante, recientemente se ha recogido algún dato que parece garantizar la seguridad de la inmunoterapia en este tipo de pacientes, de manera que la contraindicación aquí tampoco sería absoluta. En cualquier caso, hay que proceder a realizar un control especial y específico de esos enfermos.
“Avelumab es una demostración de lo que ocurre cuando dos grandes compañías, como Merck y Pfizer, mantienen un firme compromiso con los pacientes que se encuentran en una situación de especial vulnerabilidad y se unen para investigar terapias frente a una patología de muy baja incidencia, como es el CCM”, afirma la Dra. Isabel Sánchez Magro, directora Médico de Merck. Por su parte, la Dra. Cecilia Guzmán, directora Médico de Oncología de Pfizer, ha resaltado el valor de esta terapia, resultado de la alianza estratégica de Merck y Pfizer en Inmuno-oncología. “La alianza refleja la unión del talento de nuestros equipos, de nuestros bagajes en Oncología y de los recursos de ambas compañías como vehículo de consecución de nuestro objetivo principal: desarrollar programas de investigación clínica para abrir nuevos caminos para afrontar el cáncer”.
Acerca de JAVELIN Merkel 200
El ensayo Javelin Merkel 200 es el mayor ensayo que se ha realizado en esta patología y ha demostrado la eficacia y seguridad de avelumab:
• La Parte A se llevó a cabo en 88 pacientes con confirmación histológica de CCM metastásico cuya enfermedad progresó durante o después de recibir quimioterapia para la enfermedad metastásica distante.
• La Parte B, llevada a cabo en pacientes en primera línea de tratamiento, incluyó a 112 pacientes para evaluar la eficacia en relación a las respuestas duraderas en al menos 6 meses.
Los pacientes recibieron 10 mg/kg de avelumab como infusión.

(de izq. a dcha): Doctores Cecilia Guzmán, directora Médico de Oncología de Pfizer; Jaume Capdevila, responsable de la Unidad de Tumores Gastrointestinales y Endocrinos del Servicio de Oncología del Hospital Universitario Vall d'Hebron y del Instituto Oncológico Vall d’Hebron (VHIO); Ana Arance, especialista sénior del Servicio de Oncología Médica del Hospital Clínic Barcelona, e Isabel Sánchez Magro, directora Médico de Merck
Fuente: Merck / Pfizer / Weber Shandwick
El CCM metastásico es una enfermedad agresiva y poco frecuente en la que las células neoplásicas se disponen en la capa superior de la piel y suele aparecer en zonas de la piel expuestas al sol con más frecuencia, incluyendo la cabeza, el cuello y los brazos[1,3]. Los factores de riesgo del CCM son la exposición al sol, la edad, los pacientes inmunocomprometidos y la infección con poliomavirus de células de Merkel. Este tipo de tumores se suele diagnosticar erróneamente como otro tipo de cáncer cutáneo, dado que su apariencia y sintomatología es poco específica. Las opciones terapéuticas actuales para el CCM en Europa son cirugía, radiación y quimioterapia[4].
Referencias
1. Schadendorf D et al. Merkel cell carcinoma: epidemiology, prognosis, therapy and unmet medical needs. European Journal of Cancer 2017;71;53–69
2. www.farmacosalud.com “PD1, nuevo biomarcador que predice la respuesta a la inmunoterapia en cáncer”. Noticia publicada en septiembre de 2018. Difusión online: http://farmacosalud.com/pd1-nuevo-biomarcador-que-predice-la-respuesta-la-inmunoterapia-en-cancer/
3. Nghiem P. Systematic literature review of efficacy, safety and tolerability outcomes of chemotherapy regimens in patients with metastatic Merkel cell carcinoma. Future Oncology 2017;13(14):1263–1279.
4. American Cancer Society. What is Merkel cell carcinoma? http://www.cancer.org/cancer/skincancer-merkelcell/detailedguide/skin-cancer-merkel-cell-carcinoma-what-is-merkel-cell-carcinoma. Last accessed June 2017.




