Redacción Farmacosalud.com
Idorsia, compañía biofarmacéutica especializada en el desarrollo y comercialización de tratamientos con moléculas pequeñas, acaba de iniciar su actividad en España. “Las moléculas pequeñas son aquellas que tienen un peso molecular por debajo de 1000 Daltons, lo que facilita que lleguen allá donde tienen que ejercer su efecto. La investigación en Idorsia se centra en familias de proteínas que hasta ahora no se habían trabajado”, detalla la Dra. Verónica de Miguel, directora médica de la compañía en España.
Uno de los medicamentos de Idorsia que están en período de análisis es aprocitentan, cuyo uso está siendo evaluado en hipertensión arterial (HTA) resistente, “un subtipo de hipertensión con mal pronóstico hasta la fecha. De acuerdo con los resultados preliminares del ensayo en fase 3 Precision, en la semana 4 de tratamiento ya se observa una reducción de la presión arterial que se mantiene durante un periodo de 48 semanas”, explica De Miguel. Por lo pronto, el primer fármaco de la compañía que ya ha recibido la autorización de comercialización en Europa es daridorexant, indicado para el tratamiento del insomnio crónico en adultos. Una vez iniciados los procesos administrativos y regulatorios para solicitar su aprobación y comercialización en territorio español, “desde Idorsia España esperamos que daridorexant pueda llegar a las personas que lo precisen y, para ello, estaremos a disposición de las autoridades sanitarias españolas”, señala.

(de izq. a dcha): la Dra. Verónica de Miguel, directora médica; Manuel Ortega, director general, y Olga Espallardo, directora de Market Access de Idorsia España
Fuente: Idorsia / Cícero Comunicación
-Su compañía, con sede en Suiza, nació en 2017. Precisión de reloj suizo y ‘pasión’ española… ¿buena combinación para esta nueva singladura?
Es la combinación perfecta. En Idorsia nos apasionan la ciencia y la precisión. Nos centramos en los detalles, lo que nos lleva a desarrollar nuestras innovaciones farmacológicas de forma muy minuciosa y seleccionando el perfil más adecuado para los pacientes. Esto implica invertir en explorar y, en ocasiones, tomar la difícil decisión de desechar muchas moléculas candidatas hasta que damos con la que cumple con nuestros criterios científicos y de calidad. Esta misma pasión y entrega a la actividad científica es la que nos empuja a luchar, con mucha resiliencia, frente a los retos que se nos plantean por el camino, y de este modo, perseverar en nuestros objetivos y filosofía.
-Las moléculas pequeñas, con bajo peso molecular, gozan de una mayor capacidad para atravesar las membranas celulares rápidamente, dando lugar a mecanismos de acción novedosos que permiten avances cualitativos en el abordaje de las patologías. ¿Estamos hablando de nanopartículas, o bien no es lo mismo?
Las moléculas pequeñas son aquellas que tienen un peso molecular por debajo de 1000 Daltons, lo que facilita que lleguen allá donde tienen que ejercer su efecto. La investigación en Idorsia se centra en familias de proteínas que hasta ahora no se habían trabajado, y estamos demostrando que se pueden desarrollar fármacos con mecanismos de acción novedosos.

Manuel Ortega, director general de Idorsia España
Fuente: Idorsia / Cícero Comunicación
Trabajar con moléculas pequeñas exige un dominio, una precisión exquisita del proceso de síntesis y desarrollo, en el que los investigadores de Idorsia llevan embarcados más de dos décadas, así como integrar tecnologías punteras como es la Inteligencia Artificial aplicadas al diseño de fármacos.
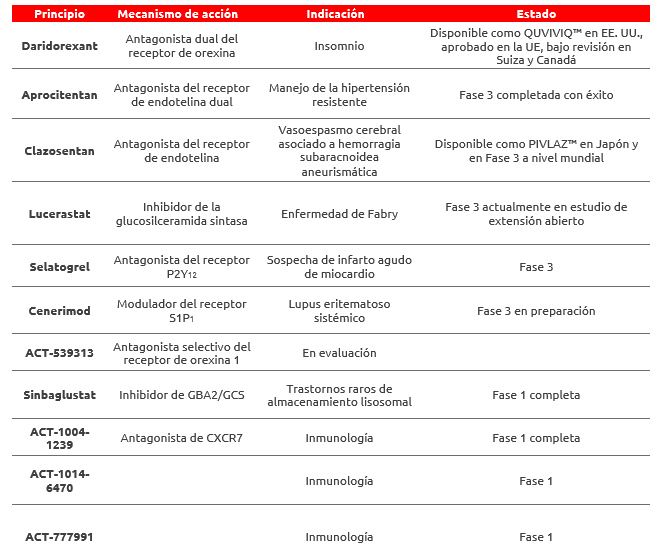
-De las cinco moléculas de Idorsia que se encuentran en fase III de desarrollo, aprocitentan está enfocada al manejo de la hipertensión resistente y cenerimod al lupus eritematoso sistémico. ¿Qué eficacia han mostrado ambos medicamentos hasta el momento?
Aprocitentan es un inhibidor dual de receptores de endotelina que está siendo evaluado en la hipertensión arterial resistente, un subtipo de hipertensión con mal pronóstico hasta la fecha. De acuerdo con los resultados preliminares del ensayo en fase 3 Precision, en la semana 4 de tratamiento ya se observa una reducción de la presión arterial que se mantiene durante un periodo de 48 semanas, con una buena tolerancia.
Cenerimod es un modulador de receptores S1P1 que está siendo investigado para el tratamiento del lupus moderado o grave. Tras completar con éxito la fase 2b, ha iniciado la fase 3.
-Selatogrel es un tratamiento centrado en la sospecha de infarto agudo de miocardio, lucerastat está pensado para el abordaje de la enfermedad de Fabry y clazosentan busca tener efectos en la prevención del vasoespasmo cerebral asociado con hemorragia subaracnoidea aneurismática. ¿Qué puede explicarnos acerca de esos nuevos medicamentos?
Es demasiado temprano para hablar de su eficacia, ya que estas moléculas aún están completando su desarrollo clínico. En cualquier caso, lo que tienen en común es que todas ellas nacen de la necesidad de aportar soluciones para enfermedades que hasta ahora carecen de un tratamiento satisfactorio y sobre las que aún hay necesidades no cubiertas.
Destacaría el caso de clazosentan, un inhibidor selectivo del receptor de endotelina A, que busca revertir el efecto de los agentes vasoconstrictores que se liberan tempranamente tras la intervención inicial del aneurisma y que condicionan en gran medida complicaciones como un déficit neurológico posterior. Por su parte, Selatogrel es un antagonista reversible del receptor P2Y12, y está siendo estudiado como fármaco antiagregante subcutáneo en pacientes con infarto agudo de miocardio en los que se busca un rápido inicio de los efectos terapéuticos para mejorar el pronóstico del propio infarto. Por último, Lucerastat es un inhibidor de la síntesis de glucosilceramida que continua con su desarrollo para la enfermedad de Fabry, en espera de completar la extensión no enmascarada del ensayo en fase 3 Modify.
-Ustedes trabajan, además, en la fase 1 de desarrollo de otras moléculas en el campo de la inmunología y los trastornos en el almacenamiento lisosomal.
Idorsia tiene un programa de desarrollo de fármacos diversificado y a la vez muy focalizado, que abarca áreas terapéuticas que incluyen el sistema nervioso central, enfermedades cardiovasculares, trastornos de origen inmunológico y enfermedades huérfanas. Todos estos desarrollos tienen algo en común: moléculas pequeñas en áreas terapéuticas donde existen necesidades no cubiertas y a las que otros no han llegado.
Fuente: Idorsia / Cícero Comunicación
-El primer fármaco de la cartera de Idorsia que ha recibido la autorización de comercialización en Europa es daridorexant, indicado para el tratamiento del insomnio crónico en adultos. ¿Tras su aprobación este pasado mes de mayo, cuándo calculan que daridorexant llegará a España? ¿Podría ser incluso ser financiado por la sanidad pública española?
Estamos muy contentos porque daridorexant es la primera orexina que recibe la aprobación para su comercialización en Europa tras 20 años sin que, en el campo del insomnio crónico, haya habido innovaciones. Ahora estamos en las fases más tempranas y, por tanto, iniciando los procesos administrativos y regulatorios a nivel nacional para solicitar su aprobación y comercialización en España y en otros países europeos. Desde Idorsia España esperamos que daridorexant pueda llegar a las personas que lo precisen y, para ello, estaremos a disposición de las autoridades sanitarias españolas.




