Drs. Ana Rosa Jurado y Francisco José Brenes / Redacción Farmacosalud.com
Las infecciones del tracto urinario (ITUs), después de las infecciones respiratorias, son la segunda causa de consulta por patología infecciosa en Atención Primaria[1,2]. Más del 50% de las mujeres presentarán al menos un episodio de ITU en su vida[2]. Generalmente se trata de ITUs no complicadas. Se considera que una ITU es no complicada cuando se presenta en individuos cuyos mecanismos de defensa se encuentran intactos y con un tracto urinario estructuralmente normal[1]. Dentro de las ITUs no complicadas, la más frecuente en la mujer es la cistitis[1].
El tratamiento de las cistitis en la mujer, debido a las características generalmente leves y la ausencia de complicaciones, suele ser empírico en base a los gérmenes habitualmente aislados y su sensibilidad a la acción de distintos antimicrobianos[1,2], por lo que periódicamente debemos conocer cuál es en nuestra zona geográfica la etiología de la ITU no complicada, la resistencia bacteriana y la actividad de los antibióticos, para que pautemos el tratamiento empírico más adecuado[1,3,4].

Autor/a: StockSnap
Fuente: Pixabay / Creative Commons
Aproximadamente un tercio de las mujeres afectas de ITU presentarán recurrencias (2 o > infecciones en 6 meses o 3 o > infecciones en un año) [2,5]. A diferencia de las cistitis aisladas, cuyo diagnóstico se realiza en base a criterios clínicos (síndrome miccional) y la tira reactiva colorimétrica de orina, las cistitis recurrentes deben diagnosticarse mediante urocultivo[6], y si son muy recidivantes podría ser necesario realizar estudios de las vías urinarias[2,7]. Las cistitis recurrentes requieren una atención especial, se asocian con una considerable morbilidad, alteraciones de la calidad de vida y uso de servicios de salud. Las características clínicas y gérmenes causantes suelen ser similares a los de los casos de cistitis aisladas[1,2,5].
Alternativas terapéuticas para las ITUs
La estrategia terapéutica clásica para su prevención se ha realizado mediante antibióticos (profilaxis antibiótica continua y postcoital, autotratamiento) [2,5,6], “por lo que es muy importante que consideremos las consecuencias que pueda tener en la flora vaginal y en la aparición de resistencias, el uso de antibióticos durante periodos largos de tiempo”, afirma el Dr. Francisco José Brenes, médico de Familia en el Centro de Atención Primaria Llefià, de Badalona (Barcelona), y miembro del Grupo de Trabajo de Nefrourología de la Sociedad Española de Médicos de Atención Primaria (SEMERGEN).
En la última década se ha avanzado considerablemente en el conocimiento de la patogenia y estrategias de prevención de las ITUs recurrentes. Así, se han añadido otras alternativas terapéuticas como la toma de extractos de arándano rojo americano, lactobacillus oral y de aplicación vaginal, estrógenos tópicos en la atrofia vaginal y, más recientemente, las vacunas[2,6].
La mayoría de las ITUs se generan por vía ascendente[1]. “Habitualmente están producidas por microorganismos aerobios gramnegativos procedentes de la zona del colon (enterobacterias); estos gérmenes suelen estar presentes en la zona periuretral y en el introito vaginal”, explica el Dr. Brenes. En España, Escherichia coli (E.coli) es el uropatógeno más frecuente en mujeres de 18 a 65 años (79,2%)[8], seguido a gran distancia por Staphylococcus saprophyticus (4,4%); más aislado en mujeres < 30 años de edad, Proteus mirabilis (4,3%); más aislado en mujeres > 50 años de edad, Enterococcus faecalis (3,2%) y Klebsiella pneumoniae (2,3%).

Autor/a: George Hodan
Fuente: www.publicdomainpictures.net
La ITU es el resultado de la interacción de un germen (patógeno) y el huésped. Los gérmenes -que son más frecuentes a nivel del introito vaginal- presentan una serie de características que pueden influir sobre su capacidad infectiva, aunque ésta será más o menos importante dependiendo de la capacidad defensiva que tenga el huésped. En la mujer sana este mecanismo defensivo fundamentalmente se debe a la presencia de lactobacillus; su función defensiva se debe a su capacidad de producir sustancias antimicrobianas como peróxido de hidrógeno (H2O2), que inhibe el crecimiento de los patógenos, a la producción de ácido láctico y surfactantes, que impiden la adherencia bacteriana, y a la capacidad que tienen los lactobacillus de estimular otras defensas del huésped como citoquinas, macrófagos y leucocitos[9-11].
En determinadas circunstancias, existe una disminución del número de lactobacillus por deficiencia estrogénica, tratamiento antibiótico, uso de espermicidas, etc, alterándose la capa protectora que éstos generan a nivel del tracto urogenital[2,6,11].
Las enterobacterias, en una primera fase, colonizan el introito vaginal y la región periuretral[1]. “Un pequeño número de bacterias consigue ascender hasta la vejiga y más excepcionalmente a la pelvis y parénquima renal”, precisa Brenes. Normalmente, estas bacterias son eliminadas por el flujo y las propiedades antibacterianas de la orina, y en menor medida por la presencia de Inmunoglobulina A (IgA) secretora y los escasos polimorfonucleares presentes en la superficie vesical. Si las bacterias no son eliminadas, se inicia una colonización (adhesión del microorganismo al urotelio, reproducción de éste y eliminación por orina) o una infección (implica lesión del epitelio vesical)[1,11]. No todas las cepas de E. coli poseen la misma capacidad para infectar el aparato urinario. Sólo las cepas con determinado grado de virulencia son capaces de producir una infección en pacientes con el aparato urinario intacto[10,11]. Entre los principales factores de virulencia de la E. coli, destacan[1,11]:
• La presencia de adhesinas que permiten su adhesión al urotelio. Se encuentra en unas estructuras alargadas denominadas fimbrias de tipo 1 y P[10].
• La capacidad de estructurarse en biopelículas.
• La liberación de toxinas (hemolisinas, factor citotóxico necrotizante).
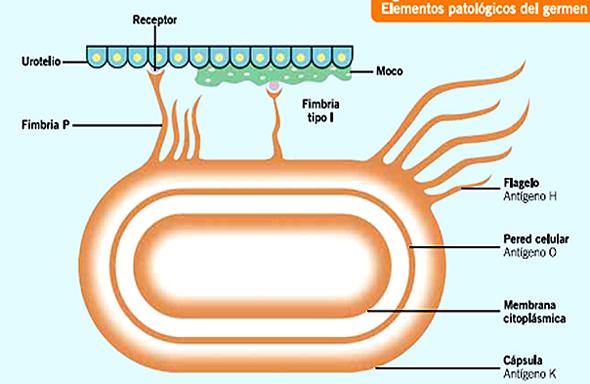
Fuente: Brenes FJ, Naval ME. Infecciones del tracto urinario. El experto responde. Preguntas y respuestas sobre patologías infecciosa en atención primaria (módulo 3). Barcelona Ed Profarmaco. 2006
Factores de riesgo
En función de la edad se pueden diferenciar varios factores de riesgo para presentar ITUs recurrentes[2,11].
En el intervalo de edad comprendido entre los 15 y los 50 años, los principales factores son: el coito, nueva pareja sexual en el año previo, uso de espermicidas, antibióticoterapia previa, ITUs previas, antecedentes de ITU en la infancia e historia de ITU familiar de primer grado en mujeres; la probabilidad de presentar ITU dependerá de diversos factores de riesgo[5,11-13]. En estas edades el coito es el principal factor de riesgo de ITU[1], ya que facilita tanto la colonización periuretral por E. coli como el ascenso del mismo hasta la vejiga. El inicio de la actividad sexual incrementa el riesgo de padecer una ITU en 3,5 veces, posteriormente según la frecuencia de su práctica se dispara desde 0 (no coitos en 7 días) a 2,6 (3 coitos en 7 días) y a 9 veces (7 coitos en 7 días)[5,7,11].
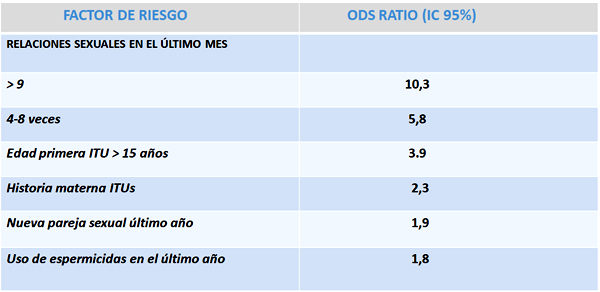
Tabla 1. Factores de riesgo ITUs
Fuente: Kodner C M,Thomas Gupton EK. Am Fam Physician. 2010 Sep 15;82(6):638-643
En mujeres postmenopáusicas entre los 50 y 70 años de edad sanas que no sean portadoras de catéter. El factor más predisponente es la disminución de los estrógenos (su déficit aumenta el pH vaginal, disminuyendo la cifra de lactobacillus y aumentando la de E coli). Otros factores son: incontinencia urinaria, cirugía urogenital, cistocele, estatus no secretor y la historia de ITU antes de la menopausia[11].
En mujeres ancianas institucionalizadas el principal factor de riesgo es el sondaje vesical y el estado funcional del sistema urinario[11].
Según la Dra. Ana Rosa Jurado, Dra. en Medicina, sexóloga en el Instituto Europeo de Sexología, y coordinadora del Grupo de Trabajo de Atención a la Mujer de SEMERGEN, hay varios factores que intervienen en el hecho de que las cistitis puedan hacerse recidivantes: “En algunos casos, puede primar la capacidad infectiva del germen, y en otros las condiciones del huésped, o ambos. Uno de los principales factores de protección del huésped viene dado por la población de lactobacilos (o lactobacillus) de la vagina, que mantiene una acidez del medio que dificulta el crecimiento de las enterobacterias (los gérmenes que más frecuentemente producen ITU)”.
En mujeres en edad reproductiva, las cistitis de repetición pueden estar más relacionadas con los cambios del pH o con la fricción mecánica de la actividad sexual, pero tras la menopausia existe un factor determinante para el desequilibrio vaginal: el déficit estrogénico, que disminuye el glucógeno que utilizan los lactobacilos en la producción de ácido láctico, lo cual implica un aumento del pH, y una reducción de la población lactobacilar[2,14].
Los probióticos aportan lactobacilos
En la última década, el uso de probióticos lactobacillus para la prevención de la ITU y restablecer la ecología vaginal está ganando cada vez más aceptación como una alternativa a la terapia antibiótica convencional[2,5,9] con un grado de evidencia IIa[6]. Su utilidad reside en la capacidad para mantener el pH vaginal en valores comprendidos entre 4 y 4,5[9,11].
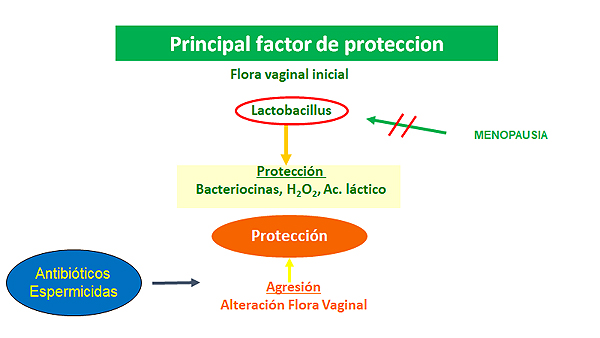
Fuente: Dr. Brenes
Las especies que están presentes en la macrobiótica vaginal varían de una mujer premenopáusica a otra postmenopáusica[15]. Antes de la menopausia, los lactobacillus son los microorganismos predominantes en la vagina de la mujer[9,11]. Protegen a la vagina frente a la colonización por uropatógenos, interfieren su adherencia al epitelio vaginal bloqueando sus receptores por mecanismos de exclusión o desplazamiento, e inhiben la multiplicación de los uropatógenos mediante la producción y excreción de diversas sustancias como H2O2, ácido láctico y bacteriocinas[5,9,15].
En estudios in vitro se ha observado que las cepas Lactobacillus plantarum CECT8675* y CECT8677* presentan una actividad bactericida elevada, lo que conlleva a una drástica reducción de la concentración de los principales patógenos de las ITU (Escherichia Coli, Proteus mirabilis, Staphylococcus saprophiticus y Klebsiella pneumoniae)[16].
Los productos probióticos aportan lactobacilos, que son los microorganismos dominantes de la microbiota vaginal. Los desequilibrios en la microbiota se deben precisamente a la reducción del número de lactobacilos, ya sea de forma directa (por productos bactericidas, antibióticos, etc.) o indirecta, como por alteraciones en el pH, hormonales, etc. Cuando disminuye el número de lactobacilos, los mecanismos de defensa de la vagina se reducen de igual modo, aumentando sobre todo el pH por la menor producción de ácido láctico, lo que permite el crecimiento de otros microorganismos que en condiciones saludables no lo harían. Se puede favorecer la invasión de patógenos, pero además se puede producir el sobrecrecimiento de gérmenes que cohabitan en condiciones normales, pero en menor número, lo cual conlleva lo que se conoce como disbacteriosis. Una vagina con menos lactobacilos también permite el sobrecrecimiento de microorganismos procedentes del intestino, lo que favorecerá su paso a la uretra para incrementar el riesgo de infecciones del tracto urinario[17].
“Los probióticos aportan una población de lactobacilos funcionantes, es decir, que son capaces de restaurar el pH vaginal para favorecer el reequilibrio bacteriano, aumentando los mecanismos de defensa típicos de la vagina”, sostiene la Dra. Jurado.
L. Rhamnosus Lcr35, eficaz frente a VB y VVC

Fuente: Archivo
En cuanto al beneficio de los probióticos en las cistitis de repetición, existen evidencias científicas que parten de ensayos controlados con placebo y de meta-análisis. Concretamente, Stapleton et al, en el 2011[18], publican un estudio donde se contrasta el efecto de un probiótico frente a placebo en mujeres que sufrían infecciones del tracto urinario de repetición. “Tras el tratamiento antibiótico, sólo el 15% de las mujeres que asociaron lactobacilos durante 5 días continuos, y después una vez a la semana, hasta completar 10 semanas, presentaron recurrencias de las infecciones urinarias, frente al 27% de las mujeres que utilizaron sólo el antibiótico y un placebo”, describe Jurado.
En algunos meta-análisis también se ha concluido sobre la buena capacidad de prevención de infecciones recurrentes del tracto urinario en mujeres tratadas con óvulos vaginales que contenían determinadas cepas de lactobacilos. Grin et al, en 2013[19] concluyen en su meta-análisis que las cepas probióticas de lactobacilos son seguras y efectivas para prevenir la ITU en mujeres, si bien se requieren más estudios controlados con placebo para poder hacer extensivas y protocolizar las recomendaciones.
Según el meta-análisis de Grin et al[19], se apreciaban buenos resultados en los estudios dependiendo de las cepas de lactobacilos que se utilizaran. Concretamente, los productos probióticos con cepas de L crispatus, o combinaciones de L rhamnosus GR-1 y L fermentum B-54, eran los productos que mejores resultados obtenían. “Es importante -expone la especialista- que los estudios utilicen cepas que hayan sido testadas in vitro y que tengan eficacia frente a los patógenos de las vías urinarias. Las cepas de L Plantarum CECT8675 y 8677 han mostrado su eficacia frente a E coli y P mirabilis, entre otros. De esta forma se podrán generalizar las recomendaciones, aunque en este momento el uso de probióticos ya forma parte de las estrategias preventivas en mujeres que sufren ITU de repetición”.
L. Rhamnosus Lcr35 -quizás uno de los lactobacilos más estudiados- ha demostrado “su eficacia en problemas ginecológicos comunes, como la Vaginosis Bacteriana (VB) o la Vulvovaginitis por Cándida (VVC). Su efecto antibacteriano, frente a Gadnerella vaginalis, o Prevotella bivia (ambos implicados en la VB), y antifúngico, frente a C albicans, es bien conocido en cultivos in vitro”, subraya la Dra. Jurado. También está contrastada su eficacia con respecto a antibióticos o antifúngicos solos, y en estudios controlados con placebo, en la restauración del pH y la microbiota vaginal, la mejora de las tasas de curación y la disminución de las recidivas[20,21].
Conclusiones
El uso regular de los probióticos tienen un efecto positivo en los casos de desequilibrios en la flora vaginal, en vaginosis bacteriana, en vulvovaginitis candidiásica y en sequedad vaginal.

Fuente: Archivo
Entre los probióticos destaca una fórmula única con Lactobacillus rhamnosus Lcr35®, que además lleva vitamina A. Lactoflora protector íntimo contribuye al mantenimiento de las mucosas en condiciones normales y contribuye al funcionamiento normal del sistema inmunitario en la mucosa de la vagina, al tiempo que restablece y mantienen el bienestar íntimo de la mujer.
Para ese mantenimiento del bienestar íntimo, se recomienda una cápsula al día vía oral durante 20 días. En fase aguda, es decir, en casos de desequilibrio, infección o deficiencia de vitamina A, dos cápsulas al día vía oral durante los primeros 10 días. Y posteriormente, tomar una cápsula al día durante 2 ó 3 meses.
El inicio del tratamiento puede ser en cualquier momento del ciclo menstrual.
Por otro lado, en el ámbito de las infecciones, “lo más importante, sostiene la Dra. Jurado, es usar probióticos que contengan cepas que hayan demostrado su eficacia frente a los patógenos de las infecciones urinarias y que estén debidamente testados y autorizados para su comercialización y venta en farmacias. El uso de las cepas probióticas como L. rhamnosus GR-1, L. reutieri RC-14 y L. crispatus (CTV-05) han demostrado efectividad en el control de las infecciones recurrentes”.
Se han llevado a cabo estudios científicos relevantes que demuestran que los productos que contienen determinadas cepas como Lactobacillus rhamnosus Lcr 35®, no solo “mejoran las tasas de curación de los medicamentos habituales, sino que disminuye el número de recidivas y aumenta el tiempo en que la mujer permanece con un pH y una microbiota adecuada tras haber sido tratada. También se ha evidenciado que el uso de esos probióticos es capaz de mantener unas condiciones vaginales más apropiadas para que no se produzca la disbacteriosis”.
“La asociación de probióticos -sostiene la experta- disminuirá las molestas recidivas de las vaginosis bacterianas y permitirá a la mujer pasar más tiempo libre de síntomas. Se aconseja en estos casos administrar el probiótico de 2 a 3 días después del tratamiento antibiótico específico, durante varios días, un mínimo de 5 días y un máximo de 20, según la vía que se utilice, y se repetirá la suplementación durante los mismos días al mes, hasta varios meses post-tratamiento”.
* Lactobacillus plantarum CECT8675 y Lactobacillus plantarum CECT8677 depositadas por AB-Biotics, S.A. en la Colección Española de Cultivos Tipo bajo Tratado de Budapest.
Bibliografía
1. Palou J, Millán F, Brenes F J, Costa J. Cistitis no complicada en la mujer. Guía de práctica clínica. Asociación Española de Urología: Actualización 2013
2. Brenes FJ. Cistitis recurrentes en la mujer. 7DM 2014; nº 856: 16-18
3. Horcajada JP. Conducta y tratamiento de la cistitis (Atención Urgente)JANO 13-19 DE ABRIL 2007. N.º 1.64 31-33
4. McIsaac WJ, Moineddin R, Ross S, Validation of a decision aid to assist physicians in reducing unnecessary antibiotic drug use for acute cystitis, Arch Intern Med. 2007; 167: 2201–2206.
5. Pigrau C. Infecciones urinarias recurrentes: Factores predisponentes y estrategias de prevención. En Pigrau C. Infección del tracto urinario. Ed Ergin; 2013: 85-104
6. Grabe M, et al. Guidelines on Urological Infections. European Association of Urology .2014
7. Kodner C M,Thomas Gupton EK. Recurrent Urinary Tract Infections in Women: Diagnosis and Management. Am Fam Physician. 2010 Sep 15;82(6):638-643
8. Palou J, Pigrau C, Molina I, Ledesma JM, Angulo J. Grupo colaborador español del estudio ARESC. Etiología y sensibilidad de los uropatógenos identificados en infecciones urinarias bajas no complicadas de la mujer en España (estudio ARESC) implicaciones en la terapia empírica Med Clin (Barc). 2011;136:1–7
9. Andreu A. Patogenia de las infecciones urinarias. En: C. Pigrau. Infección del tracto urinario. Ed Ergon 2013:85-104. ISBN:976-84-15351-63-4.
10. Brenes FJ. Generalidades de las ITUs. En Brenes FJ. Manual de evaluación diagnóstica y terapéutica de las infecciones del tracto urinario (ITUs). Abordaje desde la Atención Primaria. IMC. 2003; 12-20
11. Andreu A. Patogenia de las infecciones del tracto urinario. Enferm Infecc Microbiol Clin.2005;23(4).15-21
12. Kodner C M,Thomas Gupton EK. Recurrent Urinary Tract Infections in Women: Diagnosis and Management. Am Fam Physician. 2010 Sep 15;82(6):638-643
13. Scholes D, Hooton TM, Roberts PL, Stapleton AE, Gupta K, Stamm WE. Risk factors for recurrent urinary tract infection in young women. J Infect Dis. 2000;182(4):1177–1182
14. Cancelo MJ. GP Diagnóstico y Tratamiento de Infecciones vulvovaginales. SEGO. Actualizado 2018.
15. Jiménez-Pacheco Antonio, Jiménez-Pacheco Araceli. El uso de probióticos como alternativa en la prevención de las infecciones urinarias recurrentes en mujeres .Rev Med Chile 2013; 141: 809-810
16. Santas, J.; Cuñé, J; Lázaro, J "Probiotic strains for uninary tract infections" (EP15382051).
17. Suárez E, Beltrán DA, Daza M, González SP, Guerra JA, Jurado AR, Ojeda D, Rodríguez JM. La microbiota vaginal: composición y efectos beneficiosos. Consenso sobre usos de los probióticos en Ginecología. Disponible en: http://www.sepyp.es/probiot_vaginales.pdf
18. Stapleton, AE, au-Yeung M, Hooton TM, Fredricks DN, Roberts PL, Czaja CA, Yarova-Yarovaya Y, Fiedler T, Cox m, Stamm WE. Randomized, placebo-controlled phase 2 trial of Lactobacillus crispatus probiotic given intravaginally for prevention of recurent urinary tract infection. Clin Infect Dis. 2011 May;52(10):1212-7.
19. Grin PM, Kowalewska PM, Alhazzan W, Fox-Robichaud AE. Lactobacillus for preventing recurrent urinary tract infections in women: meta-analysis. Canadian Journal of Urology 2013; 20(1): 6607-6614
20. Bertuccini L, Russo R, Iosi F, Superti F. Effects of Lactobacillus rhamnosus and Lactobacillus acodophilus on bacterial vaginal pathogens. Int J Inmunopathol Pharmacol .2017 Jun;30(2):163-167.
21. Rossi A, Rossi T, Bertini M, Caccia G. The use of lactobacillus rhamnosus int the therapy of bacterial vaginosis. Evaluation of clinical efficacy in a population of 40 women treated for 24 months. Arch Gynecol Obstet. 2010 Jun;281(6):1065-9





