El cáncer de próstata es el tercero en incidencia en España si se tienen en cuenta ambos sexos. Entre los hombres, se sitúa en primer lugar en incidencia y en tercer lugar en mortalidad. En 2018 se estimaron 31.728 nuevos casos diagnosticados, con 139 casos por cada 100.000 hombres1.
Existen tres factores de riesgo importantes para padecer esta enfermedad, como son la edad, tener familiares de primer grado con cáncer de próstata y ser de raza negra. Obviamente, ninguno de estos tres factores son controlables. Sin embargo, se ha visto cierta relación de riesgo de padecer esta afección con ciertos hábitos que sí son controlables: la obesidad, especialmente la asociada a alto consumo de carne roja, el sedentarismo y el tabaquismo. Este último parece tener relación con la agresividad del cáncer2,3.

Dr. Álvaro Juárez Soto
Fuente: AEU / RG comunicación
El sistema Gleason sigue siendo uno de los predictores pronósticos más potentes
A pesar de los cambios significativos en el diagnóstico clínico e histológico del tumor prostático maligno, el sistema de clasificación de Gleason sigue siendo uno de los predictores pronósticos más potentes del cáncer de próstata4. La puntuación de Gleason se basa en la medida en la que el cáncer se asemeja a tejido sano cuando se visualiza bajo un microscopio. Los tumores menos agresivos, por lo general, tienen un aspecto más semejante al del tejido sano. Los tumores que son más agresivos tienen probabilidades de crecer y diseminarse a otras partes del cuerpo. Tienen un aspecto menos semejante al tejido sano5.
Las puntuaciones de Gleason de 5 o menos no se usan. La puntuación de Gleason más baja es 6, que es un cáncer de grado bajo. Una puntuación de Gleason de 7 es un cáncer de grado medio, y una puntuación de 8, 9 o 10 es un cáncer de grado alto5.
La prevalencia del cáncer de próstata de alta puntuación de Gleason es significativamente menor que el de baja puntuación de Gleason o puntuación intermedia.
El screening con PSA tiene un impacto en la mortalidad de la enfermedad
La posibilidad de que el cáncer de próstata de alto grado pueda encontrarse muy confinado dentro de la glándula prostática, ser localmente avanzado, o bien ser ya metastásico depende básicamente del desarrollo sanitario de cada país y de la universalización de programas de screening con el Antígeno Prostático Específico o PSA (determinación de PSA a varones mayores de 40 años si tienen antecedentes familiares de cáncer de próstata, y a mayores de 50 años si no lo tienen).
En países con poco nivel de desarrollo sanitario, los pacientes con cánceres de alto grado acuden ya en la fase localmente avanzada o metastásica. En los países más desarrollados, se identifican en fase localizada. En mi opinión, aunque pueda haber controversias, el screening de cáncer de próstata con PSA tiene un impacto en la mortalidad de la enfermedad, es decir, si se realiza como prueba rutinaria de cribado la mortalidad tiende a bajar.
La RM multiparamétrica, una herramienta diagnóstica de gran ayuda
Recientemente se ha incorporado al diagnóstico del tumor prostático un nuevo procedimiento conocido como resonancia magnética (RM) multiparamétrica de la próstata. Básicamente, esta prueba de imagen permite identificar lesiones sospechosas de cáncer en la próstata para, a partir de aquí, poder dirigir la biopsia a dicha lesión. Esto, que parece una obviedad -y es lo que se hace en el resto de los órganos-, no ocurría en el caso de la glándula prostática. Hasta hace poco (y aún hay sitios donde sigue ocurriendo) la próstata se biopsiaba a ciegas.
La RM multiparamétrica es una herramienta de gran ayuda tanto en el seguimiento de pacientes en vigilancia activa como en el diagnóstico de nuevos cánceres. La RM multiparamétrica permite correlacionar el tipo de lesión que se visualiza en la próstata con el Gleason de la misma tras la biopsia.
Tratar el tumor primario con cirugía o radioterapia, independientemente del Gleason
Los pacientes con un cáncer de próstata de alto riesgo -Gleason >8, PSA> 20 ng/ml y estadio clínico>T2c (el tumor ha crecido a ambos lados de la próstata)- considerados dentro de esta categoría, presentan una alta probabilidad de fracaso terapéutico y una peor supervivencia6. En estos escenarios procede aplicar, como tratamiento de primera línea, la prostatectomía (extirpación de la próstata) y la aplicación de radioterapia, en tanto que tratar el tumor primario mediante prostatectomía radical o radioterapia es clave desde un punto de vista estratégico. En un estudio7 presentado por un grupo de investigadores españoles en ASCO genitourinario, en concreto en Chicago 2019, se objetivó que aquellos pacientes diagnosticados de cáncer de próstata que fueron tratados con cirugía o radioterapia, independientemente del Gleason, tardaban significativamente más tiempo en progresar a las etapas finales de la enfermedad, en comparación con aquellos a los que sólo se les había tratado con Terapia de Privación Androgénica (TDA).
Material quirúrgico
Autor/a de la imagen: E. Arandes / www.farmacosalud.com
Fuente: Gentileza del Hospital Sagrat Cor de Barcelona (ARCHIVO)
El tratamiento hormonal o supresión androgénica trata de reducir al máximo los niveles de testosterona (andrógeno más importante) en el organismo. Así, el conocido como bloqueo androgénico o TDA permite inducir apoptosis (‘suicidio de las células tumorales’) en ciertas células susceptibles del cáncer de próstata, al reducir la síntesis de andrógenos y su interacción con el receptor androgénico8.
El bloqueo androgénico es la piedra angular en el tratamiento del tumor prostático metastásico. También se emplea de forma coadyuvante en las terapias con intento curativo como la radioterapia externa y braquiterapia (radiación interna mediante colocación de un implante radiactivo) en la enfermedad localizada de alto riesgo y localmente avanzada8. Con todo, si bien es cierto que el bloqueo androgénico o TDA es el eje sobre el que gira el tratamiento del cáncer de próstata avanzado, cada vez se dispone de más evidencia del valor del tratamiento quirúrgico o radioterápico del tumor primario retrasando la TDA.
De entre los ensayos clínicos que actualmente se están realizando en pacientes diagnosticados de cáncer de próstata de alto riesgo destaca PROTEUS9. En este trabajo se combina TDA con cirugía, pero en este caso, la TDA por un periodo limitado de tiempo de 1 año. La gran relevancia que podría tener PROTEUS en el abordaje de esta enfermedad me llevará a incidir de nuevo en este estudio más adelante.
El cáncer de próstata no responde muy bien a los tratamientos inmunoterápicos
La crioterapia, una opción alternativa para el tratamiento del cáncer de próstata, incluye la congelación total de la próstata (tratamiento total de la glándula) o sólo del cáncer (tratamiento focal)10. De todos modos, cabe especificar que, en la actualidad, las terapias focales no son una alternativa para el cáncer de próstata de alto riesgo o alto grado.
La quimioterapia únicamente es una opción para aquellos cánceres de próstata de alto grado que, en el momento de su diagnóstico, ya presentan una alta carga de metástasis. Cuando la enfermedad está localizada en la próstata, la quimioterapia no es alternativa. El eje sobre el que gira el tratamiento del cáncer de próstata avanzado es el receptor androgénico.
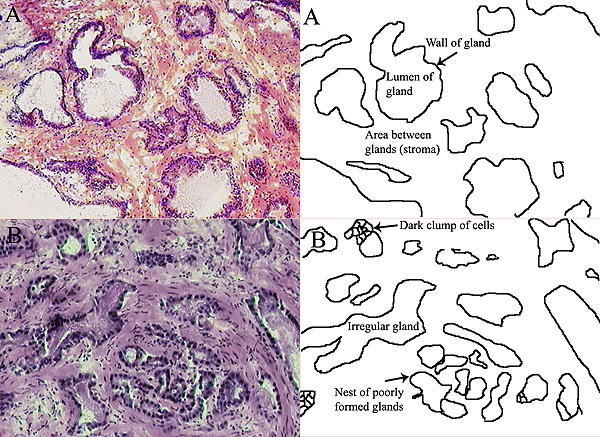
Próstata normal (A) y próstata con cáncer (B). En el cáncer de próstata, las glándulas normales de la próstata son sustituidas per masas de células irregulares, como se ve en estas imágenes tomadas al microscopio
Autor/a de la imagen: Created by me based on photomicrographs from US government site http://cgap-mf.nih.gov/ProstateExample/ProstateMAandResults/Histology/Pr10.html http://cgap-mf.nih.gov/ProstateExample/ProstateMAandResults/Histology/Pr2.html All changes released into public domain
Fuente: Viquipèdia /Wikipedia
La inmunoterapia, a diferencia de los demás tratamientos disponibles, no se dirige a destruir las células del tumor sino que su acción es estimular el sistema inmunitario del enfermo para que sea el propio sistema inmunitario el que ataque y destruya el tumor11. En general, el cáncer de próstata no es un tumor muy inmunogénico, es decir, no responde muy bien a los tratamientos inmunoterápicos. Cuando se habla de tumor prostático, puede decirse que las mejores respuestas con tratamientos inmunoterápicos aislados se han observado en pacientes con baja carga tumoral, lo cual puede sugerir que su aplicación óptima podría establecerse en fases más precoces de la enfermedad12. Los resultados obtenidos sugieren que la inmunoterapia puede ser más efectiva en modo tratamiento combinado con otros tratamientos activos (abiraterona, enzalutamida, Radio 223, docetaxel) en la lucha por lograr cronificar la enfermedad12.
En la actualidad, el único tratamiento inmunoterápico aprobado para el abordaje del cáncer de próstata en sus fases avanzadas es SPILUCEL T, que no está aprobado por las autoridades europeas, sino únicamente por las americanas.
El ensayo clínico PROTEUS puede cambiar la práctica clínica diaria
Los resultados del ensayo clínico PROTEUS9 -al que me referí antes- pueden cambiar la práctica clínica diaria en el ámbito del cáncer de próstata de alto riesgo localizado. Este ensayo combina cirugía con un año de un antiandrógeno de última generación denominado apalutamida. El objetivo principal de este ensayo es determinar si la combinación de cirugía más apalutamida limitada a un año tiene un impacto en la progresión de la enfermedad a etapa metastásica.
Entrando de lleno ya en la enfermedad metastásica, los recientes resultados de los ensayos clínicos TITAN13, LATITUDE14, ENZAMET15 y ARCHES16 han cambiado nuestra práctica clínica en el sentido de que ya no todo es Terapia de Privación Androgénica para el cáncer de próstata metastásico, sino que hay nuevos tratamientos, como abiraterona, apalutamida y enzalutamida, con impacto en la supervivencia global de estos pacientes.

Fuente: www.farmacosalud.com / Archivo
Gentileza del Centro Nacional de Microbiología. Instituto de Salud Carlos III de Madrid
En el escenario de la etapa más avanzada de la enfermedad, la resistencia a la castración, la investigación de tratamientos dirigidos exclusivamente a tumores que expresan ciertos marcadores moleculares, como el fármaco niraparib, supondrá dar los primeros pasos para poder desarrollar una medicina personalizada en cáncer de próstata.
Es importante que los enfermos sepan que, en los últimos años, el tratamiento del cáncer de próstata ha cambiado y que ahora disponemos de tratamientos que hace unos pocos años no teníamos. Los Servicios de Urología Españoles se han adaptado a este cambio adoptando todo el nuevo conocimiento existente y adecuando la estructura organizativa de los Servicios para dar la mejor atención uro-oncológica a los pacientes.
Conclusiones
El desarrollo sanitario de cada país y el nivel de implantación de programas de screening con el Antígeno Prostático Específico (PSA) son factores que influyen a la hora de poder encontrar un cáncer de próstata de alto grado muy confinado dentro de la glándula prostática, o bien en una fase localmente avanzada, e incluso ya en un estadío metastásico.
La reciente incorporación de la resonancia magnética multiparamétrica como procedimiento diagnóstico en cáncer de próstata ha sido de gran ayuda tanto en el seguimiento de pacientes en vigilancia activa como en la detección de nuevos cánceres. Esta herramienta identifica lesiones sospechosas y permite dirigir la biopsia a dicha lesión, lo que evita tener que biopsiar la glándula prostática a ciegas.
Entre los ensayos clínicos que hay en marcha, destaca PROTEUS, cuyos resultados podrían cambiar la práctica clínica diaria. El estudio pretende determinar si la cirugía, combinada con apalutamida limitada a un año, tiene un impacto en la progresión del cáncer de próstata de alto grado a etapa metastásica. Asimismo, los ensayos TITAN, LATITUDE, ENZAMET y ARCHES han demostrado que, además de la Terapia de Privación Androgénica, hay otros tratamientos, como abiraterona, apalutamida y enzalutamida, que tienen un impacto en la supervivencia global de los pacientes con tumor prostático en fase metastásica. En paralelo, tratamientos como niraparib podrían ser el germen de una medicina personalizada para las etapas más avanzadas de la enfermedad.
Referencias
1. Asociación Española Contra el Cáncer (AECC). Todo sobre el cáncer. Cáncer de próstata. Incidencia del cáncer de próstata. 2018. https://www.aecc.es/es/todo-sobre-cancer/tipos-cancer/cancer-prostata/pronostico
2. Allott EH, Masko EM, Freedland SJ. Obesity and Prostate Cancer: Weighing the Evidence. Eur Urol. 2013;63(5):800–9
3. Perez-Cornago A, Appleby PN, Pischon T, Tsilidis KK, Tjønneland A, Olsen A, et al. Tall height and obesity are associated with an increased risk of aggressive prostate cancer: results from the EPIC cohort study. BMC Med [Internet]. 2017 [cited 2017 Dec 1];15(1). http://bmcmedicine.biomedcentral.com/articles/10.1186/s12916-017-0876-
4. Gordetsky J, Epstein J. Grading of prostatic adenocarcinoma: current state and prognostic implications. Diagn Pathol. 2016 Mar 9;11:25.
5. Junta Editorial de Cancer.Net (American Society of Clinical Oncology, ASCO). Cáncer de próstata: Estadios y Grados. 2018. https://www.cancer.net/es/tipos-de-c%C3%A1ncer/c%C3%A1ncer-de-pr%C3%B3stata/estadios-y-grados
6. Rioja Zuazu J, Zudaire Berbera J.J, Rincón Mayans A, Rosell Costa D, Robles Garcia J.E, Berian Polo J.M. Adenocarcinoma de próstata gleason clínico 8-10: influencia pronóstica en la supervivencia libre de progresión bioquímica. Actas Urol Esp 2008. 32(8): 792-798.
7. Juárez-Soto A, Carballido Rodríguez J, Rubio-Briones J, Rodríguez Antolín A, Amores Bermúdez J, Medina González, A. et al. CLINICAL DRIVERS FOR IMAGING TESTING IN NON-METASTATIC CASTRATION-RESISTANT PROSTATE CANCER: MAY THEY BE OPTIMIZED? FINAL ANALYSIS OF “IDENTIFICA” STUDY. Poster presented at ASCO-GU. 2019, California, USA
8. Arroyo-Kuribreña JC, Soto-Vega E, Muñoz-Pérez M, Contreras JM, Varela-Cabrera JA. Bloqueo androgénico en cáncer de próstata, revisión de la literatura. Rev Mex Urol 2012;72(4):182-196.
9. Taplin ME, Gleave M, Evans CP, Efstathiou E, Kantoff PW, Ross A, Shore ND, et al. PROTEUS: A randomized, double-blind, placebo (PBO)-controlled, phase 3 trial of apalutamide (APA) plus androgen deprivation therapy (ADT) versus PBO plus ADT prior to radical prostatectomy (RP) in patients with localized high-risk or locally advanced prostate cancer (PC). Journal of Clinical Oncology. 2019. 37, no 15_suppl.
10. Jung JH, Risk MC, Goldfarb R, Reddy B, Coles B, Dahm P. Primary cryotherapy for localised or locally advanced prostate cancer. Cochrane Database of Systematic Reviews 2018, Issue 5. Art. No.: CD005010.
11. Sociedad Española de Oncología Médica (SEOM). La inmunoterapia del cáncer. 2019. https://seom.org/guia-actualizada-de-tratamientos/la-inmunoterapia-del-cancer
12. Miñana López B, Villacampa Aubá F, De Fata Chillón FR, Ancizu Markert FJ, García Cortés A, Doménech López P, et al. Inmunoterapia en cáncer de próstata resistente a la castración. Archiv Esp Urol. 2018. ISSN 0004-0614. 71(8): 685-695.
13. Agarwal N, McQuarrie K, Bjartell A, Chowdhury S, Pereira de Santana Gomes AJ, Chung BH, et al. Health-related quality of life after apalutamide treatment in patients with metastatic castration-sensitive prostate cancer (TITAN): a randomised, placebo-controlled, phase 3 study. Lancet Oncol. 2019; 20(11):1518-1530.
14. Fizazi K, Tran N, Fein L, Matsubara N, Rodriguez-Antolin A, Alekseev BY, et al for the LATITUDE Investigators. Abiraterone plus Prednisone in Metastatic, Castration-Sensitive Prostate Cancer. N Engl J Med 2017; 377:352-360.
15. Davis ID, Martin AJ, Stockler MR, Begbie S, Chi KN, Chowdhury S, et al for the ENZAMET Trial Investigators. Enzalutamide with Standard First-Line Therapy in Metastatic Prostate Cancer. N Engl J Med 2019; 381:121-131
16. Armstrong AJ, Szmulewitz RZ, Petrylak DP, Holzbeierlein J, Villers A, Azad A, et al. ARCHES: A Randomized, Phase III Study of Androgen Deprivation Therapy With Enzalutamide or Placebo in Men With Metastatic Hormone-Sensitive Prostate Cancer. J Clin Oncol. 2019; 37(32):2974-2986.




