Marcos López
El asma es un síndrome inflamatorio de la vía aérea que requiere un abordaje multidisciplinar y cuyo tratamiento se ha visto notablemente optimizado con la aparición de los fármacos biológicos. Así, y con el objetivo de analizar los últimos avances en el abordaje del asma, se celebró el pasado 8 de noviembre en Palma, en el marco del LXIII Congreso Nacional de la Sociedad Española de Farmacia Hospitalaria (SEFH) y con el apoyo de GSK, el simposio ‘Abordaje de los fármacos biológicos en el tratamiento del asma grave’.
Asma grave
A día de hoy conviven en todo el mundo en torno a 360 millones de personas con asma. Una enfermedad que, en el caso específico de nuestro país, afecta al 5-6% de los adultos y a hasta un 10% de la población infantil y adolescente. Además, en torno a un 4% de los casos padecen asma grave, cuya falta de control, tal y como indica el Dr. Álvaro Moreno-Ancillo, médico especialista en Alergología del Hospital General Nuestra Señora del Prado de Talavera de la Reina (Toledo), “tiene que ver con las exacerbaciones graves, el uso de corticosteroides, la hospitalización y la pérdida de la función pulmonar y del flujo aéreo a lo largo de la vida. El resultado es que aún en la actualidad hablamos de mortalidad en asma, sobre todo en mujeres mayores de 50-60 años y, en algunos casos, en población joven”.

Fuente: www.farmacosalud.com
El asma es en realidad un síndrome inflamatorio de la vía aérea, por lo que no puede aludirse a que todos los afectados, caso de los niños y las mujeres añosas, padecen la misma enfermedad. De hecho, la tendencia en los últimos 20-30 años ha sido agrupar a los pacientes en función de ciertas características comunes –adultos, adolescentes, obesos, etc.– y tratar las exacerbaciones con incrementos de dosis de corticosteroides inhalados (CI) u orales. Sin embargo, “hoy en día –indica el Dr. Moreno-Ancillo– ya no podemos administrar el mismo tratamiento para todos, sobre todo en el asma grave. Hay que seleccionar a los pacientes que sean tratables en función de una diana terapéutica”.
Concretamente, el estudio de Bruselle y cols[1] identifica tres fenotipos de asma grave: asma alérgica eosinofílica, asma no alérgica eosinofílica, y asma neutrofílica. Unos fenotipos a los que se aúna el asma por obesidad y que, caracterizados por una sintomatología y biomarcadores específicos, requerirán un tratamiento diferenciado[2]. Así, en el asma alérgica eosinofílica, la célula presentadora de antígeno (APC) presenta el alérgeno al linfocito T naïve e induce su conversión en linfocito Th2, responsable de la amplificación del sistema inmunológico. El resultado es la liberación de interleucinas –entre otras, la IL-13, responsable de incrementar el remodelado del epitelio de la vía aérea y generar células mucosas; y la IL-5, responsable del reclutamiento de eosinófilos– que, sin embargo, son comunes al asma no alérgica eosinofílica.
Tratamiento

Dr. Álvaro Moreno-Ancillo
Fuente: www.farmacosalud.com
Por tanto, el bloqueo de los distintos mediadores, caso de la IL-5 y la IL-13, posibilitará el tratamiento del asma eosinofílica –alérgica y no alérgica o tardía–. En este contexto, refiere el Dr. Moreno-Ancillo, “si intentamos actuar sobre el fenómeno final, que tiene que ver con el remodelado, una diana principal debería ser la IL-5, pues potencia, atrae y favorece la maduración de los eosinófilos. Para ello contamos con mepolizumab y reslizumab, fármacos ambos con efecto antieosinófilo (anti IL5). Por su parte, benralizumab señala a los eosinófilos a través del receptor de la IL-5 para favorecer su destrucción por las células NK; dupilumab, actualmente indicado en la dermatitis atópica, bloquea la señal de IL-4 –interleucina que potencia la producción de inmunoglobulina E (IgE) a través de la transformación de linfocitos B productores de IgE e IL-13 en distintos tipos de células; tezepelumab bloquea la linfopoyetina estromal tímica (TSLP), y omalizumab actúa inhibiendo la IgE.
En palabras del Dr. Moreno-Ancillo, “los estudios[3] han demostrado la eficacia de todos estos fármacos a la hora de reducir las exacerbaciones y mejorar la función pulmonar. Además, en Estados Unidos se ha aprobado el uso de mepolizumab para el asma infantil*”. Sea como fuere, la elección del medicamento deberá establecerse en función de la experiencia real con el uso de cada uno de los fármacos[3] y de otros aspectos diferentes de la mera eficacia clínica –caso de la posología–. Asimismo, y en los pacientes con solapamiento, deberá valorarse la situación en función de que predomine la IgE o el factor eosinofílico[4]. A este respecto, “como clínicos no debemos valorar solo las cifras –apunta el Dr. Moreno-Ancillo–, sino pacientes. Debemos conocer la historia vital del paciente para seleccionar el fármaco biológico. La decisión clínica dependerá de un examen exhaustivo que nos llevará a una medicina de precisión. El problema es que aún no tenemos datos de biomarcador que nos ayuden más que la historia clínica a la hora de seleccionar el tratamiento”.
* La indicación pediátrica ha sido aprobada en Europa. En España está pendiente de decisión de precio y financiación.
En consecuencia, y en caso de alergia ‘pura’ en el asma grave, deberá emplearse un anti-IgE; si la alergia no resulta relevante, deberá indicarse un fármaco anti-IL5 –caso de mepolizumab–, y en caso de que el componente alérgico sea difuso, como sucede en los pacientes mayores de 45 años, puede alternarse entre un anti-IgE y un anti-IL5 en función de las características del enfermo, pudiendo en un futuro recurrirse a un fármaco anticitocinas T2 –dupilumab, tezepelumab– en caso de fracaso terapéutico.
Anticuerpos monoclonales
El asma es una patología cuya primera descripción, recogida en el papiro de Ebers, data del año 1.500 a. J.C. Sin embargo, como recuerda el Dr. Iñigo Ojanguren Arranz, médico especialista en Neumología del Hospital Universitari Vall d’Hebron de Barcelona, “hubo que esperar hasta la década de los años 80 del pasado siglo XX para que llegasen los CI y experimentáramos un antes y un después en el control de los síntomas y la reducción de las exacerbaciones y la mortalidad por crisis asmáticas”. Una evolución grave cuyo último hito ha venido establecido por el desarrollo, ya en el siglo XXI, de los anticuerpos monoclonales.

Dr. Iñigo Ojanguren Arranz
Fuente: www.farmacosalud.com
El objetivo actual del tratamiento del asma grave viene definido por la denominada ‘medicina P4’ –Preventiva, Personalizada, Participativa, y de Precisión[5]–. Así, y para llevar a cabo la medicina de precisión, los especialistas deben llevar a cabo una identificación de los rasgos tratables pulmonares a partir de la historia clínica y la evaluación, entre otros parámetros, de la función pulmonar, el óxido nítrico exhalado (FeNO) y la eosinofilia en sangre periférica[5].
De acuerdo con lo establecido en los escalones terapéuticos de la Guía española para el manejo del asma (GEMA)[6], la piedra angular del tratamiento de mantenimiento del asma es el CI. Como apunta el Dr. Ojanguren, “de resultar necesario, las dosis de CI se aumentarán progresivamente y se añadirán otros fármacos como los broncodilatadores de acción larga o los anticolinérgicos para lograr el control de la enfermedad. Además, en los escalones 5 y 6 contamos con los anticuerpos monoclonales, encontrándose disponibles hoy en día para su prescripción en la práctica clínica omalizumab, mepolizumab y reslizumab”.
Omalizumab, fármaco que actúa a nivel de la IgE, constituye el anticuerpo monoclonal con el que se ha alcanzado una mayor experiencia clínica en el abordaje del asma grave. Un fármaco, asimismo, cuya eficacia ha sido demostrada en distintos estudios[7]. Además, como sugiere el estudio de Ollé-Monge y cols[8], es probable que el papel de omalizumab no se limite al bloqueo de la IgE, pudiendo también actuar sobre otros niveles de la inflamación en el asma, caso de la estabilización de la membrana del mastocito.
Un momento de la sesión
Fuente: www.farmacosalud.com
Mepolizumab
Mepolizumab es un inhibidor específico de la IL-5 cuya eficacia en el tratamiento del asma grave ha sido confirmada por numerosos estudios. El trabajo de Ortega y cols[9], ensayo clínico aleatorizado doble ciego diseñado para evaluar la eficacia de mepolizumab en la prevención de exacerbaciones en 576 pacientes con asma grave eosinofílica, mostró que, concluidas las 32 semanas de tratamiento, los pacientes que recibieron el anticuerpo monoclonal experimentaron la mitad de exacerbaciones que los tratados con placebo. Es más, la terapia con mepolizumab también se asoció con una mejora promedio del 8% en el FEV1 con respecto a placebo. En definitiva, como destaca el Dr. Ojanguren, “el estudio concluye que mepolizumab se asocia a una disminución significativa en las exacerbaciones asmáticas y a una mejora de diferentes marcadores relacionados con un mejor control del asma”.
En este contexto, la experiencia alcanzada con los 10 primeros pacientes tratados con mepolizumab en el Hospital Universitari Vall d’Hebron constata la eficacia de este anticuerpo monoclonal en el abordaje del asma grave. Los pacientes, ocho mujeres y dos varones, presentaban una edad entre los 35 y los 65 años y se encontraban en el sexto escalón terapéutico de la GEMA[6]. Todos los pacientes habían padecido entre 1 y 10 exacerbaciones en los 12 meses previos y presentaban un FEV1 deteriorado, unos niveles superiores a 400-500 eosinófilos por μL en sangre periférica, y un test ACT inferior a 20. Administrado el tratamiento con mepolizumab, y tras 6-12 meses de seguimiento, la mayoría de pacientes no padeció ninguna exacerbación, registrándose algún caso con una única exacerbación; el FEV1 mejoró en la mitad de los casos; los niveles de eosinófilos se redujeron en todos los pacientes a 0-100 unidades por μL, y el test ACT mejoró en casi todos los casos. En consecuencia, y dados los resultados, se pudo reducir la dosis de corticosteroides orales en la mitad de los pacientes. Como refiere en Dr. Ojanguren, “consideramos que en ocho pacientes hubo una buena respuesta”.
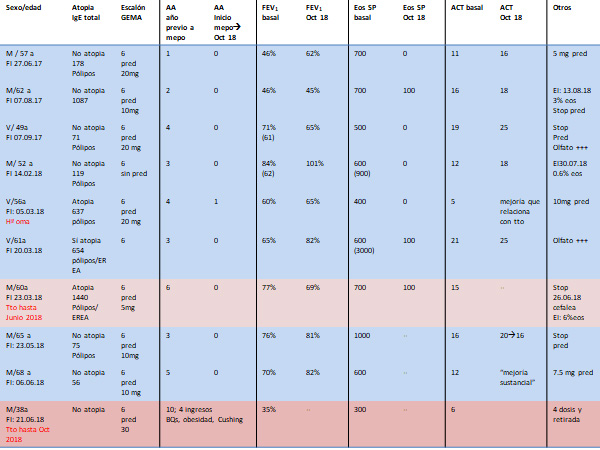
Fuente: Unidad Asma grave. Hospital Univ. Vall d'Hebron. Barcelona
Finalmente, diversos estudios han mostrado la eficacia y seguridad de reslizumab en la prevención de agudizaciones en el asma grave eosinofílica[10]; la eficacia de benralizumab a la hora de reducir la dosis de corticosteroides orales y las exacerbaciones en el asma grave[11], y la eficacia de tezepelumab en el manejo del asma grave no controlada[12,13]. A este respecto, como concluye el Dr. Ojanguren, “de cara a la selección del tratamiento, deben establecerse comités multidisciplinares para la aceptación y elección de fármacos biológicos en asma grave, algo que ya se está haciendo en algunos hospitales terciarios”.
Comités de farmacia
El diagnóstico del tipo de asma es absolutamente esencial de cara al establecimiento del tratamiento. Como resalta el Dr. Carlos Crespo Diz, jefe de Servicio de Farmacia del Área Sanitaria Pontevedra y O Salnés (Pontevedra), “la tipificación clara por el fenotipo de los pacientes es decisiva. En nuestra práctica farmacéutica habitual nos encontramos con pacientes con asma alérgica eosinofílica y con asma no alérgica eosinofílica, para la que contamos con mepolizumab, reslizumab y benralizumab. Sin embargo, no contamos con estudios comparativos entre estos fármacos, lo que dificulta la selección del tratamiento”.

Dr. Carlos Crespo Diz
Fuente: www.farmacosalud.com
Los comités de farmacia terapéutica de cada comunidad autónoma elaboran dictámenes para armonizar los criterios de utilización de un fármaco dentro de su CCAA. Unos dictámenes en los que, además de valorar el componente clínico, se establecen los criterios para un uso racional del medicamento. Sin embargo, tanto los servicios médicos como farmacéuticos de los centros hospitalarios juegan un papel relevante en el seguimiento de los medicamentos. Como indica el Dr. Crespo, “el papel, trascendental, que se otorga a los comités de farmacia para la selección del medicamento no sirve absolutamente para nada en caso de no acompañarse de un buen seguimiento, tratamiento y valoración de resultados”.
Los posicionamientos pueden ser parciales –por ejemplo, indicación– o completos –indicación, condiciones de prescripción y dispensación, duración y seguimiento, y evaluación de resultados–. Pero como apunta el Dr. Crespo, “no hay ningún trabajo publicado sobre evaluación de resultados en asma grave, ni siquiera con omalizumab. Los ensayos clínicos se llevan a cabo con pacientes muy bien seleccionados, pero en la práctica real presentan comorbilidades y han de ser tratados de forma individualizada, por lo que el seguimiento es clave. Y aquí los servicios de farmacia juegan un papel fundamental”.
En este contexto, el dictamen de la Comisión Autonómica Central de Farmacia y Terapéutica del Servicio Gallego de Salud (SERGAS) sobre mepolizumab establece su indicación en el asma eosinofílica refractaria grave en adultos cuyo fenotipo eosinofílico se encuentre adecuadamente caracterizado y especifica que, ‘en pacientes con asma eosinofílica mediada por IgE, candidatos a recibir mepolizumab u omalizumab, la selección tendrá en cuenta criterios de eficiencia’. Así, la selección recaerá en los comités multidisciplinares de centro.
En relación al binomio paciente-medicamento, “no solo las compañías farmacéuticas –concluye el Dr. Crespo– tienen intereses. También la administración sanitaria y los profesionales sanitarios, que buscan hacer un uso racional de los medicamentos y no dejar a pacientes sin tratamiento, siempre buscando la equidad. Pero también las sociedades científicas, ciertamente influyentes, y las asociaciones de pacientes, cada vez con mayor influencia y que en ocasiones ponen en entredicho el uso racional de los fármacos”.

(de izq. a dcha): Drs. Iñigo Ojanguren Arranz, Álvaro Moreno-Ancillo y Carlos Crespo Diz
Fuente: www.farmacosalud.com
Bibliografía
1. Brusselle G, Bracke K. Targeting immune pathways for therapy in asthma and chronic obstructive pulmonary disease. Ann Am Thorac Soc. 2014 Dec; 11 Suppl 5: S322-8. doi: 10.1513/AnnalsATS.201403-118AW.
2. GEMA4.2. Guía española para el manejo del asma. Disponible en: https://www.semfyc.es/wp-content/uploads/2017/05/GEMA_4.2_final.pdf
3. Farne HA, Wilson A, Powell C, Bax L, Milan SJ. Anti-IL5 therapies for asthma. Cochrane Database Syst Rev. 2017 Sep 21; 9: CD010834. doi: 10.1002/14651858.CD010834.pub3.
4. Domingo C. Overlapping Effects of New Monoclonal Antibodies for Severe Asthma. Drugs. 2017 Oct; 77(16): 1769-1787. doi: 10.1007/s40265-017-0810-5.
5. Agusti A, Bel E, Thomas M, Vogelmeier C, Brusselle G, Holgate S, et al. Treatable traits: toward precision medicine of chronic airway diseases. Eur Respir J. 2016 Feb; 47(2): 410-9. doi: 10.1183/13993003.01359-2015.
6. GEMA4.3. Guía española para el manejo del asma. Disponible en: https://www.semg.es/images/documentos/docs_varios/GEMA_43.pdf
7. Vennera Mdel C, Pérez De Llano L, Bardagí S, Ausin P, Sanjuas C, González H, et al. Omalizumab therapy in severe asthma: experience from the Spanish registry--some new approaches. J Asthma. 2012 May; 49(4): 416-22. doi: 10.3109/02770903.2012.668255. Epub 2012 Mar 23.
8. Ollé-Monge M, Cruz MJ, Gomez-Ollés S, Ojanguren I, Vanoirbeek J, Muñoz X. Effect of anti-IgE in occupational asthma caused by exposure to low molecular weight agents. Allergy. 2017 Nov; 72(11): 1720-1727. doi: 10.1111/all.13190. Epub 2017 Jul 20.
9. Ortega HG, Liu MC, Pavord ID, Brusselle GG, FitzGerald JM, Chetta A. Mepolizumab treatment in patients with severe eosinophilic asthma. N Engl J Med. 2014 Sep 25; 371(13): 1198-207. doi: 10.1056/NEJMoa1403290. Epub 2014 Sep 8.
10. Castro M, Zangrilli J, Wechsler ME, Bateman ED, Brusselle GG, Bardin P, et al. Reslizumab for inadequately controlled asthma with elevated blood eosinophil counts: results from two multicentre, parallel, double-blind, randomised, placebo-controlled, phase 3 trials. Lancet Respir Med. 2015 May; 3(5): 355-66. doi: 10.1016/S2213-2600(15)00042-9. Epub 2015 Feb 23.
11. Nair P, Wenzel S, Rabe KF, Bourdin A, Lugogo NL, Kuna P, et al. Oral Glucocorticoid-Sparing Effect of Benralizumab in Severe Asthma. N Engl J Med. 2017 Jun 22; 376(25): 2448-2458. doi: 10.1056/NEJMoa1703501. Epub 2017 May 22.
12. Ojanguren I, Martin JG, Lemiere C. Linfopoyetina del estroma tímico: ¿un objetivo prometedor para el tratamiento del asma? Arch Bronconeumol. 2017 Oct; 53(10): 545-546. doi: 10.1016/j.arbres.2017.05.015. Epub 2017 Jun 20.
13. Corren J, Parnes JR, Wang L, Mo M, Roseti SL, Griffiths JM, et al. Tezepelumab in Adults with Uncontrolled Asthma. N Engl J Med. 2017 Sep 7; 377(10): 936-946. doi: 10.1056/NEJMoa1704064.




