Redacción Farmacosalud.com
En el presente informe se reseñan los medicamentos ya evaluados por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), considerados de mayor interés para el profesional sanitario. Se trata de opiniones técnicas positivas de la AEMPS correspondientes al mes de junio de 2020 que son previas a la autorización y puesta en el mercado del medicamento, lo que sucederá dentro de algunos meses, informa este organismo mediante un comunicado. Una vez los nuevos fármacos se hayan autorizado, toda la información de cada uno de ellos (desde la ficha técnica y prospecto, hasta sus condiciones de prescripción, uso y disponibilidad real en el mercado) se podrá consultar en la web de la AEMPS, dentro de la sección CIMA: Centro de Información Online de Medicamentos de la AEMPS.
Idefirix (IMLIFIDASA)
Indicación aprobada: Idefirix está indicado para el tratamiento de desensibilización de pacientes adultos altamente sensibilizados, que esperan un trasplante renal y que tienen una prueba cruzada positiva frente al riñón disponible de un donante fallecido. El uso de Idefirix debe ser reservado a pacientes que es improbable que puedan recibir el trasplante en el sistema de asignación de riñones disponibles, incluyendo los programas de priorización para pacientes altamente sensibilizados. Idefirix estará disponible como polvo para concentrado para solución para perfusión (11 mg). La sustancia activa de Idefirix es imlifidasa, un inmunosupresor.
Perfusor de medicamentos
Autor/a de la imagen: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com / Gentileza del Hospital Sagrat Cor de Barcelona
Kaftrio (ELEXACAFTOR/ TEZACAFTOR/ IVACAFTOR)
Indicación aprobada: Kaftrio está indicado en un régimen combinado con ivacaftor 150 mg comprimidos para el tratamiento de la fibrosis quística en pacientes de 12 años de edad y mayores, que son homocigotos para la mutación F508del en el gen regulador de la conductancia transmembrana de la fibrosis quística (CFTR, por sus siglas en inglés), o que son heterocigotos para F508del en el gen CFTR con una mutación de función mínima (MF, por sus siglas en inglés). Kaftrio estará disponible como comprimidos recubiertos con película (100 mg elexacaftor/50 mg tezacaftor/75 mg ivacaftor).
Veklury (REMDESIVIR)
Indicación aprobada: Veklury está indicado para el tratamiento de la enfermedad del coronavirus 2019 (COVID-19) en adultos y adolescentes (12 años de edad y mayores con un peso corporal de al menos 40 kg) con neumonía, que requieren oxígeno suplementario. Veklury estará disponible como concentrado para solución para perfusión (100 mg por vial, cada mililitro de concentrado contiene 5 mg de remdesivir). El Comité Europeo de Evaluación de Medicamentos (CHMP) ha recomendado de manera condicional la autorización de comercialización, al satisfacer una necesidad médica no cubierta, en la medida en que el beneficio para la salud pública de su inmediata disponibilidad es superior al riesgo inherente de que todavía se requieran datos adicionales.
Gencebok (CITRATO DE CAFEÍNA)
Indicación aprobada: Gencebok está indicado para el tratamiento de la apnea primaria de los recién nacidos prematuros. Gencebok estará disponible como solución para perfusión (10 mg/ml).
Methylthioninium chloride Cosmo (CLORURO DE METILTIONINIO)
Indicación aprobada: Methylthioninium chloride Cosmo está indicado como un agente de diagnóstico que mejora la visualización de lesiones colorrectales en pacientes adultos que se someten a una colonoscopia de screening o de seguimiento. Methylthioninium chloride Cosmo estará disponible como comprimidos de liberación prolongada (25 mg).

Autor/a de la imagen: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
Biosimilares
Livogiva (TERIPARATIDA)
Indicación aprobada: Livogiva está indicado en adultos para: el tratamiento de la osteoporosis en mujeres posmenopáusicas y en varones con un aumento del riesgo de fractura, y tratamiento de la osteoporosis asociada a terapia sistémica mantenida con glucocorticoides en mujeres y hombres con un incremento del riesgo de fractura. Livogiva estará disponible como solución inyectable (20 microgramos/80 microlitros).
Qutavina (TERIPARATIDA)
Indicación aprobada: Qutavina está indicado en adultos para: tratamiento de la osteoporosis en mujeres posmenopáusicas y en varones con un aumento del riesgo de fractura, y tratamiento de la osteoporosis asociada a terapia sistémica mantenida con glucocorticoides en mujeres y hombres con un incremento del riesgo de fractura. Qutavina estará disponible como solución inyectable (20 microgramos/80 microlitros).
Cambios de especial interés sanitario en medicamentos ya autorizados
Nuevas indicaciones con dictamen positivo para su autorización
Para las indicaciones ya autorizadas se recomienda consultar el texto completo de las mismas en las fichas técnicas disponibles en la web de la AEMPS, dentro de la sección CIMA: Centro de Información Online de Medicamentos de la AEMPS.
Cosentyx (SECUKINUMAB)
Autor/a: TeemaTuotanto (pixabay.com)
Fuente: www.needpix.com (Creative Commons)
Extensión de la indicación (en negrita): Psoriasis en placas. Cosentyx está indicado para el tratamiento de la psoriasis en placas de moderada a grave en adultos candidatos a tratamientos sistémicos. Psoriasis pediátrica en placas. Cosentyx está indicado para el tratamiento de la psoriasis en placas de moderada a grave en niños y adolescentes a partir de los 6 años de edad que son candidatos a tratamientos sistémicos. Artritis psoriásica. Cosentyx, solo o en combinación con metotrexato (MTX), está indicado para el tratamiento de la artritis psoriásica activa en pacientes adultos que han mostrado una respuesta inadecuada a tratamientos previos con fármacos antirreumáticos modificadores de la enfermedad (FAME).
Espondiloartrititis axial (EspAax). Espondilitis anquilosante (EA, espondiloartritis axial radiográfica). Cosentyx está indicado para el tratamiento de la espondilitis anquilosante activa en adultos que no han respondido adecuadamente al tratamiento convencional. Espondiloartritis axial no radiográfica (EspAax-nr). Cosentyx está indicado para el tratamiento de la espondiloartritis axial no radiográfica activa en adultos con signos objetivos de inflamación, como elevación de la proteína C-reactiva y/o Imagen por Resonancia Magnética (IRM), que han tenido una respuesta inadecuada a los antiinflamatorios no esteroideos (AINEs).
Epclusa (SOFOSBUVIR/VELPATASVIR)
Extensión de la indicación (en negrita): Epclusa está indicado para el tratamiento del virus de la hepatitis C (VHC) crónica en pacientes de 6 años de edad y mayores y con un peso corporal de al menos 17 kg.
Remsima (INFLIXIMAB)
Extensión de la indicación (en negrita): Artritis reumatoide. Remsima, en combinación con metotrexato, está indicado en la reducción de los signos y síntomas, así como en la mejoría de la función física en: pacientes adultos con enfermedad activa, cuando la respuesta a los medicamentos antirreumáticos modificadores de la enfermedad (FAME), entre ellos el metotrexato, ha sido inadecuada, y pacientes adultos con enfermedad grave, activa y progresiva no tratados previamente con metotrexato u otros FAME. Enfermedad de Crohn en adultos. Remsima está indicado para: el tratamiento de la enfermedad de Crohn activa, de moderada a grave, en pacientes adultos que no han respondido, a pesar de un curso de tratamiento completo y adecuado con un corticosteroide y/o un inmunosupresor; o que sean intolerantes o presenten contraindicaciones médicas a dichos tratamientos, y el tratamiento de la enfermedad de Crohn activa, fistulizante, en pacientes adultos que no han respondido, a pesar de un curso de tratamiento completo y adecuado con tratamiento convencional (entre ellos antibióticos, drenaje y tratamiento inmunosupresor).
Colitis ulcerosa. Remsima está indicado para el tratamiento de la colitis ulcerosa activa, de moderada a grave, en pacientes adultos que han presentado una respuesta inadecuada al tratamiento convencional, que incluye corticosteroides y 6-mercaptopurina (6-MP) o azatioprina (AZA), o que sean intolerantes o presenten contraindicaciones médicas a dichos tratamientos. Espondilitis anquilosante. Remsima está indicado para el tratamiento de la espondilitis anquilosante activa, grave, en pacientes adultos que hayan respondido de forma inadecuada al tratamiento convencional.
Fuente: Archivo
Artritis psoriásica. Remsima está indicado para el tratamiento de la artritis psoriásica activa y progresiva en pacientes adultos cuando la respuesta al tratamiento previo con FAME no ha sido adecuada. Remsima se debe administrar: en combinación con metotrexato, en monoterapia en pacientes que presenten intolerancia a metotrexato o en los que esté contraindicado metotrexato. Psoriasis. Remsima está indicado en el tratamiento de la psoriasis en placas, de moderada a grave, en pacientes adultos que no han respondido, o que tienen contraindicación, o que son intolerantes a otro tratamiento sistémico, entre ellos ciclosporina, metotrexato o psoraleno-ultravioleta A (PUVA).
Sivextro (TEDIZOLID FOSFATO)
Extensión de la indicación (en negrita): Sivextro está indicado para el tratamiento de infecciones bacterianas agudas de la piel y tejidos blandos (ABSSSI por sus siglas en inglés) en adultos y adolescentes de 12 años de edad y mayores.
Xolair (OMALIZUMAB)
Extensión de la indicación (en negrita): Asma alérgica. Xolair está indicado en adultos, adolescentes y niños (de 6 a <12 años). El tratamiento con Xolair deberá ser considerado únicamente para pacientes con asma mediada de forma convincente por IgE (inmunoglobulina E)). Adultos y adolescentes (a partir de 12 años de edad) Xolair está indicado para mejorar el control del asma cuando se administra como tratamiento adicional en pacientes con asma alérgica grave persistente, que presentan test cutáneo positivo o reactividad in vitro a aeroalergenos perennes y con función pulmonar reducida (FEV1<80%), así como síntomas frecuentes durante el día o despertares por la noche, y que han presentado múltiples exacerbaciones asmáticas graves documentadas, a pesar de utilizar corticosteroides diarios inhalados a dosis altas, más un agonista beta2 inhalado de larga duración. Niños (6 a <12 años de edad). Xolair está indicado para mejorar el control del asma cuando se administra como tratamiento adicional en pacientes con asma alérgica grave persistente, que presentan test cutáneo positivo o reactividad in vitro a aeroalergenos perennes, y síntomas frecuentes durante el día o despertares por la noche y que han presentado múltiples exacerbaciones asmáticas graves documentadas, a pesar de utilizar corticosteroides diarios inhalados a dosis altas, más un agonista beta2 inhalado de larga duración.
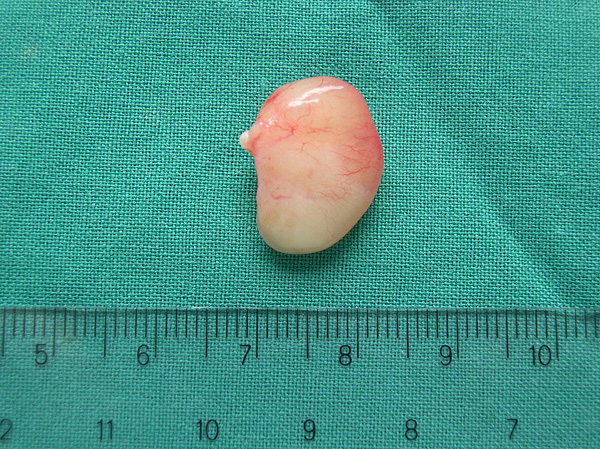
Pólipo nasal extirpado
Autor/a de la imagen: Klaus D. Peter, Wiehl, Germany
Fuente: Wikipedia
Urticaria crónica espontánea (UCE). Xolair está indicado como tratamiento adicional para el tratamiento de la urticaria crónica espontánea en pacientes adultos y adolescentes (a partir de 12 años) con respuesta inadecuada al tratamiento con antihistamínicos H1. Rinosinusitis crónica con pólipos nasales (RSCcPN). Xolair está indicado como tratamiento adicional a los corticoides intranasales para el tratamiento de adultos (a partir de 18 años de edad) con RSCcPN grave, para quienes el tratamiento con corticoides intranasales no proporciona un control adecuado de la enfermedad.
Zavicefta (ZEFTACIDIME/AVIBACTAM)
Extensión de la indicación: Zavicefta está indicado en adultos para el tratamiento de las siguientes infecciones: infección intraabdominal complicada (IIAc), infección complicada del tracto urinario (ITUc), incluyendo pielonefritis, neumonía adquirida en el hospital (NAH), incluyendo neumonía asociada a ventilación mecánica (NAV), y tratamiento de pacientes con bacteriemia que ocurre en asociación con, o se sospecha que está asociada con, cualquiera de las infecciones anteriormente mencionadas. Zavicefta está también indicado para el tratamiento de infecciones por microorganismos aerobios Gram-negativos, en pacientes adultos con opciones terapéuticas limitadas.




