Redacción Farmacosalud.com
La compañía Novartis ha anunciado la publicación en ‘New England Journal of Medicine’ (NEJM) de una serie de resultados detallados de dos ensayos pivotales de Fase III en los que se evaluó la administración del inhibidor de la interleuquina -17A (IL-17A) secukinumab (AIN457). Secukinumab cumplió todos los objetivos primarios y secundarios en la semana 12 en los ensayos ERASURE y FIXTURE, demostrando su superioridad respecto a Enbrel®* (etanercept) en la mejoría de los síntomas de la psoriasis en placas de moderada a grave en el ensayo FIXTURE, y la superioridad respecto al placebo en ambos ensayos, sostiene Novartis mediante un comunicado.
La psoriasis es una enfermedad autoinmune crónica que se caracteriza por la aparición de unas lesiones extensas y gruesas en la piel llamadas placas, que producen prurito, descamación y dolor, y que están asociadas con un importante deterioro de la calidad de vida, tanto en el plano físico, como en el psicológico. Hasta el 50% de los pacientes no se encuentra satisfecho con el tratamiento que reciben actualmente para la psoriasis, incluidas las terapias biológicas autorizadas.
Un anticuerpo monoclonal
Secukinumab (AIN457) es un anticuerpo monoclonal totalmente humano que se une y neutraliza selectivamente la interleuquina-17A (IL-17A)11-13. La IL-17A es una citoquina fundamental (proteína mensajera) involucrada en el desarrollo de la psoriasis, y que se encuentra en altas concentraciones en la piel afectada por la enfermedad. Las investigaciones demuestran que la IL-17A desempeña un papel fundamental en el desarrollo de la respuesta inmunitaria del cuerpo en trastornos como la psoriasis en placas de moderada a grave y es una diana clave en las terapias en investigación. Secukinumab (AIN457) es el primer medicamento dirigido selectivamente a la IL-17A que presenta resultados de Fase III.
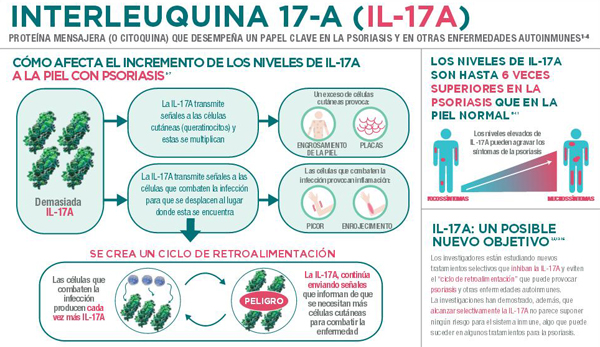
Fuente: Novartis
Más de la mitad de los pacientes que recibieron secukinumab 300 mg experimentaron un blanqueamiento total (PASI 100) o casi total (PASI 90) de la piel, según los parámetros del índice de intensidad y gravedad de la psoriasis (Índice de Área y Gravedad de la Psoriasis, PASI, por sus siglas en inglés) 90 o 100 (PASI 90/PASI 100) en la semana 12 (59,2% en ERASURE y 54,2% en FIXTURE, p<0,001). En comparación, tan solo el 20,7% de los pacientes tratados con Enbrel® obtuvieron un PASI 90 o 100 en el ensayo FIXTURE. La respuesta de los pacientes que recibieron 300 mg de secukinumab continuó mejorando a partir de la semana 12, y más del 70% experimentó una blanqueamiento total o casi total de la piel en la semana 16 (72,4% y 36,8% para PASI 90 y 100, respectivamente) en el ensayo FIXTURE, que se mantuvo en la mayoría de los sujetos hasta la semana 52 (con un tratamiento continuo).
Resolución más rápida de los síntomas
El PASI mide el enrojecimiento, la descamación y el grosor de las placas de psoriasis, así como el alcance de la afectación de cada una de las partes del cuerpo. La eficacia del tratamiento se evalúa mediante la reducción de la puntuación respecto a los niveles basales (esto es, una reducción del 75% se conoce como PASI 75, una reducción del 90% se considera PASI 90, y PASI 100 representa el blanqueamiento total de la piel). PASI 90 y 100 son las medidas más fiables de alcance de blanqueamiento de la piel en comparación con las mediciones estándar, como el PASI 75, que se ha utilizado en la mayoría de los ensayos clínicos.
Los datos publicados en NEJM muestran además que los pacientes que recibieron Secukinumab lograron una resolución más rápida de los síntomas que los tratados con Enbrel® en el ensayo FIXTURE. Ya en la semana 2, se observaron diferencias clínicamente relevantes y, de media, los pacientes que recibieron 300 mg de secukinumab vieron reducidos a la mitad sus síntomas en la semana 3, en comparación con la semana 7 en el caso de los pacientes que recibieron Enbrel®.

Autor: PublicDomainPictures
Fuente: Pixabay / Public Domain
Mejoras en prurito, dolor y descamación
Además de los elevados índices de blanqueamiento total o prácticamente total de la piel, los pacientes que recibieron secukinumab también informaron de mejoras en el prurito, el dolor y la descamación en comparación con el placebo en la semana 12 del ensayo ERASURE. Del mismo modo, la Calidad de Vida Relacionada con la Salud (CdVRS) mejoró de forma significativa entre los pacientes tratados con secukinumab en la semana 12 en comparación con el placebo en ambos ensayos, según los parámetros del Índice de Calidad de Vida Dermatológica (DLQI). El efecto de la psoriasis sobre la calidad de vida ha demostrado ser similar al de enfermedades como el cáncer, las patologías cardiacas, la artritis, la diabetes de tipo 2 y la depresión.
Tanto en ERASURE como en FIXTURE, Secukinumab mostró un perfil de seguridad aceptable que se correspondió con los resultados de los ensayos de Fase II1. En ambos estudios, la incidencia de acontecimientos adversos (AA) fue similar en los dos grupos de tratamiento con secukinumab (300 mg y 150 mg), y fue algo más elevada que en el grupo de placebo durante el periodo de introducción de 12 semanas, tratándose en la mayoría de los casos de infecciones respiratorias de leves a moderadas de las vías altas. La incidencia de AA en los grupos de secukinumab durante el periodo de inducción y el periodo de tratamiento completo de 52 semanas de FIXTURE fue comparable a la de Enbrel®.




