Guillermo González Castilla
La psoriasis es una enfermedad cutánea de elevada prevalencia que, en la mayoría de los casos, evoluciona de forma crónica. En España afecta al 2,3% de la población, presentando una afectación por sexos semejante[1].
La gravedad o intensidad de la enfermedad viene determinada por factores tales como la forma clínica, la extensión y la intensidad de las lesiones, y juega un papel primordial en la elección del tratamiento. La determinación del PASI (psoriasis area and severity index) - que incluye tanto la extensión como la intensidad de las lesiones medidas en eritema, induración y descamación- es hoy en día el parámetro principal de medición del grado de actividad de la psoriasis. Otros índices de estimación de la gravedad de la enfermedad incluyen por ejemplo el body surface area (BSA) como medida simple de la extensión corporal afectada, el physician’s global assessment (PGA) como evaluación global por parte del médico, o el dermatology life quality index (DLQI), que evalúa la calidad de vida (no es específico para la psoriasis; se aplica también a otras enfermedades no necesariamente cutáneas)[2].
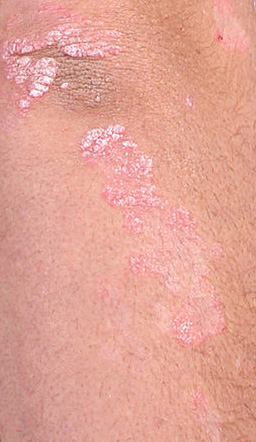
Un brazo con psoriasis
(imagen recortada) Autor/a del original: Jacopo188
Fuente: Wikimedia Commons
El tratamiento tópico conforma la base terapéutica para cualquier forma de psoriasis y juega un papel fundamental en las formas leves, siendo utilizado en las formas de moderadas a graves como adyuvante a las terapias sistémicas. Estas últimas comprenden diferentes modalidades entre las que se encuentran la fototerapia y los agentes sistémicos, ya sean biológicos o no[2].
La fototerapia es una opción terapéutica que ocupa un lugar destacado en cualquier guía de tratamiento para la psoriasis. En términos generales, dado que existen pautas concretas para su aplicación, es una técnica segura, aunque existe el riesgo de daño actínico que se puede presentar por medio de signos de envejecimiento cutáneo prematuro o bien en forma de complicaciones más serias, como el desarrollo de tumores cutáneos derivados de su efecto carcinógeno[3].
Los fármacos sistémicos para la psoriasis aprobados en España incluían hasta el momento diferentes principios activos con mayor o menor acción inmunosupresora: metotrexato, ciclosporina, acitretina y apremilast. Éstos presentan diferencias notables en cuanto a la efectividad y la seguridad. Metotrexato, aunque eficaz, suele ser lento en su inicio de acción y puede ser hepatotóxico y teratogénico.
Ciclosporina presenta en general una rápida respuesta, pero no se recomienda a largo plazo dado el riesgo de desarrollo de insuficiencia renal e hipertensión arterial, además de elevar la probabilidad de sufrir neoplasias cutáneas y linfoma. Acitretina tiene un campo de acción más limitado (es usada preferentemente para la afectación palmo-plantar o en formas pustulosas): interactúa de forma destacable con el metabolismo lipídico, y es altamente teratógenica[4]. Aunque más novedosos en el panorama terapéutico de la psoriasis, y por tanto con menor experiencia acumulada de uso, tanto apremilast como los fármacos biológicos presentan un perfil de efectividad-seguridad favorable, siendo el elevado coste que suponen para el sistema sanitario su principal inconveniente[4,5].
La reciente comercialización en España de dimetilfumarato como opción terapéutica sistémica para la psoriasis en las formas de moderadas a graves de la enfermedad, apoyada por su posicionamiento en las principales guías europeas como tratamiento de primera opción, amplía el actual arsenal terapéutico y supondrá un importante beneficio para numerosos pacientes que hasta ahora no tenían acceso a esta alternativa. Dimetilfumarato es el principal exponente de los ésteres del ácido fumárico (fumaratos o FAE, por sus siglas en inglés), que han demostrado tras décadas de uso en países centroeuropeos, donde suponen la primera opción terapéutica sistémica, una eminente y sostenida eficacia clínica combinada con un perfil de seguridad favorable para el tratamiento a largo plazo de la psoriasis de moderada a grave[6].
Ésteres de ácido fumárico (fumaratos)
Los fumaratos son utilizados desde hace más de tres décadas como principal tratamiento sistémico de la psoriasis en placas moderada-grave en algunos países centroeuropeos (sobre todo en Suiza, Alemania, Austria y Holanda). Las primeras investigaciones con fumaratos datan de 1959[7]. En las siguientes dos décadas se realizaron varios estudios pivotales de eficacia y seguridad, cuyos resultados llevaron a su aprobación como terapia sistémica para la psoriasis. En 1994 se aprobó finalmente Fumaderm® (Biogen Idec GmbH), una combinación de dimetilfumarato con las sales de calcio, magnesio y zinc de monoetilfumarato, que a lo largo de los años ha demostrado un perfil de eficacia y seguridad muy favorable en el tratamiento a largo plazo de la enfermedad[8,9]. Se considera que el ingrediente activo de la combinación es dimetilfumarato, ya que las sales de monoetilfumarato por sí solas no han demostrado eficacia clínica significativa[10].
El mecanismo de acción de los fumaratos es complejo, y aunque cada día se conoce mejor, siguen siendo necesarios estudios que profundicen en su funcionamiento. Lo que se sabe hasta hoy es que dimetilfumarato, el principal componente en las combinaciones de fumaratos, es el único con un efecto clínico demostrado[11].
La guías europeas[4] recomiendan el uso de los fumaratos tanto en fase aguda o brote como en el tratamiento a largo plazo de la psoriasis. El procedimiento clínico estándar consiste en iniciar el tratamiento con dosis bajas de fumaratos e ir aumentando progresivamente la dosis de acuerdo a la respuesta y tolerabilidad individual. A largo plazo los fumaratos han mostrado la mayor supervivencia acumulada en comparación los otros fármacos sistémicos no biológicos[12]. De hecho, se ha reportado que incluso algún paciente con psoriasis ha recibido tratamiento con fumaratos durante más de 30 años[13].
Skilarence®: el primer fumarato para psoriasis aprobado en España por la AEMPS
Skilarence®, comercializado por Almirall desde el 1 de Septiembre, es un nuevo tratamiento oral que contiene dimetilfumarato como único principio activo y que ha sido aprobado por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) para el tratamiento de la psoriasis en placas de moderada a grave en adultos que precisan de un tratamiento con un medicamento sistémico[14].
Dimetilfumarato presenta un doble mecanismo de acción sobre los linfocitos, inmunomodulador y antiinflamatorio, que provoca la conversión de los linfocitos con perfil Th1 y Th17 a Th2 (fenotipo menos inflamatorio), y favorece la producción de IL-4[14].
Sobre los queratinocitos actúa previniendo la expresión de citoquinas e inhibiendo la proliferación y diferenciación celular[15].
Otros mecanismos descritos son la inducción de eventos proapoptóticos, la expresión reducida de moléculas de adhesión y la disminución de los infiltrados inflamatorios en las placas psoriásicas[14].
![Mecanismo de acción de Skilarence®[14] Mecanismo de acción de Skilarence®[14] Fuente: Ficha técnica Skilarence®. Agencia Española de Medicamentos y Productos Sanitarios. Centro de Información del Medicamento. (Acceso: 11/2018). https://cima.aemps.es/cima/dochtml/ft/1171201004/FT_1171201004.html](http://farmacosalud.com/wp-content/uploads/2019/02/tabla-1.jpg)
Mecanismo de acción de Skilarence®[14]
Fuente: Ficha técnica Skilarence®. Agencia Española de Medicamentos y Productos Sanitarios. Centro de Información del Medicamento. (Acceso: 11/2018). https://cima.aemps.es/cima/dochtml/ft/1171201004/FT_1171201004.html
El estudio BRIDGE[10] es un estudio multicéntrico, aleatorizado, doble ciego, sobre una cohorte de 671 pacientes que fueron asignados aleatoriamente en 3 grupos (n=267, Skilarence®; n=273, Fumaderm®; n=131, placebo). El objetivo del estudio fue el de evaluar la eficacia y seguridad de dimetilfumarato para el tratamiento de adultos con psoriasis en placas de moderada a grave, y se llevó a cabo en Alemania, Austria, Países Bajos y Polonia.
Dimetilfumarato demostró no inferioridad frente a la combinación de fumaratos que se utiliza en Alemania (Fumaderm®), teniendo un efecto clínicamente significativo frente a placebo a las 16 semanas tanto en el PASI 75 (37,5% de los pacientes) como en la calidad de vida (reducción del 52% del DLQI)[10].
![Fuente: Estudio BRIDGE[10] Efficacy and safety of LAS41008 (dimethyl fumarate) in adults with moderate-to-severe chronic plaque psoriasis: a randomized, double-blind, Fumaderm® – and placebo-controlled trial (BRIDGE). Fuente: Estudio BRIDGE[10] Efficacy and safety of LAS41008 (dimethyl fumarate) in adults with moderate-to-severe chronic plaque psoriasis: a randomized, double-blind, Fumaderm® - and placebo-controlled trial (BRIDGE).](http://farmacosalud.com/wp-content/uploads/2019/02/tabla-2.jpg)
Fuente: Estudio BRIDGE[10] Efficacy and safety of LAS41008 (dimethyl fumarate) in adults with moderate-to-severe chronic plaque psoriasis: a randomized, double-blind, Fumaderm® - and placebo-controlled trial (BRIDGE).
Los acontecimientos adversos (AA) más frecuentes fueron trastornos gastrointestinales y rubefacción, sobre todo al inicio del tratamiento, así como linfopenia. La mayoría de los efectos adversos reportados fueron leves y controlables con ajuste de dosis, sin necesidad de discontinuar el tratamiento[10].
Debido a los resultados de los estudios y según puede observarse en la ficha técnica de Skilarence®[14], se recomienda comenzar el tratamiento con una dosis inicial baja seguida de aumentos graduales semanales en función de la tolerabilidad y la respuesta del paciente. Si una dosis concreta del escalado no se tolera se puede reducir temporalmente a la última dosis tolerada. Si el tratamiento tiene éxito antes de que se alcance la dosis máxima, no será necesario seguir aumentando la dosis. Se considera éxito terapéutico cuando se alcanza el objetivo que hayan pactado el dermatólogo juntamente con el paciente. Al alcanzar una mejoría clínicamente relevante de las lesiones cutáneas, la dosis diaria puede reducirse gradualmente hasta la dosis de mantenimiento que necesite el paciente. Este ajuste gradual de la dosis, así como la posibilidad de poder reducir la dosis de forma temporal, mejora notablemente la tolerabilidad, siendo una estrategia útil para minimizar el impacto de posibles acontecimientos adversos, sobre todo gastrointestinales[14].
Dado su carácter inmunomodulador puede reducir el recuento de leucocitos en general y linfocitos en particular, por lo que se recomienda monitorizarlos para prevenir posibles efectos adversos[14]. Antes de iniciar el tratamiento es necesario disponer de un hemograma completo reciente que incluya la fórmula leucocitaria y recuento de plaquetas. No se debe iniciar el tratamiento si se detecta una leucopenia <3000/μl, una linfopenia <1000/μl u otros resultados patológicos. Durante el tratamiento, se debe repetir la analítica cada 3 meses. Si se observan anomalías, es posible que se deba modificar la frecuencia de los controles, así como la dosis, tal y como se recoge en la tabla[14].
![Supervisión durante el tratamiento Supervisión durante el tratamiento Fuente: Ficha técnica Skilarence®[14]. Agencia Española de Medicamentos y Productos Sanitarios. Centro de Información del Medicamento. (Acceso: 11/2018). https://cima.aemps.es/cima/dochtml/ft/1171201004/FT_1171201004.html](http://farmacosalud.com/wp-content/uploads/2019/02/tabla-3.jpg)
Supervisión durante el tratamiento
Fuente: Ficha técnica Skilarence®[14]. Agencia Española de Medicamentos y Productos Sanitarios. Centro de Información del Medicamento. (Acceso: 11/2018). https://cima.aemps.es/cima/dochtml/ft/1171201004/FT_1171201004.html
Los fumaratos en el tratamiento a largo plazo de la psoriasis
La eficacia y seguridad a largo plazo de un fármaco sistémico es un aspecto fundamental para determinar su idoneidad durante periodos prolongados de tratamiento, dado que la psoriasis es una patología inflamatoria crónica asociada a un mayor riesgo de desarrollar otro tipo de enfermedades sistémicas como cardiovasculares y metabólicas[16,17].
El estudio retrospectivo FUTURE[6] recolectó datos sobre la seguridad y eficacia de los fumaratos en el tratamiento a largo plazo de la psoriasis de moderada a grave en 163 centros de Dermatología en Alemania.
Se incluyeron 984 pacientes con una duración media de 44 meses de tratamiento a dosis estándar. El 71% de los pacientes fueron tratados ininterrumpidamente con fumaratos durante al menos 2 años, siendo la duración media del tratamiento en este grupo de pacientes de 50 meses. El 46% recibió tratamiento con fumaratos durante más de 3 años (con interrupciones no superiores a 6 meses), siendo la duración media del tratamiento de 66 meses en este grupo.
La gravedad de las lesiones de la piel se evaluó con las escalas PGA y PASI, observándose que las tasas de mejoría notable y blanqueamiento eran similares en pacientes con enfermedad moderada o grave, y que éstas fueron aumentando hasta 1 año después de iniciado el tratamiento. Este supone un dato importante para recomendar no suspender la terapia de forma prematura ni determinar definitivamente la tasa de respuesta terapéutica antes de los 6 meses de tratamiento continuado[6].
![Curso de la enfermedad (según PGA) Curso de la enfermedad (según PGA) Fuente: Estudio FUTURE[6]. Efficacy and safety of fumaric acid esters in the long-term treatment of psoriasis – a retrospective study (FUTURE).](http://farmacosalud.com/wp-content/uploads/2019/02/tabla-4-600.jpg)
Curso de la enfermedad (según PGA)
Fuente: Estudio FUTURE[6]. Efficacy and safety of fumaric acid esters in the long-term treatment of psoriasis – a retrospective study (FUTURE).
Los cambios en los parámetros de laboratorio fueron por lo general insignificantes, no requiriéndose modificación del tratamiento en más del 90% de los casos[6].
Los autores concluyeron que en el tratamiento a largo plazo de pacientes con psoriasis de moderada a grave, los fumaratos muestran una eficacia clínica buena y sostenida, junto con un perfil de seguridad favorable[6].
Dickel y colaboradores[13] mostraron los datos de eficacia y seguridad en condiciones de práctica clínica mediante una cohorte de 859 pacientes, todos ellos pacientes naive a fumaratos en el momento de la inclusión. De ellos, 763 (88,8%) recibieron fumaratos como primer tratamiento sistémico. Solamente un 11,2% habían recibido anteriormente un tratamiento sistémico previo, sobre todo metotrexato (4,4%) o retinoides (4,4%). La dosis media recibida en el período de tiempo observado fue de 384,1 mg/d (equivalente a 3-4 comprimidos/día), siendo la duración media del tratamiento para toda la cohorte 3,6 años (rango de 0,1 a 32,5 años).
En relación a la efectividad, los índices PGA y PASI mostraron una mejoría de la gravedad de las lesiones, mejoría que mostró una tendencia alcista durante el tratamiento con fumaratos (tal y como se ha observado en otras series como la de Reich[6], dato que avala de nuevo la recomendación de realizar la valoración global de la eficacia no antes de 6 meses de tratamiento. En esta cohorte en concreto, el tiempo transcurrido desde el inicio de la terapia con fumaratos hasta una tasa de respuesta acumulativa de sPGA del 50% y al menos una reducción de 2 puntos en la PGA inicial fue de 1 año. Estos resultados fueron comparables tanto en la cohorte con monoterapia como en las que recibieron una terapia combinada con metotrexato o fototerapia, de forma que la asociación a ambas opciones no mostró un beneficio extra a largo plazo.
En cuanto a la seguridad, los AA más frecuentemente observados fueron las molestias gastrointestinales (aproximadamente en 1/3 de los pacientes). Aparecieron sobre todo en las primeras semanas, desde pocos minutos hasta 30 minutos tras la ingesta del preparado. En su mayoría resultaron ser de leves a moderados, y se resolvieron en la continuación del tratamiento. Raramente se necesitó ajustes de la dosis o retirada del medicamento. El segundo AA más frecuente fue la rubefacción (sensación de calor y eritema facial, 6-14%), que igualmente apareció al inicio del tratamiento y mostró una tendencia a la resolución a lo largo del tiempo.

Autor/a: George Hodan
Fuente: www.publicdomainpictures.net
Las alteraciones de la serie blanca (leucopenia, linfopenia y eosinofilia) conformaron el tercer AA en frecuencia. La proporción de pacientes en los que se decidió retirar la medicación por problemas hematológicos varió del 2,6 al 12%. La eosinofilia apareció en los primeros 3 meses para normalizarse después. De los pacientes que presentaron linfopenia, solamente en torno al 10% lo hicieron en términos de linfopenia severa (<500/μl). La caída más intensa del valor absoluto se observó en los primeros 3-6 meses.
Respecto a la afectación de la función renal, un porcentaje menor de pacientes puede presentar elevación de creatinina y/o proteinuria. En general los trastornos renales observados fueron reversibles con la reducción o la retirada del tratamiento; la retirada de la medicación se produjo solamente en una minoría de los casos.
Los fumaratos en las guías clínicas europeas para el tratamiento de la psoriasis
Las guías europeas para el tratamiento de la psoriasis incluyen los fumaratos desde 2009, cuando se evaluaron 13 estudios observándose buena eficacia tanto en la inducción como en el tratamiento a largo plazo[3]. Según dichas guías, el tratamiento con fumaratos para la psoriasis representa un tratamiento sistémico eficaz que ha demostrado una buena seguridad y tolerabilidad a largo plazo, limitado fundamentalmente por los efectos gastrointestinales y la rubefacción, aunque el análisis riesgo-beneficio de los fumaratos es positivo. Estas guías también señalan como aspectos positivos del tratamiento con fumaratos la ausencia de interacciones medicamentosas, así como el hecho de que el tratamiento a largo plazo no da lugar a un mayor riesgo de infecciones o enfermedades neoplásicas malignas[3].
La actualización de las guías clínicas europeas para tratamiento de la psoriasis, publicada en 2015, recomienda los fumaratos tanto para la inducción como en el tratamiento a largo plazo con un alto grado de consenso[4].
Referencias
1. Ferrándiz C, Carrascosa JM, Toro M. Prevalence of psoriasis in Spain in the age of biologics. Actas Dermosifiliogr. 2014 Jun;105(5):504-9.
2. Puig L, Bordas X, Carrascosa JM, Daudén E, Ferrándiz C, Hernanz JM, et al. Consensus document on the evaluation and treatment of moderate-to-severe psoriasis. Spanish psoriasis group of the Spanish Academy of Dermatology and Venereology. Actas Dermosifiliogr. 2009 May;100(4):277-86.
3. Pathirana D, Ormerod AD, Saiag P, Smith C, Spuls PI, Nast A, et al. European S3-guidelines on the systemic treatment of psoriasis vulgaris. J Eur Acad Dermatol Venereol. 2009 Oct;23 Suppl 2:5-70.
4. Nast A, Gisondi P, Ormerod AD, Salag P, Smith C, Spuls PI, et al. European S3-Guidelines on the systemic treatment of psoriasis vulgaris--Update 2015--Short version--EDF in cooperation with EADV and IPC. J Eur Acad Dermatol Venereol. 2015 Dec;29(12):2277-94.
5. Schmitt J, Rosumeck S, Thomaschewski G, Sporbeck B, Haufe E, Nast A. Efficacy and safety of systemic treatments for moderate-to-severe psoriasis: meta-analysis of randomized controlled trials. Br J Dermatol, 170(2):274-303.
6. Reich K, Thaci D, Mrowietz U, Kamps A, Neureither M, Luger T. Efficacy and safety of fumaric acid esters in the long-term treatment of psoriasis – a retrospective study (FUTURE). J Dtsch Dermatol Ges 2009; 7:603–10.
7. Schweckendieck W. Heilung von Psoriasis vulgaris. Med Monatsschr. 1959 Feb;13(2):103-4.
8. Mrowietz U, Altmeyer P, Bieber T, Röcken M, Schopf RE, Sterry W. Treatment of psoriasis with fumaric acid esters (Fumaderm). J Dtsch Dermatol Ges 2007; 5:716–17.
9. Balak DM, Fallah Arani S, Hajdarbegovic E, Hagemans CA, Bramer WM, Thio HB, et al. Efficacy, effectiveness and safety of fumaric acid esters in the treatment of psoriasis: a systematic review of randomized and observational studies. Br J Dermatol. 2016 Aug;175(2):250-62.
10. Mrowietz U, Szepietowski JC, Loewe R, van de Kerkhof P, Lamarca R, Ocker WG, et al. Efficacy and safety of LAS41008 (dimethyl fumarate) in adults with moderate-to-severe chronic plaque psoriasis: a randomized, double-blind, Fumaderm® - and placebo-controlled trial (BRIDGE). Br J Dermatol. 2017 Mar;176(3):615-623.
11. Nieboer C, de Hoop D, Langendijk PN, van Loenen AC, Gubbels J. Fumaric acid therapy in psoriasis: a double-blind comparison between fumaric acid compound therapy and monotherapy with dimethylfumaric acid ester. Dermatologica 1990; 181:33–7.
12. Arnold T, Schaarschmidt ML, Herr R, Fischer JE, Goerdt S, Peitsch WK1. Drug survival rates and reasons for drug discontinuation in psoriasis. J Dtsch Dermatol Ges. 2016 Nov;14(11):1089-1099.
13. Dickel H, Bruckner T, Altmeyer P. Long-term real-life safety profile and effectiveness of fumaric acid esters in psoriasis patients: a single-centre, retrospective, observational study. J Eur Acad Dermatol Venereol. 2018 Oct;32(10):1710-1727.
14. Ficha técnica Skilarence®. Agencia Española de Medicamentos y Productos Sanitarios. Centro de Información del Medicamento. (Acceso: 11/2018). https://cima.aemps.es/cima/dochtml/ft/1171201004/FT_1171201004.html
15. Brück J, Dringen R, Amasuno A, Pau-Charles I, Ghoreschi K. A review of the mechanisms of action of dimethylfumarate in the treatment of psoriasis. Exp Dermatol. 2018 Jun;27(6):611-624.
16. Boehncke S, Thaci D, Beschmann H, Ludwig RJ, Ackermann H, Badenhoop K, et al. Psoriasis patients show signs of insulin resistance. Br J Dermatol. 2007 Dec;157(6):1249-51.
17. Wu Y, Mills D, Bala M. Psoriasis: cardiovascular risk factors and other disease comorbidities. J Drugs Dermatol. 2008 Apr;7(4):373-7.





