Redacción Farmacosalud.com
La Food and Drug Administration (FDA) de Estados Unidos ha aprobado ZINPLAVA® (bezlotoxumab) en inyección de 25 mg/ml, informa la compañía MSD. Este fármaco está indicado en EE.UU. para reducir la recurrencia de la infección por Clostridium difficile (ICD) en pacientes de 18 años o más que estén recibiendo tratamiento antibiótico para la ICD y presenten alto riesgo de recurrencia por dicha infección. ZINPLAVA® no está indicado para tratar la ICD, ya que no es un antibiótico.
ZINPLAVA® solo debe utilizarse junto con antibióticos que tratan la ICD.
La infección por C. difficile está causada por bacterias que producen toxinas, entre ellas la toxina B. Los síntomas de la ICD pueden ser diarrea, de leve a grave, dolor abdominal y fiebre. La incidencia de ICD recurrente es mayor en ciertas poblaciones de pacientes, incluidas personas de 65 años o más de edad y personas con el sistema inmune comprometido.
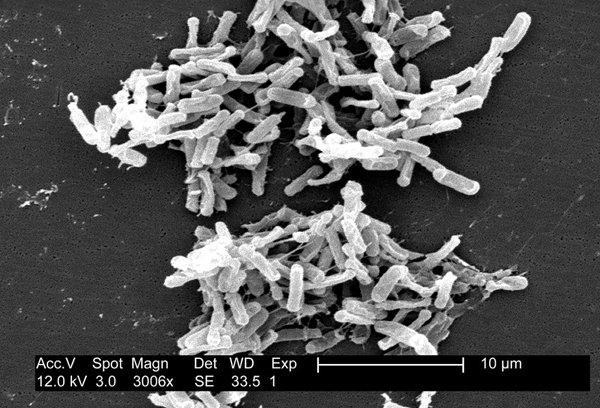
C. difficile al microscopio electrónico de barrido
Autor/a de la imagen: Transferido desde en.wikipedia a Commons. This media comes from the Centers for Disease Control and Prevention’s Public Health Image Library (PHIL), with identification number #6260. CDC Public Health Image Library. Image credit: CDC/ Lois S. Wiggs (PHIL #6260), 2004.
Fuente: Wikipedia
Un anticuerpo monoclonal humano que se une a la toxina B de C. difficile
“Durante generaciones, MSD se ha mantenido fiel a su compromiso de combatir las enfermedades infecciosas y ese compromiso continúa hoy. ZINPLAVA® es un anticuerpo monoclonal humano que se une a la toxina B de C. difficile y neutraliza sus efectos”, explica el Dr. Nicholas Kartsonis, vicepresidente de desarrollo clínico para enfermedades infecciosas, en MSD Research Laboratories.
Bezlotoxumab fue desarrollado por investigadores del MassBiologics Laboratory de la Facultad de Medicina de la Universidad de Massachusetts, conjuntamente con Medarex (ahora parte de Bristol-Myers Squibb), y MSD adquirió la licencia correspondiente en 2009.




