Redacción Farmacosalud.com
Investigadores del Salk Institute for Biological Studies de California, en colaboración con el Dr. Josep Maria Campistol, director general y nefrólogo del Hospital Clínic (Barcelona) y Marta Lazo, investigadora del IDIBAPS (Barcelona), han conseguido crear y mantener estructuras renales gracias a la utilización de un cultivo tridimensional y de una nueva combinación de moléculas de señalización. Es la primera vez que se consigue conservar un cultivo de células progenitoras de nefrona (CPN), lo que supone un gran espaldarazo a la investigación básica y traslacional sobre el desarrollo de las enfermedades renales y un paso más hacia la posibilidad de crear un riñón trasplantable. El estudio, liderado por el Dr. Juan Carlos Izpisua Belmonte, profesor del Laboratorio de Expresión Génica en el Salk Institute, se publica en la revista ‘Cell Stem Cell’.

Los doctores Juan Carlos Izpisua Belmonte (a la izq. de la imagen) y Josep M. Campistol
Fuente: Hospital Clínic
Los intentos previos de mantener cultivos de CPN habían fracasado, pero ahora se aporta "una prueba sobre cómo crear y mantener un número ilimitado de células precursoras de riñón", afirma el Dr. Izpisua, y añade que el hecho de conseguir "un suministro de estas células podría ser un punto de partida para hacer crecer órganos funcionales en el laboratorio, así como una manera de empezar a aplicar terapias celulares en riñones con genes defectuosos". Además de una terapia regenerativa para reemplazar órganos enfermos, las CPN podrían utilizarse para modelar enfermedades en los laboratorios. Mediante la introducción de mutaciones relacionadas con la enfermedad de las células, los investigadores serían capaces de estudiar su aparición y progresión y obtener nuevos conocimientos sobre ella que podrían derivar en el descubrimiento de medicamentos para su tratamiento.
Las CPN, presentes durante una breve etapa del desarrollo embrionario
Normalmente, las CPN están presentes, en los humanos, durante una breve etapa del desarrollo embrionario. Las células pasan a formar nefronas, la unidad básica y funcional del riñón responsable de la filtración de la sangre y de la excreción de la orina. Después de la vida embrionaria, no tenemos las CPN que permitirían hacer crecer nuevo tejido renal después de sufrir una enfermedad o daño, por lo que su generación en el laboratorio ofrecerá una nueva manera de estudiar el desarrollo del riñón y, finalmente, de tratar las enfermedades renales.
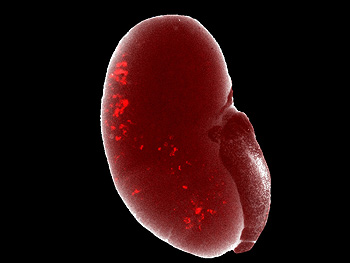
Células progenitoras renales de laboratorio (en rojo) después de ser trasplantadas a un riñón y que tienen la capacidad de integrarse funcionalmente y formar parte del mismo
Fuente: Hospital Clínic
Anteriormente, se habían utilizado otros métodos para conseguir crear células precursoras de riñón que sobrevivieran en el laboratorio. Sin embargo, en estas tentativas, las CPN maduraban en células de riñón adultas en cuestión de días y no dejaban células progenitoras para estudiar. El descubrimiento de los Dres. Izpisua, Zhongwei Li, también del Salk Instiute, Campistol y otros expertos se ha basado en la utilización de un cultivo donde las células podían crecer en un entorno tridimensional y no en un plano bidimensional, así como en una nueva combinación de moléculas de señalización, lo cual ha permitido conservar las CPN durante más de quince meses. Así, las células, gracias a estas nuevas condiciones, pueden ser inducidas a convertirse en estructuras de nefronas en el laboratorio o cuando se trasplantan en animales. El equipo del Salk Institute utilizó CPN embrionarias, así como otras, generadas de células madre, para ajustar el protocolo para el uso humano y se ha podido demostrar, en ambos casos, que las CPN se podían mantener a largo plazo.
El siguiente eslabón que se deberá superar es el de profundizar en la investigación sobre cómo poder cultivar otros tipos de progenitores indispensables para regenerar un riñón entero. "Hay varias células progenitoras que trabajan conjuntamente para crear un órgano completo", dice el Dr. Li, "Si somos capaces de cultivar también otras células progenitoras, estaremos más cerca de crear un riñón trasplantable", añade. Por otro lado, el cultivo tridimensional utilizado en este estudio puede aplicarse, potencialmente, para la formación de otros tejidos orgánicos.
Referencia del artículo:
Zhongwei Li, Toshikazu Araoka, Jun Wu, Hsin-Kai Liao, Mo Li, Marta Lazo, Bing Zhou, Yinghui Sui, Min-Zu Wu, Isao Tamura, Yun Xia, Ergin Beyret, Taiji Matsusaka, Ira Pastan, Concepcion Rodriguez Esteban, Pedro Guillen, Josep M. Campistol, and Juan Carlos Izpisua Belmonte. ‘3D Culture Supports Long-Term Expansion of Mouse and Human Nephrogenic Progenitors’. Cell Stem Cell (2016), DOI: 10.1016/j.stem.2016.07.016




