Doctor Fernando Anaya
Desde que en 1985 Brown y Goldstein fueron galardonados con el Premio Nobel de Medicina por su excelente trabajo sobre la regulación de Metabolismo del Colesterol, han dado lugar actualmente a nuevas Evidencias y Reflexiones, y estas son: 1) El Colesterol Total (CT) es un componente clave en el desarrollo de la ateroesclerosis. 2) Los niveles altos de CT son responsables de casi 4,5 millones de muertes cada año. 3) La reducción del CT y del C-LDL puede disminuir considerablemente la incidencia y la mortalidad de la enfermedad coronaria. El C-LDL y el CT son los objetivos terapéuticos primarios seleccionados en las recomendaciones europeas recientes sobre la prevención de la ECV en la práctica clínica. 4) Los Triglicéridos elevados y el C-HDL bajo no se consideran actualmente como objetivos terapéuticos sino como factores de riesgo CV emergentes y 5) La reducción de los niveles de Lp(a) son prioritarios en prevenir la ECV.
La base del tratamiento es conseguir el descenso del Colesterol Total (CT), (< 200 mg/dl (5.1mmol/l), de la LDL (< 100 mg/dl (2,6mmol/l) y Lp(a) (< 30 mg/dl (0.85mmol/l). Cuando el tratamiento convencional como: el ejercicio físico y la dieta, junto a grupos de fármacos más eficaces como los inhibidores de la hidroxi-metil-glutaril-CoA-reductasa o estatinas (inhibidores de la síntesis de colesterol intracelular), Ezetimibe y otros fármacos de última generación, no son eficaces para conseguir dicho objetivo, es cuando está indicado el tratamiento con LDL-Aféresis, siempre considerado como un tratamiento coadyuvante al tratamiento anterior y nunca alternativo.

Doctor Fernando Anaya
Fuente: Dr. Anaya
Definición de la LDL-Aféresis. La LDL-Aféresis es la eliminación selectiva de los componentes aterogenéticos del plasma, tales como Colesterol Total, LDL, Lp(a) y Fibrinógeno, conservando al mismo tiempo las lipoproteínas fisiológicas anti-aterogenéticas.
Indicación de la LDL-Aféresis. De acuerdo a la 'Guidelines on the Use of Therapeutic Apheresis in Clinical Practice Evidence Based Approach from the Apheresis Applications Committee of the American Society for Apheresis', se considera la indicación y eficacia de la LDL-Aféresis como Evidencia A o Categoría 1 en las siguientes dislipemias: [1-2]
-Hipercolesterolemia Familiar Homocigótica.
-Pacientes con Hipercolesterolemia Familiar Heterocigótica, acompañados de Enfermedad Arteriosclerótica Severa, y riesgo de enfermedad isquémica progresiva que no se controlan con dieta y altas dosis de Estatinas de última generación y Ezetemibe y otros fármacos.
-Hipercolesterolemia severa que tienen >1 de un factor de riesgo de EAC definido por el último reporte de la National Cholesterol Education Program Expert Panel, con intolerancia, contraindicación o no respuesta al tratamiento convencional.
-Lp(a) > 60 mg/dl con cardiopatía isquémica en pacientes relativamente jóvenes (< 55 años) y antecedentes familiares de ECV.
-Hipertrigliceridemias agudas (>1000 mg/dl).
Procedimientos de LDL-Aféresis.- Existen 5 métodos distintos disponibles: 1) Plasmaféresis de Doble Filtración; 2) Inmunoabsorción Específica; 3) Absorción mediante Sulfato Dextrano; 4) Precipitación Extracorpórea de las LDL y 5) Absorción Directa de Lipoproteínas (DALI). Las distintas técnicas reducen de forma rápida el CT, LDL, VLDL y Lp(a ) entre un 60 y 80%. Una vez que el procedimiento finaliza, las distintas partículas se van acumulando nuevamente dependiendo de su tasa de producción. De ahí, que la frecuencia de la aféresis suela ser una vez cada 2 semanas en la HF homocigota y cada 3 semanas en la HF heterocigota grave o con enfermedad coronaria que no responde satisfactoriamente al tratamiento farmacológico. La duración del procedimiento es aproximadamente de 2-3 horas y la tolerancia es buena. La incidencia de efectos adversos es generalmente baja y suele ser similar con todos los métodos. El efecto adverso más frecuente es el descenso de la presión arterial, que puede afectar al 3% de los casos.
Los procedimientos utilizados por nosotros han sido: Doble Filtración en 3.825 tratamientos y DALI en 662 tratamientos. [3-7]
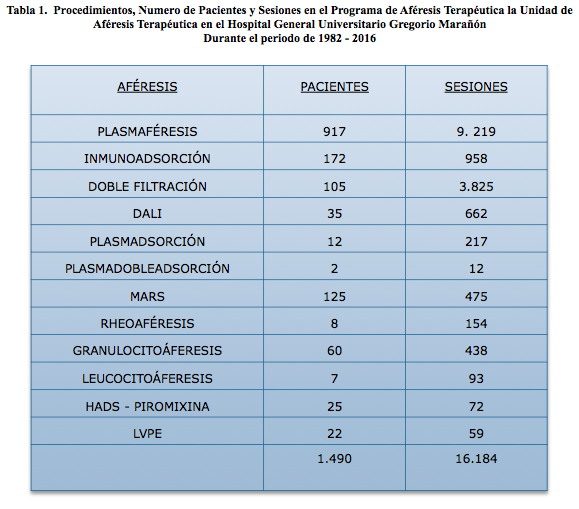
Resultados. En nuestro Programa de Aféresis Terapéutica, que iniciamos en junio de 1982, hasta la fecha actual, se han realizado 16.184 tratamientos de Aféresis en 1.490 pacientes como se muestra en la Tabla 1. Dentro del mismo figuran los tratamientos de LDL-Aféresis, como la Doble Filtración en 105 pacientes con 3.825 tratamientos y el DALI en 35 pacientes y 662 tratamientos. La tolerancia de ambos procedimientos fue muy buena en la mayoría de los pacientes, presentando solo complicaciones del acceso vascular el 0,54% e Hipotensión durante el procedimiento el 1,98%.
Los resultados del efecto del tratamiento de la LDL-Aféresis sobre los valores de Lipoproteinas quedan reflejados en la Tabla 2.
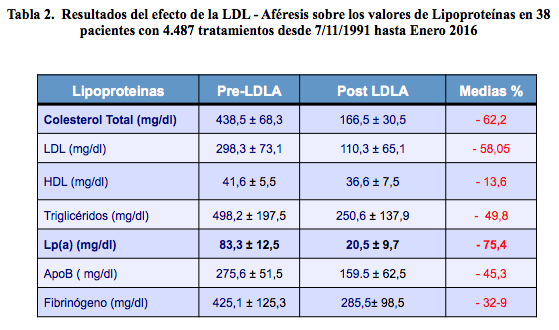
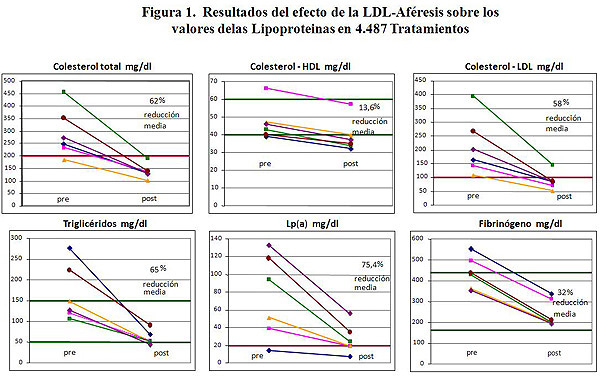
Es de reseñar el descenso del Colesterol Total en un 62.2%, la LDL en un 58.05%, y la Lp(a) en un 75,4%. La HDL en 13.6%, los Triglicéridos en 49.8% y la ApoB en un 45, 3%. De forma gráfica se muestran estos descensos en la Figura 1.
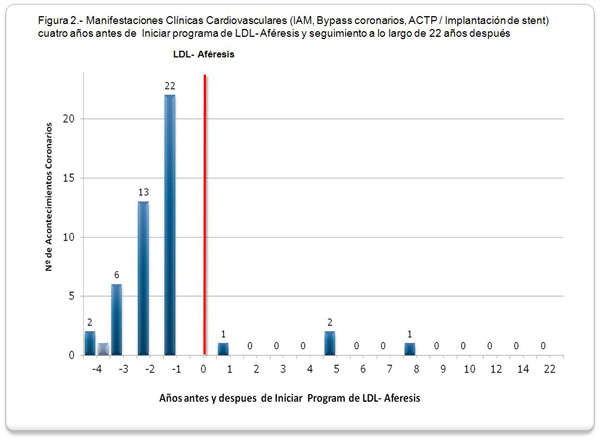
En la Figura 2, se muestran las manifestaciones Clínicas Cardiovasculares (IAM, Bypass coronarios, ACTP / Implantación de stent) cuatro años antes de Iniciar programa de LDL-Aféresis y el seguimiento a lo largo de 22 años.
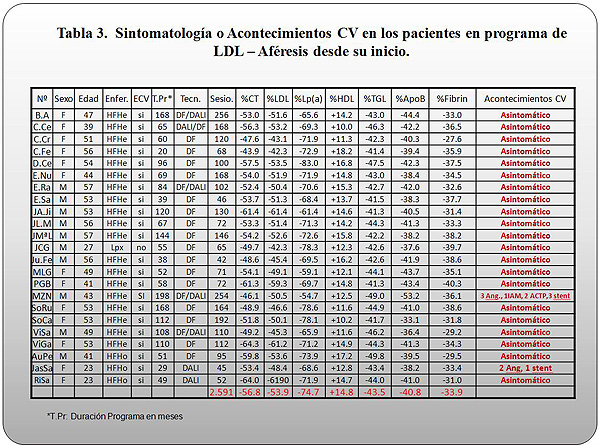
La presencia de cualquier sintomatología o acontecimientos CV en los pacientes en programa de LDL–Aféresis desde su inicio, queda reflejada en la Tabla 3.
Lp(a). No podemos dejar de mencionar la importancia de la Lp(a) dentro de la hipercolesterolemia familiar severa y su tratamiento con LDL-Aféresis. Descubierta por Kare Berg en 1963, hoy se conoce bien su estructura molecular, el lugar de su síntesis y su determinación genética. La Lp(a), cuyas concentraciones están determinadas genéticamente, permanecen relativamente estables durante toda la vida de un individuo y no se afectan por la dieta ni el ejercicio físico. Valores plasmáticos de Lp(a) > 30 mg/dl pueden indicar un factor de riesgo independiente para la EAC. La Lp(a) elevada no tiene actualmente un tratamiento farmacológico específico y eficaz. La LDL-Aféresis es el único tratamiento efectivo para disminuir los niveles de Lp(a) en más de un 60%. Con coronariográfica y ultrasonido intravascular se ha observado una disminución del volumen del ateroma hasta en un 7.2 mm³ cuando la Lp(a) se disminuye un 60%.
Hace 8 años incluimos en nuestro programa de LDL-Aféresis a pacientes con FRCV y ECV y como único factor de riesgo cifras elevadas de Lp(a). En el momento actual son 10 pacientes y se han realizado 145 tratamientos, con un plan de un tratamiento cada 15-30 días. Muy buena tolerancia, un descenso de las cifras de Lp(a) entre un 60%-75% y sin ninguna complicación.
Su uso en clínica aún no constituye una práctica generalizada a pesar de poseer un importante valor predictivo en la cardiopatía coronaria de aparición temprana y estar vinculada también en los fenómenos trombogénicos (efecto aterotrombótico). Dos metaanálisis han demostrado que la concentración de Lp(a) está asociada con un riesgo CV aumentado, por lo que la Sociedad Europea de Arteriosclerosis (EAS) ha recomendado la detección de Lp(a) en pacientes jóvenes con FRCV o antecedentes de Cardiopatía Isquémica (< 45 años) y con Hipercolesterolemia Familiar o no controlable. Una concentración sanguínea elevada de Lp(a) se asocia con: a) Un riesgo aumentado de infarto del miocardio y de la enfermedad de la arteria coronaria, b) De restenosis de un injerto vascular y d) De oclusión arterial de la retina.
En la actualidad se recomienda la medición de la Lp(a) en varios subgrupos de pacientes en los cuales el exceso de Lp(a) puede tener consecuencias clínicas importantes. Entre estos se encuentran: 1) Pacientes con aterosclerosis prematura. 2) Pacientes con historia familiar fuerte de enfermedad coronaria prematura. 3) Pacientes con colesterol-LDL elevado y factor de riesgo mayor o igual a 2 factores de riesgo y 4) Pacientes que han tenido una angioplastia o bypass coronario, en los cuales el exceso de Lp(a) pueden aumentar el riesgo de restenosis.[7-15]
Fuente: Archivo
Conclusión
La LDL-Aféresis es segura y eficaz. Es la única opción terapéutica disponible coadyuvante al tratamiento farmacológico convencional cuando éste no responde o hay intolerancia al mismo, en la HF homocigota, así como en la HF heterocigota grave u otros casos de Hiperlipemias graves. También está claramente indicada en pacientes con Lp(a) elevada, como único factor dislipémico y antecedentes de ECV o riesgos de presentarlos por antecedentes familiares o estar acompañados de otros factores de riesgos CV. Aunque el coste de aproximadamente 1.500-1.700 € por sesión es sustancial, se estima que el coste anual total de la LDL-aféresis representa menos del 1% de la cantidad gastada anualmente en la hemodiálisis de los enfermos renales.
Sus efectos han mostrado ser claramente beneficiosos: a) Descienden significativamente las fracciones aterogenéticas del plasma (Colesterol Total, LDL, Lp(a) y Fibrinógeno), b) Elimina los depósitos aterogenéticos: aterosis, xantelasmas y xantomas, c) Tiene una acción altamente antiinflamatoria, d) Aumenta significativamente la proliferación de las Células Endoteliales Progenitoras (CEP) y e) Aumenta significativamente la expresión del enzima sintetasa endotelial del óxido nítrico (eNOS) en las CEP.
Bibliografía
1. Guidelines on the use of therapeutic apheresis in clinical practice-evidence-based approach from the Writing Committee of the American Society for Apheresis: the sixth special issue. Schwartz J, Winters JL, Padmanabhan A, Balogun RA, Delaney M, Linenberger ML, Szczepiorkowski ZM, Williams ME, Wu Y, Shaz BH.J Clin Apher. 2013.
2. Guidelines for the management of familial hypercholesterolemia.Harada- M, Arai H, Oikawa S, Ohta T, Okada T, Okamura T, Nohara A, Bujo H, Yokote K, Wakatsuki A, Ishibashi S, Yamashita S. J Atheroscler Thromb. 2012;19(12)
3. Long-Term Follow-Up of a Homozygous Familial Hypercholesterolemic Patient Receiving Regular Double Filtration Plasmapheresis - Case Report and Literature Review. Tsai JL, Wu MJ, Shu KH, Tsai SF. Blood Purif. 2016 Jan 6;41(4):264-269.
4. Familial hypercholesterolemia. Bouhairie VE, Cardiol Clin. 2015 May;33(2):169-79.Review
5. Impact of LDL apheresis on aortic root atheroma in children with homozygous familial hypercholesterolemia. Lefort B, Saheb S, Bruckert E, Giraud C,. Atherosclerosis. 2015 Mar; 239 (1):158-62.
6. Recommendations for the management of patients with homozygous familial hypercholesterolaemia: overview of a new European Atherosclerosis Society . Bruckert E. Atheroscler Suppl. 2014 Sep;15(2):26-32. Review
7. Lipoprotein(a), cardiovascular disease, and contemporary management. Jacobson TA Mayo Clin Proc. 2013 Nov;88(11):1294-311. Review.
8. LDL-apheresis affects markers of endothelial function in patients with homozygous familial hypercholesterolemia. Nenseter MS, Bogsrud MP, Græsdal A, Narverud I, Halvorsen B, Ose L, Aukrust P, Holven KB. Thromb Res. 2012 Nov;130(5):823-5
9. Lipoprotein(a) Levels and Risk of Future Coronary Heart Disease Arch Intern Med. 2008;168(6):598-608
10. Shape of the Association Between Baseline Lp(a) Concentration and CVD Risk (826 Participants, 148 Incident CVD Events) Peter Willeit, MD, PHD. Journal Of The American College Of Cardiology. Vol. 64, No. 9, 2014
11. La lipoproteína (a) es predictora de severidad angiográfica en varones menores de 50 años con inicio clínico de enfermedad coronaria. Alberto Batalla Celorioa, José Julián Rodríguez Reguero, Gustavo Iglesias Cubero, Sergio Hevia Nava, Socorro Braga Fernández, Enrique Fernández Bustillo y Arturo Cortina Llosa. Sección de Cardiología. Hospital de Cabueñes. Gijón.Servicio de Cardiología. Hospital Central de Asturias. Oviedo. Rev Esp Cardiol Vol. 53, Núm. 8, Agosto 2000;
12. Lipoprotein(a) as a cardiovascular risk factor:current status. Børge G. Nordestgaard1*, M. John Chapman2, Kausik Ray3, Jan Bore´n4, Felicita Andreotti 5, Gerald F.Watts 6, Henry Ginsberg7, European Heart Journal (2010) 31, 2844–2853
13. Is Lp(a) Ready for Prime Time? Stephen J. Nicholls, MBBS, PHD,yz Alex Brown, MBBS, Phdyx Journal of The American College Of Cardiology VolL . 64, No. 9, 2 0 1 4
14. Discrimination and Net Reclassification of Cardiovascular Risk With Lipoprotein(a) Prospective 15-Year Outcomes in the Bruneck Study Peter Willeit, MD, PHD,*y Stefan Kiechl, MD,* Florian Kronenberg, MD,z Joseph L. Witztum, MD, PHD,x Peter Santer, MD,k Manuel Mayr, MD, PHD,{ Qingbo Xu, MD, Sotirios Tsimikas, MDx . Journal of The American College Of Cardiology Vol . 64, No. 9, 2014
15. Clinical benefit of long-term lipoprotein apheresis in patients with severe hypercholesterolemia or Lp(a)-hyperlipoproteinemia with progressive cardiovascular disease. Franz Heigl • Reinhard Hettich • Norbert Lotz • Harduin Reeg • Tobias Pflederer • Dirk Osterkorn • Klaus Osterkorn • Reinhard Klingel. Clin Res Cardiol Suppl DOI 10.1007/s11789-015-0071-3 February 2015




