Redacción Farmacosalud.com
La llegada de JINARC ® (tolvaptan) marca un antes y un después… además de un ‘quizás’ más que esperanzador para los pacientes de poliquistosis renal autosómica dominante (PQRAD). De entrada, el fármaco -el primero aprobado en Europa para adultos con PQRAD- “enlentece el deterioro del funcionamiento renal y disminuye el crecimiento de los riñones”, asegura la doctora Roser Torra Balcells, responsable de la Unidad de Enfermedades Renales Hereditarias de la Fundación Puigvert de Barcelona, Universidad Autónoma de Barcelona. Tolvaptan también tiene un “efecto positivo sobre el dolor” y “retrasa la necesidad de diálisis o trasplante con la consecuente mejora en calidad de vida” para el paciente, señala Torra. Por ahora ya queda claro que el nuevo fármaco marca un antes y un después en el tratamiento de la poliquistosis renal autosómica dominante… el ‘quizás’ más que esperanzador llega con la siguiente pregunta: ¿Tolvaptan puede llegar a evitar que un paciente de poliquistosis renal autosómica dominante acabe teniendo que someterse a diálisis o bien a un trasplante renal? “Potencialmente sí, pero habría que hacer estudios, dándolo en fases tempranas de la enfermedad y siguiendo a los pacientes durante muchos años con el fin de asegurarlo”, responde la nefróloga.

Doctora Roser Torra
Fuente: Cícero Comunicación
La compañía Ostuka Pharmaceutical Co., Ltd. ha anunciado que la Comisión Europea ha concedido la autorización de comercialización para tolvaptan para el tratamiento de la PQRAD en adultos con enfermedad renal crónica (ERC) en estadios uno a tres al inicio del tratamiento y que presentan características de rápida progresión de su enfermedad. Al recibir esta autorización de comercialización, tolvaptan se convierte en el primer tratamiento farmacéutico autorizado en Europa para el tratamiento de la fisiopatología subyacente de la PQRAD. Hasta la llegada de este medicamento, a los afectados de poliquistosis renal autosómica dominante se les trataba “mediante consejos para mantener una buena salud cardiovascular y el tratamiento propio de las alteraciones asociadas a la insuficiencia renal. Asimismo, se tratan las complicaciones propias de la poliquistosis como aneurismas cerebrales y crisis quísticas de forma específica. Las guías clínicas españolas son una buena herramienta para el manejo del paciente poliquístico”, remarca la doctora Torra.
Administración oral, dos veces al día
Tolvaptan, que se administra “por vía oral, dos veces al día”, estará disponible en España “cuando lo autorice la Agencia Española del Medicamento y se le asigne un precio para su comercialización”, comenta la especialista.
La autorización de comercialización para tolvaptan se basa en los resultados de un estudio pivotal fase III, randomizado, doble ciego y controlado con placebo: el estudio TEMPO 3:4 -el mayor estudio clínico realizado en pacientes con PQRAD hasta la fecha[1]-. En el estudio de tres años de duración, la tasa de crecimiento del volumen renal total (VRT) durante un periodo de 3 años fue significativamente menor para los sujetos tratados con tolvaptan que para los sujetos que recibieron placebo: 2,80% al año frente a 5,51% al año, respectivamente (cociente de medias geométricas 0,974; IC del 95% 0,969 a 0,980; p <0,0001); estos datos demuestran una reducción significativa de aproximadamente del 50% del incremento anual del VRT frente a placebo[3]. Además, tolvaptan mostró una reducción estadísticamente significativa en el riesgo de múltiples eventos relacionados con empeoramiento de la función renal, dolor renal, hipertensión o albuminuria (hazard ratio = 0,87, IC del 95%: 0,78-0,97, p=0,0095)[3]. Los resultados del objetivo secundario compuesto más importante se atribuye principalmente a los efectos sobre el empeoramiento de la función renal (61,4% menos probable con tolvaptan que con placebo) y el dolor renal médicamente significativo (35,8% menos probable en los pacientes tratados con tolvaptan)[3].
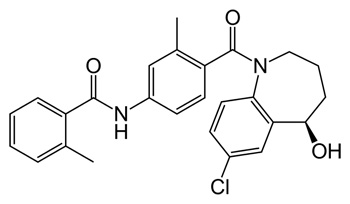
Diagrama estructural de tolvaptan
Autor/a de la imagen: Fvasconcellos
Fuente: Wikipedia
Análisis de sangre durante los primeros 18 meses de tratamiento
Aparte de los efectos secundarios asociados a los mecanismos de acción de tolvaptan (p. ej., sed, poliuria, poliaquiuria), la mayoría de los efectos secundarios observados en los pacientes con PQRAD que recibieron tolvaptan fueron comparables a los que recibieron placebo[1]. No obstante, se detectó un riesgo de lesión hepática en los pacientes con PQRAD que tomaban tolvaptan. Se observó una elevación de la alanina transaminasa (ALT) en el 4,4% de los pacientes tratados con tolvaptan y el 1% de los pacientes tratados con placebo[3]. Dos (2/957, 0,2%) pacientes tratados con tolvaptan, además de un tercer paciente en el ensayo abierto de extensión, presentaron aumentos clínicamente significativos de la ALT con elevaciones concomitantes de la bilirrubina total (BT)[3]. Aunque estas elevaciones concomitantes fueron reversibles con la suspensión inmediata de tolvaptan, representan una posibilidad de lesión hepática significativa, de manera que los pacientes que toman tolvaptan tendrán que someterse a análisis de sangre mensuales durante los primeros 18 meses de tratamiento con tolvaptan y cada tres meses a partir de entonces para mitigar este riesgo[3]. “Se ha detectado -precisa Torra- que un bajo porcentaje de pacientes muestra elevación reversible de los enzimas hepáticas durante los primeros 18 meses. De aquí viene la recomendación de analizar estos parámetros de forma mensual durante los primeros 18 meses y trimestral a continuación. La elevación de enzimas hepáticas podría conducir, de forma excepcional, a un daño hepático grave y el programa de análisis mensual está diseñado para minimizar este riesgo”. El tratamiento con tolvaptan debe ser iniciado y monitorizado bajo la supervisión de un clínico experto en el manejo de PQRAD que debe comprender los riesgos asociados a la terapia con tolvaptan incluyendo la toxicidad hepática y las necesidades de monitorización[3].
La PQRAD es la enfermedad renal hereditaria más frecuente y se caracteriza principalmente por la proliferación y el crecimiento de múltiples quistes llenos de líquido en el riñón[1,6]. El crecimiento y la expansión de los quistes en ambos riñones conduce al progresivo deterioro de la función renal. Así las cosas, aproximadamente la mitad de los pacientes acaban desarrollando enfermedad renal terminal (ERT) y requieren terapia renal sustitutiva (TRS), ya sea en forma de diálisis o trasplante renal alrededor de los 54 años[2,7]. La PQRAD es la cuarta causa de ERT en el adulto[8] y representa en torno al 10% de los pacientes que necesitan TRS[9].
Un potente antagonista de los receptores V2 de la vasopresina
Tolvaptan es un potente antagonista de los receptores V2 de la vasopresina que ha demostrado enlentecer el crecimiento de quistes y el deterioro de la función renal en pacientes con PQRAD en ERC en estadios uno a tres, que presentan características de rápida progresión de su enfermedad[1]. La formación de quistes asociados a la PQRAD puede producir daño renal significativo, aunque la función renal no esté afectada[10] y provocar complicaciones como dolor agudo y crónico, hipertensión y fallo renal[1]. Además de los síntomas físicos, la PQRAD provoca una profunda carga psicológica y emocional para las personas que viven con la enfermedad, sus familias y sus seres queridos[11-13]. Al bloquear de manera selectiva la vasopresina en su receptor V2, tolvaptan reduce la proliferación de las células de los quistes y la secreción de líquido, reduciendo a la larga el desarrollo de quistes y de los eventos clínicos renales asociados a la progresión de la enfermedad[14].
Referencias bibliográficas
1. Torres VE, Harris PC et al. Tolvaptan in patients with autosomal dominant polycystic kidney disease. The New England Journal of Medicine. 2012;367 (25): 2407-2418
2. Takiar V, Caplan MJ. Polycystic kidney disease: pathogenesis and potential therapies. Biochimica et Biophysica Acta. 2011;1812(10):1337-43
3. JINARC® (tolvaptan) summary of product characteristics 2015
4. Neumann H, Jilg C et al. Epidemiology of autosomal-dominant polycystic kidney disease: an in-depth clinical study for south-western Germany. Nephrology Dialysis Transplantation. 2013;28:1472-1487
5. Patch C, Charlton J et al. Use of antihypertensive medications and mortality of patients with autosomal dominant polycystic kidney disease: a population-based study. American Journal of Kidney Disease. 2011;57(6):856-862
6. Patel V, Chowdhury R et al. Advances in the pathogenesis and treatment of polycystic kidney disease. Current Opinion in Nephrology and Hypertension. 2009;18:99-106
7. Alam A, Perrone RD. Management of ESRD in Patients With Autosomal Dominant Polycystic Kidney Disease. Advances in Chronic Kidney Disease. Vol 17, No 2. March 2010: pp 164-172.
8. Masoumi A, Reed-Gitomer B et al. Developments in the Management of Autosomal Dominant Polycystic Kidney Disease. Therapeutics and Clinical Risk Management. 2008;4(2):393–407
9. Thong KM, Ong ACM. The natural history of autosomal dominant polycystic kidney disease: 30-year experience from a single centre. QJM. 2013;2-8
10. Grantham JJ, Chapman AB et al. Volume progression in Autosomal Dominant Polycystic Kidney Disease: The Major Factor Determining Clinical Outcomes. Clinical Journal of the American Society of Nephrology. 2006;1:148-157
11. Christophe JL, van Ypersele de Strihou C et al. Complications of autosomal dominant polycystic kidney disease in 50 haemodialysed patients. A case-control study. Nephrology Dialysis Transplantation. 1996;11(7):1271-1276
12. Rizk D, Jurkovitz C et al. Quality of life in Autosomal Dominant Polycystic Kidney Disease patients not yet on dialysis. Clinical Journal of the American Society of Nephrology. 2009;4:560-6
13. Perlman RL, Finkelstein FO et al. Quality of life in chronic kidney disease (CKD): a cross-sectional analysis in the Renal Research Institute-CKD study. American Journal of Kidney Diseases. 2005;45:658-66
14. Reif GA, Yamaguchi T et al. Tolvaptan inhibits ERK-dependent cell proliferation, Cl− secretion, and in vitro cyst growth of human ADPKD cells stimulated by vasopressin. American Journal of Physiology - Renal Physiology. 2011;301(5):F1005-F1013




