Redacción Farmacosalud.com
Astellas Pharma y Pfizer han anunciado resultados positivos del ensayo clínico fase 3 EV-304 (también conocido como KEYNOTE-B15) con PADCEV™ (enfortumab vedotina), un conjugado anticuerpo-fármaco (ADC, por sus siglas en inglés) dirigido contra la proteína nectina-4, en combinación con Keytruda™ (pembrolizumab), un inhibidor de PD-1, en pacientes con cáncer de vejiga músculo-invasivo (MIBC, por sus siglas en inglés) elegibles para quimioterapia basada en cisplatino. El tratamiento perioperatorio (antes y después de la cirugía) con enfortumab vedotina + pembrolizumab demostró una reducción del 47% en el riesgo de recurrencia tumoral, progresión o muerte en comparación con los pacientes tratados con el estándar de tratamiento neoadyuvante (antes de la cirugía) con gemcitabina y cisplatino (HR 0,53; IC 95%: 0,41–0,70; p unilateral <0,0001).
Se estima que el 79,4% de los pacientes no presentaron eventos a los dos años, en comparación con el 66,2% de los tratados con quimioterapia neoadyuvante estándar1. Estos datos se han presentado en el Simposio sobre Cánceres Genitourinarios de la American Society of Clinical Oncology (ASCO GU), celebrado en San Francisco (Estados Unidos).

Fuente: Archivo
Posible cambio respecto a la ‘quimio’ basada en platino como pilar básico del tratamiento
Christopher Hoimes, director del Programa de Cáncer de Vejiga y del Centro de Inmunoterapia Oncológica del Duke Cancer Institute (EE.UU.), e investigador principal del ensayo EV-304, señala: “aproximadamente la mitad de los pacientes con cáncer de vejiga músculo-invasivo experimentan recurrencia de la enfermedad incluso después de la extirpación de la vejiga. Los resultados del EV-304, junto con los del estudio EV-303, aportan evidencia sólida de que el tratamiento perioperatorio con enfortumab vedotina más pembrolizumab puede ofrecer beneficios en supervivencia en un escenario potencialmente curativo para los pacientes con cáncer de vejiga músculo-invasivo, lo que sugiere un posible cambio respecto a la quimioterapia basada en platino como pilar fundamental del tratamiento”.
La supervivencia global fue un criterio de valoración secundario clave en el ensayo EV-304 y mostró una reducción del 35% en el riesgo de muerte en pacientes tratados con enfortumab vedotina más pembrolizumab en el entorno perioperatorio frente a la quimioterapia neoadyuvante (HR 0,65; IC 95%: 0,48–0,89; p unilateral = 0,0029)1.
Tasa de respuesta completa patológica (pCR) del 55,8%
La combinación también demostró una tasa de respuesta completa patológica (pCR) del 55,8%, frente al 32,5% en el momento de la cirugía (diferencia estimada del 23,4%; IC 95%: 16,7–29,8; p unilateral <0,0001), lo que indica que más de la mitad de los sujetos tratados con la combinación no presentaban enfermedad detectable en el momento de la cirugía. Los beneficios en supervivencia libre de eventos (EFS), supervivencia global (OS) y pCR fueron generalmente consistentes en todos los subgrupos predefinidos, incluidos edad, sexo, estado de PD-L1, estadio clínico y región geográfica1.
El perfil de seguridad del tratamiento perioperatorio con enfortumab vedotina más pembrolizumab observado en el ensayo EV-304 fue coherente con la experiencia previa con la combinación y no se identificaron nuevas señales de seguridad. Los acontecimientos adversos de grado ≥3 por cualquier causa se produjeron en el 75,7% de los pacientes tratados con la combinación, frente al 67,2% de los pacientes tratados con quimioterapia neoadyuvante1.
El tumor malignos vesical es el noveno cáncer más frecuente en el mundo y se diagnostica en más de 614.000 pacientes cada año a nivel global. El cáncer de vejiga músculo-invasivo (MIBC) supone cerca del 30% de todos los casos de cáncer de vejiga. En España, se espera que en 2026 se diagnostiquen casi 24.000 nuevos casos de tumores vesicales, lo que lo convierte en el quinto tumor más frecuente en territorio español. Incluso tras someterse a una cirugía con intención curativa, la mitad de los pacientes con MIBC experimenta una recurrencia de la enfermedad2-5.

Autor/a de la imagen: gerasimov
Fuente: depositphotos.com
Actualmente, enfortumab vedotina más pembrolizumab no está aprobado como tratamiento perioperatorio en pacientes con MIBC candidatos a cisplatino. Esta combinación fue aprobada en noviembre de 2025 por la Administración estadounidense de Alimentos y Medicamentos (FDA) como tratamiento perioperatorio en pacientes con MIBC no candidatos a cisplatino, basándose en los resultados del ensayo clínico fase 3 EV-303 (también conocido como KEYNOTE-905), que fueron publicados en ‘The New England Journal of Medicine’.
En ambos brazos del ensayo se llevó a cabo cirugía con intención curativa
El ensayo EV-304 es un estudio de fase 3, en curso, abierto, aleatorizado y controlado, que evalúa enfortumab vedotina en combinación con pembrolizumab como tratamiento neoadyuvante y adyuvante frente a quimioterapia neoadyuvante (gemcitabina y cisplatino) en pacientes con MIBC candidatos a quimioterapia basada en cisplatino. Los pacientes fueron aleatorizados para recibir tratamiento neoadyuvante y adyuvante con enfortumab vedotina en combinación con pembrolizumab (brazo A) o quimioterapia neoadyuvante (brazo B). En ambos brazos se realizó cirugía con intención curativa (cistectomía). En el brazo de combinación, enfortumab vedotina junto con pembrolizumab se administró con un total planificado de 9 ciclos de enfortumab vedotina y 17 ciclos de pembrolizumab, distribuidos antes y después de la cirugía6.
El criterio principal de valoración del ensayo es la supervivencia libre de eventos, definida como el tiempo desde la aleatorización hasta la primera aparición de cualquiera de los siguientes acontecimientos: progresión de la enfermedad que impida la realización de una cistectomía radical o imposibilidad de someterse a dicha operación en participantes con enfermedad residual, enfermedad residual macroscópica en el momento de la cirugía, recurrencia local o a distancia evaluada mediante revisión central independiente y ciega (BICR), o muerte por cualquier causa. Entre los criterios secundarios clave se incluyen la supervivencia global (SG) y la tasa de respuesta completa patológica (pCR)7.
Nectina-4: proteína de adhesión localizada en la superficie de las células tumorales
Enfortumab vedotina es un conjugado anticuerpo-fármaco (ADC, por sus siglas en inglés), primero de su clase, dirigido frente a nectina-4, una proteína de adhesión localizada en la superficie de las células tumorales y altamente expresada en el cáncer de vejiga. Datos no clínicos sugieren que la actividad antitumoral de PADCEV™ se debe a su unión a las células que expresan nectina-4, seguida de su internalización y la liberación del agente antitumoral monometil auristatina E (MMAE) en el interior de la célula, lo que induce la detención del ciclo celular (arresto del ciclo celular) y la muerte celular programada (apoptosis)8.
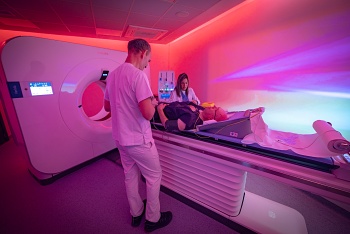
Verida Spectral CT
Fuente: Philips Ibérica / Europa Press
La combinación de PADCEV™ más pembrolizumab está aprobada para el tratamiento de pacientes adultos con cáncer urotelial localmente avanzado o metastásico (la/mUC) en Estados Unidos, la Unión Europea, Japón y otros países del mundo. PADCEV™ también está aprobado a nivel global en monoterapia para el tratamiento de adultos con la/mUC que hayan recibido previamente un inhibidor de PD-1/PD-L1 y quimioterapia con platino, o que no sean candidatos a quimioterapia basada en cisplatino y hayan recibido una o más líneas de tratamiento previas8.
Instalado en España el primer Verida Spectral CT del mundo
Por otro lado, el servicio de RM (resonancia magnética) y TAC (tomografía computarizada) del Hospital Universitario Nuestra Señora del Rosario de Madrid se ha convertido en el primer centro del mundo en instalar el Verida Spectral CT, el nuevo sistema de tomografía computarizada espectral de Philips que combina tecnología espectral basada en detección e Inteligencia Artificial (IA) para ofrecer información anatómica y funcional en un único escáner de baja dosis.
El Verida Spectral CT representa una nueva generación de TAC diseñada para integrar la imagen espectral en la práctica clínica diaria sin añadir complejidad operativa. Gracias a su cadena de imagen impulsada por IA —desde el detector NanoPanel Prism Precise de tercera generación hasta el motor de reconstrucción Spectral Precise Image—, el sistema permite obtener resultados espectrales en todos los estudios, de forma automática y sin pasos adicionales, facilitando diagnósticos más rápidos y precisos en áreas clave como por ejemplo la oncología.
Referencias
1. Neoadjuvant and adjuvant enfortumab vedotin plus pembrolizumab for participants with muscle-invasive bladder cancer who are eligible for cisplatin: randomized, open-label, phase 3 KEYNOTE-B15 study. Abstract #LBA630. 2026 American Society of Clinical Oncology Genitourinary (ASCO GU) Congress.
2. World Bladder Cancer Patient Coalition. GLOBOCAN 2022: Bladder cancer 9th most common worldwide. Accessed January 29, 2026. Available at: https://worldbladdercancer.org/news_events/globocan-2022-bladder-cancer-is-the-9th-most-commonly-diagnosed-worldwide/
3. Bladder Cancer Awareness Network. What is Muscle Invasive Bladder Cancer? Accessed January 29, 2026. Available at: https://bcan.org/what-is-muscle-invasive-bladder-cancer/#:~:text=When%20tumors%20grow%20into%20or,Virginia%20Health%20System%20explain%20MIBC.
4. Sociedad Española de Oncología Médica (SEOM). (2026). Las cifras del cáncer en España 2026. SEOM. https://seom.org/prensa/el-cancer-en-cifras
5. Squires P, Cook EE, Song Y, Wang C, Zhang A, Seshasayee SM, Rogiers A, Li H, Mamtani R. Treatment Patterns, Disease Recurrence, and Overall Survival in Patients with Muscle-Invasive Bladder Cancer after Radical Cystectomy: A Population-Level Claims-Based Analysis. Clinical Genitourinary Cancer. 2025 Nov;102466. https://doi.org/10.1016/j.clgc.2025.102466.
6. National Institute of Health. National Library of Medicine. Perioperative Enfortumab Vedotin (EV) Plus Pembrolizumab (MK-3475) Versus Neoadjuvant Chemotherapy for Cisplatin-Eligible Muscle Invasive Bladder Cancer (MIBC) (MK-3475-B15/ KEYNOTE-B15 / EV-304) (KEYNOTE-B15). ClinicalTrials.gov identifier: NCT04700124. Published January 7, 2021. Updated August 26, 2025. Accessed January 29, 2026. Available at: https://www.clinicaltrials.gov/study/NCT04700124.
7. Challita-Eid PM, Satpayev D, Yang P, et al. Enfortumab vedotin antibody-drug conjugate targeting nectin-4 is a highly potent therapeutic agent in multiple preclinical cancer models. Cancer Res 2016;76(10):3003-13.
8. PADCEV [package insert]. Northbrook, IL: Astellas Pharma US, Inc.




