Redacción Farmacosalud.com
La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) ha concedido la designación de medicamento huérfano a una terapia génica para la esclerosis lateral amiotrófica (ELA) que ha sido desarrollada en la Universidad Autónoma de Barcelona (UAB) y licenciada a la empresa norteamericana Klotho Neurosciences, Inc. Por ahora, el nuevo tratamiento ha sido probado únicamente en modelos murinos. Según la Dra. Assumpció Bosch, científica de la UAB e investigadora principal del estudio centrado en dicho avance, esta terapia génica "no sólo funciona en ratones tratados antes del inicio de la enfermedad, como medida preventiva, sino también cuando éstos ya presentan una reducción de la función neuromuscular, lo cual es muy relevante, ya que muchos fármacos sólo tienen efecto en modelos animales cuando se administran en etapas muy tempranas, cuando aún no se han iniciado los primeros síntomas. Esto es importante, dado que, cuando se diagnostican los posibles candidatos al tratamiento, tales candidatos ya manifiestan los síntomas".
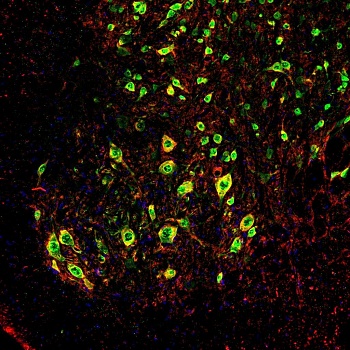
Motoneuronas de médula espinal de ratón
Autoría de la imagen y fuente: UAB
El nuevo fármaco utiliza un vector vírico del tipo AAV (virus adenoasociado) que expresa la isoforma secretada de la proteína Klotho (s-KL), caracterizada por sus propiedades neuro-regeneradoras, antioxidantes y antiinflamatorias. Con el fin de llegar a las uniones neuromusculares afectadas por la ELA, el vector actúa bajo el control de una secuencia de ADN que regula la expresión de la proteína específicamente en el músculo (un promotor específico de músculo), de tal manera que la actividad terapéutica va dirigida hacia las uniones neuromusculares.
KLTO-202
"Tenemos la propiedad intelectual del tratamiento licenciada a la empresa Klotho Neurosciences. En su pipeline, esta terapia recibe el nombre de KLTO-202, pero aún no está aceptada como tratamiento para pacientes. De momento la hemos probado en ratones y se ha otorgado la designación de medicamento huérfano por parte de la FDA, que es lo que ha generado la noticia. Esta designación de medicamento huérfano reconoce el potencial del tratamiento para una enfermedad rara como la ELA", explica Bosch a través de www.farmacosalud.com.
Esta aproximación innovadora ha demostrado resultados muy prometedores en el modelo de ratón más utilizado para el estudio preclínico de la ELA, ya que ha retrasado el inicio de la afección, ha preservado la función neuromuscular y ha prolongado la supervivencia.
La proteína terapéutica, sin toxicidad
En cuanto al perfil de seguridad de KLTO-202, la Dra. Bosch remarca que "la proteína terapéutica no causa ningún tipo de toxicidad, pero los vectores virales sí podrían. Ahora estamos probando si es un tratamiento eficaz en otros modelos de ELA, tanto en otro modelo genético de ratón como en motoneuronas de pacientes, para ver si podría ser aplicable a un número amplio de pacientes, independientemente de si se trata de ELA familiar o esporádica. Una vez confirmado, realizaremos los estudios de toxicidad en los modelos y finalmente se solicitará el ensayo clínico a la FDA".

Dra. Assumpció Bosch
Fuente: UAB / Dra. Bosch
El desarrollo tecnológico de la nueva terapia ha sido liderado por personal investigador de la UAB, con la participación del CIBER, del ICREA y del Vall d’Hebron Instituto de Investigación (Barcelona), que son copropietarios de la propiedad intelectual licenciada a Klotho Neurosciences -compañía start-up basada en conocimiento generado en la UAB y que entró en el Nasdaq en el año 2023-. La tecnología ha sido elaborada por los grupos de investigación de Bosch y de Miquel Chillón, ambos profesionales del Departamento de Bioquímica y de Biología Molecular de la UAB y en el Instituto de Neurociencias de la UAB (INc-UAB).
El proyecto de investigación también ha contado con la colaboración del grupo del investigador del Instituto de Neurociencias Xavier Navarro, experto en neuroregeneración y patologías de la motoneurona.
“La designación de medicamento huérfano para la terapia que hemos desarrollado reconoce la relevancia de los tratamientos dirigidos al músculo y a la unión neuromuscular como estrategia para la ELA”, declara mediante un comunicado la Dra. Bosch. “A fecha de hoy se ha podido demostrar la eficacia en un modelo animal de referencia para esta patología. Ahora lo estamos probando en otros modelos de ELA para confirmar que esta solución terapéutica se podrá aplicar al número más amplio de pacientes posible”, remarca Sergi Verdés, investigador postdoctoral del equipo científico.
Avanzando hacia los primeros ensayos en humanos
La designación de medicamento huérfano por parte de la FDA reconoce el potencial del tratamiento para una enfermedad rara y gravemente discapacitante como la ELA, que afecta a alrededor de 65.000 personas en Europa y para la que actualmente no hay ningún tratamiento eficaz. Este reconocimiento farmacológico ofrece ventajas como siete años de exclusividad del fármaco en el mercado de EE.UU., reducción de tasas y fomento de incentivos fiscales para la realización de estudios clínicos.
Klotho Neurosciences llevará a cabo la producción del vector para iniciar próximamente conversaciones con la FDA y la Agencia Europea del Medicamento (EMA) con el objetivo de avanzar hacia los primeros ensayos en humanos.
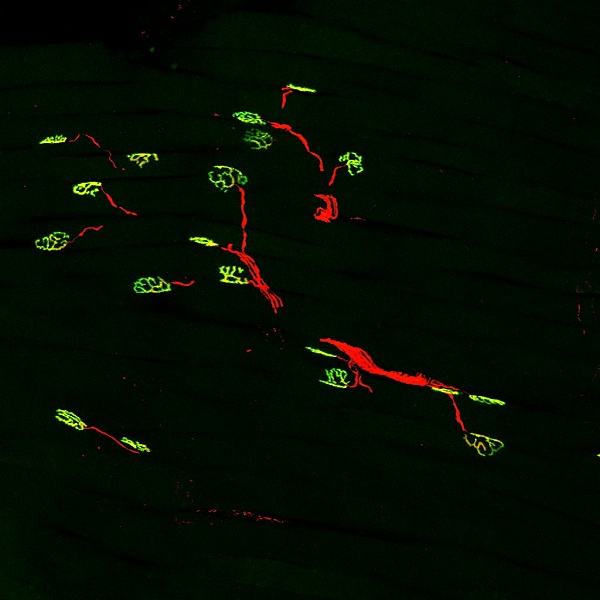
Uniones neuromusculares de ratón
Autoría de la imagen y fuente: UAB




